
早在西汉时期,我国就用铁与硫酸铜溶液反应制取铜,称为“湿法炼铜”。求:
(1)请写出“湿法炼铜”的化学方程式______________。
(2)若用该方法制得铜32 g,反应的铁的质量为多少克?若同时消耗了500 g硫酸铜溶液,则该硫酸铜溶液中硫酸铜的质量分数为多少?(请写出计算过程)
本题考查化学方程式和溶液的有关计算。本题涉及化学反应Fe+CuSO4====Cu+FeSO4,把铜的质量32 g代入方程式求出反应的铁和硫酸铜的质量,然后根据硫酸铜和硫酸铜溶液的质量求出硫酸铜溶液中硫酸铜的质量分数。
答案:(1)Fe+CuSO4====Cu+FeSO4
(2)解:设参加反应的铁的质量为x,500 g硫酸铜溶液中硫酸铜的质量为y。
Fe + CuSO4 ==== Cu + FeSO4
56 160 64
x y 32 g
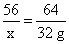 x=28 g
x=28 g 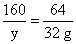 y=80 g
y=80 g
硫酸铜溶液中硫酸铜的质量分数为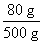 ×100%=16%
×100%=16%
答:反应的铁的质量是28 g,硫酸铜溶液中硫酸铜的质量分数为16%。


科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
(6分)早在西汉时期,我国就用铁与硫酸铜溶液反应制取铜,称为“湿法炼铜”。。求:
(1)请写出“湿法炼铜”的化学方程式 。
(2)若用该方法制得铜32g,反应的铁的质量 g,若同时消耗了500g硫酸铜溶液,则该硫酸铜溶液中硫酸铜的质量分数为 %。
查看答案和解析>>
科目:初中化学 来源:2014年鲁教版九年级化学下册 9.2 金属的化学性质练习卷(解析版) 题型:填空题
早在西汉时期,我国就用铁与硫酸铜溶液反应制取铜,称为“湿法炼铜”。
(1)请写出“湿法炼铜”的化学方程式???????????????????????????? 。
(2)若用该方法制得铜32 g,反应的铁的质量为????? g,若同时消耗了500 g硫酸铜溶液,则该硫酸铜溶液中硫酸铜的质量分数为? ????? %。
查看答案和解析>>
科目:初中化学 来源:2011年全国中考真题专题汇编专题六化学方程式计算(一) 题型:填空题
(2011四川宜宾,17题)早在西汉时期,我国就用铁与硫酸铜溶液反应制取铜,称为“湿法炼铜”。求:
⑴请写出“湿法炼铜”的化学方程式: 。
⑵若用该方法制得铜32g,反应的铁的质量 g,若同时消耗了500g硫酸铜溶液,则该硫酸铜溶液中硫酸铜的质量分数为 %。
查看答案和解析>>
科目:初中化学 来源:2013年四川省广元市中考化学模拟试卷(一)(解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com