
【题目】如图为A、B、C三种固体物质(不含结晶水)的溶解度曲线.下列说法错误的是( )
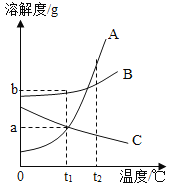
A. t1℃时,三种物质中B的溶解度最大
B. t2℃时,三种物质的饱和溶液中,溶质质量分数最大的是A
C. 可用降低温度的方法使t2℃时C的饱和溶液变为不饱和溶液
D. t1℃时,将等质量A、C不饱和溶液分别用添加溶质的方法形成饱和溶液,所加的溶质质量相等
 中考解读考点精练系列答案
中考解读考点精练系列答案科目:初中化学 来源: 题型:
【题目】图a是铯元素在元素周期表中的信息,图b是铝原子结构示意图,图C为元素周期表的一部分,X、Y、Z代表三种不同元素.
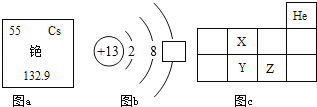
(1)由图a可知,铯元素它属于_____(填“金属”或“非金属”),该元素的原子核外电子数为_____,图中的132.9表示铯元素的_____.
(2)图b方框内的数字是_____;该原子在化学反应中容易_____(填“得到”或“失去”)电子,形成稳定结构,其离子符号为_____.
(3)有关图C的说法,正确的是_____(填序号).
A 原子序数:Z>Y B 核外电子数:X=Y C Y和Z同处于第二周期.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】尿素[CO(NH2)2]是一种常用的化肥,工业上生产尿素的反应的微观示意图如图,请据图回答下列问题:
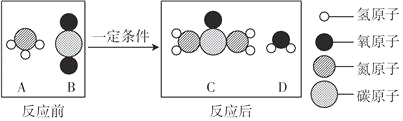
(1)图中属于氧化物的有_____(填化学式)。
(2)该反应的化学方程式为_____。
(3)鉴别尿素与氯化铵的方法为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
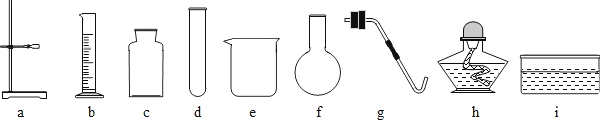
【题目】某实验小组在实验室中用高锰酸钾受热分解制取氧气.
(1)写出该反应的化学方程式______.
(2)为组装制取氧气的装置(包括收集装置),请你从如图中选择所需的仪器,(填序号,下同)______.装药品前应首先______.
(3)实验室里还可采用如图装置,通过分解过氧化氢(H2O2)的方法制取氧气.
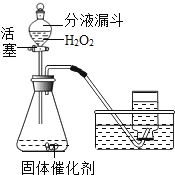
写出该反应化学方程式:______收集氧气的方法还可以用______.
(4)比较两种方法,后一种方法的主要优点是:______.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)如图为电解水的实验。

①.当电源开关闭合后,发生反应的化学方程式为_____
②乙图所示的现象与实验事实不相符,请指出不相符的地方是_____。
(2)如图是探究燃烧条件的实验,图示的现象与实验事实不相符,火焰出现的地方应该是_____(填“a”、“b”或“c”)点,该反应的化学方程式为:_____
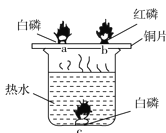
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用珍珠加工成的“珍珠粉”是一种名贵中药材、保健品,可近年来市场上出现了一些假冒的“珍珠粉”,仅用肉眼观察难辨真假.为了向消费者提供鉴别方法,须找出真假“珍珠粉”理化性质上的差异.为此,某工商局提供了真、假“珍珠粉”样品和有关真假珍珠粉的资料如表:
品种 | 外观 | 成分 | 制作过程 |
真珍珠粉 | 白色无味粉末 | 主要为碳酸钙,可能含少量碳酸镁、壳角蛋白等. | 直接将珍珠磨成粉末. |
假珍珠粉 | 白色无味粉末 | 贝壳粉(主要成分为CaCO3),可能含少量碳酸镁并掺有少量淀粉. | 将贝壳漂白(漂白过程中用到过NaOH),然后磨成粉末. |
其中,真珍珠粉中的壳角蛋白(蛋白质的一种)不溶于水,加入浓硝酸加热后会变黄色.某研究性学习小组对提供的真假珍珠粉进行了如下探究.
(探究一)对真假珍珠粉的初步鉴定:
(1)真、假珍珠粉均属于_____(“纯净物”或“混合物”).取少量珍珠粉样品于试管中,加入_____并加热,若观察到变黄色,则该样品是真珍珠粉.
(2)另取少量市售廉价珍珠粉于试管中,加入足量水振荡后静置,将上层清液分别倒入2支试管中,向一支试管中滴加_____,混合液变成蓝色,说明其中掺有淀粉;再向另一支试管中加入1~2滴_____,溶液变成微红色,说明在漂白贝壳的过程中用到过氢氧化钠,使溶液呈碱性.
(探究二)测定市售珍珠粉中碳酸钙的质量分数:
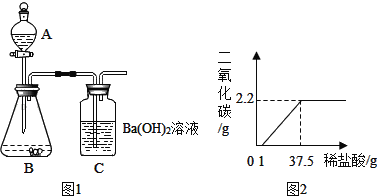
步骤Ⅰ:连接仪器组成如图1所示实验装置.某学生堵住C末端玻璃导管口,在A中装入少量水并取下上部塞子,打开玻璃活塞,A中水不能全部滴下,你认为该装置是否漏气?_____(填“漏气”或“不漏气”)
步骤Ⅱ:准确称取5.00g珍珠粉样品装入仪器B中,在A中装入一定浓度的稀盐酸.
步骤Ⅲ:向B中珍珠粉样品中滴加足量的稀盐酸.在仪器B、C中可观察到的现象分别为_____、_____.
步骤Ⅳ:完全反应后C中的混合液经_____、_____、干燥,称得白色固体的质量为9.85g(不考虑装置中原有空气及装置外空气的影响),由此求得珍珠粉样品中碳酸钙的质量分数为100%.
(实验反思)这个测定结果令研究小组的同学们感到难以理解,经过讨论分析,大家认为可能的原因是_____.(填数字序号)
①样品中含有碳酸镁 ②盐酸未滴加足量
③CO2气流速度太快导致未被Ba(OH)2完全吸收 ④装置B中水蒸气、HCl等进入装置C中
(拓展延伸)同学们根据测定数据计算出样品中碳酸根离子的质量分数为_____%.
有同学提出在探究二中不需要装置C,只要用电子天平准确称量装置A、B反应前后的总质量,也可以求得珍珠粉样品中碳酸根离子的质量分数.你认为这样求得的碳酸根离子的质量分数与上面所得数值相比,将会_____(填“不变”、“偏大”或“偏小”).后来,同学们经过精确测定,得到所加稀盐酸与产生的二氧化碳气体质量关系如图2所示.
(分析讨论)
(1)在加入稀盐酸的过程中,开始没有气体产生,是因为固体样品中还含有少量_____(填“碳酸镁”或“氢氧化钠”)的缘故.
(2)根据图示,求出所用稀盐酸的溶质质量分数____?(需有计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硫酸铝铵晶体(NH4Al(SO4)2·xH2O)是一种用途广泛的含铝化合物。兴趣小组在科研人员指导下,设计实验研究硫酸铝铵晶体受热分解的产物。
(查阅资料)①SO2可与稀KMnO4溶液反应使其褪色。
②SO3+H2O=H2SO4。
③硫酸铝铵热分解可得到纳米氧化铝。
④碱石灰是CaO和NaOH的混合物。
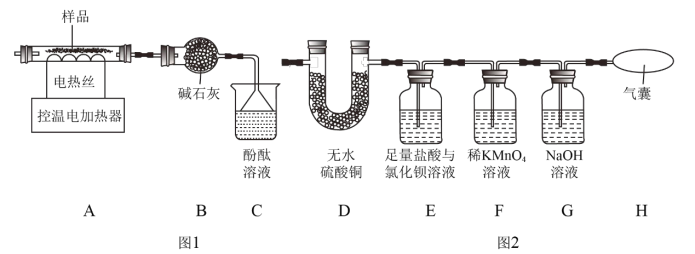
(1)硫酸铝铵晶体分解产物的定性探究
①装置C中观察到酚酞溶液变红色,由此可知分解的产物中有_____(写化学式)。
②某同学认为硫酸铝铵晶体受热分解的产物中还有H2O、SO2、SO3和N2。为进行验证,用图1中的装置A和图2所示装置连接进行实验。实验中,装置D中现象是_____,证明有H2O生成;装置E中现象是_____,证明有SO3生成;而装置F中现象是_____、H最终没有胀大,证明没有SO2和N2生成。
(2)硫酸铝铵晶体成分及分解产物的定量探究为确定硫酸铝铵晶体的组成,称取45.3g样品在空气中持续加热,测定剩余固体质量随温度变化的曲线如图所示。
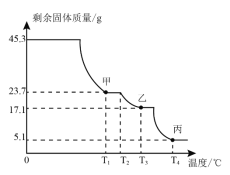
①固体甲是T1℃刚好完全失去结晶水的产物,则x=_____。
②T3℃时固体乙的成分是_____(填字母)。
A Al2(SO4)3
B Al(OH)3
C Al2(SO4)3和Al(OH)3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“卓筒井”是手工制盐的活化石,是我国古代劳动人民勤劳、智慧的象征。其工艺流程包括下面五个步骤:钻井→汲卤→晒卤→滤卤→煎盐。请回答下列问题:
(1)上述步骤中,_____与实验室过滤的原理一样,“煎盐”和实验室_____结晶的原理相同。
(2)“汲卤”获得卤水主要成分是氯化钠与氯化钾,卤水中氯化钠的质量分数大约为 7%~10%,“晒卤”目的是_____;“煎盐”得到的食盐中含有氯化钾,实验室可用_____检验,操作方法是_____。
(3)下列数据是氯化钠和氯化钾固体在不同温度时的溶解度。
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度 g/100g 水 | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
KCl | 27.6 | 34.0 | 40.0 | 45.5 | 51.1 | 56.7 | |
根据表中数据可得出:40℃时,氯化钠溶解度_____氯化钾溶解度(填:大于、小于、等于); 氯化钠与氯化钾溶解度相同的温度范围是_____;20℃时,100g 卤水氯化钠的质量分数为 9%,含氯化钾 1.00g,蒸发掉水大于_____g,开始有氯化钠析出。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上采用离子交换膜电解槽电解饱和食盐水,可得到高浓度的烧碱溶液(含NaOH 35%~48%),某兴趣小组欲验证一化工厂生产的NaOH溶液是否达到了高浓度标准,进行了如下操作,请你参与计算:
(1)用37%的浓盐酸配制200g7.3%的盐酸,需要加水mL?(密度为1gmL-1)(计算结果保留一位小数)____
(2)采集该化工厂电解槽中的NaOH溶液20g,向其中滴入所配制的盐酸,当溶液的pH=7时,消耗盐酸100g,判断电解槽中NaOH溶液是否达到高浓度标准?____
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com