
【题目】以下是初中化学一些常见物质间互相转化的关系图(有些反应条件已省略):已知高温下CO能与多种金属氧化物反应生成相应的金属和CO2.下列关系图中A、B、X、Y均为无色气体,甲、乙、丙均为黑色固体,E、F为常见金属.

请回答:
(1)A的名称为___;蓝色溶液中溶质的化学式为___.
(2)生成固体甲的化学方程式为___.
(3)固体乙与丙反应的化学方程式为___.
(4)写出图中属于复分解反应的化学方程式___.
(5)固体乙与X的反应,说明X具有___性.
【答案】氢气 H2SO4和CuSO4 3Fe+2O2![]() Fe3O4 C+2CuO
Fe3O4 C+2CuO![]() 2Cu+CO2↑ CuO+H2SO4═CuSO4+H2O 还原
2Cu+CO2↑ CuO+H2SO4═CuSO4+H2O 还原
【解析】
无色液体通电会生成A、B,所以A、B为氢气或氧气中的一种,黑色固体乙与硫酸反应生成蓝色溶液,所以乙为氧化铜,蓝色溶液是硫酸铜,且E与蓝色溶液反应生成浅绿色溶液,所以E为铁,F为铜,都会与B反应,所以B是氧气,黑色固体甲是四氧化三铁,E和硫酸反应生成硫酸亚铁和氢气,又因X为无色气体,且能还原金属氧化物,且生成物也是气体,所以X为一氧化碳,经过验证,推导正确。
由分析可知(1)A是氢气,蓝色溶液中溶质的化学式为:H2SO4和CuSO4;
(2)生成固体甲的反应是铁和氧气在点燃的条件下生成四氧化三铁,化学方程式为:3Fe+2O2![]() Fe3O4;
Fe3O4;
(3)固体乙与丙的反应是氧化铜和碳在高温的条件下生成铜和二氧化碳,化学方程式为:C+2CuO![]() 2Cu+CO2↑;
2Cu+CO2↑;
(4)属于复分解反应的是氧化铜和硫酸反应生成硫酸铜和水,化学方程式为:CuO+H2SO4═CuSO4+H2O;
(5)固体乙与X的反应,说明X具有还原性。


科目:初中化学 来源: 题型:
【题目】(5分)下图是a、b、c三种物质的溶解度曲线,回答下列问题:
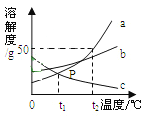
(1)P点的含义是 。
(2)t2℃时,将50ga物质放入50g水中充分溶解得到溶液的质量为 g。
(3)将t2℃时,a、b、c三种物质的饱和溶液降温到t1℃,所得溶液中溶质的质量分 数由大到小的顺序是 。
(4)将t1℃时,将盛有c的饱和溶液的小试管放入盛水的烧杯中(如图),向水中加入一 定量的氢氧化钠固体后,试管中的溶液变浑浊,原因是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上常利用电石制乙炔气体![]() 时产生的灰浆和残渣制备化工原料
时产生的灰浆和残渣制备化工原料![]() 和超细
和超细![]() .
.
![]() 电石制乙炔气体
电石制乙炔气体![]() 时产生灰浆和残渣的过程如下:电石
时产生灰浆和残渣的过程如下:电石![]() 灰浆
灰浆![]() 残渣,其中电石与水反应生成氢氧化钙和乙炔,写出该反应的化学方程式 ______,残渣中主要成分是
残渣,其中电石与水反应生成氢氧化钙和乙炔,写出该反应的化学方程式 ______,残渣中主要成分是![]() 和 ______ .
和 ______ .
Ⅰ![]() 制备
制备![]() 的流程如图:
的流程如图:
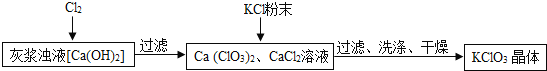
![]() 向灰浆浊液中通入
向灰浆浊液中通入![]() ,得到
,得到![]() 、
、![]() 溶液.反应中
溶液.反应中![]() 与
与![]() 的化学计量数分别为1和
的化学计量数分别为1和![]() 写出此反应的化学方程式 ______ .
写出此反应的化学方程式 ______ .
![]() 有关物质在常温下的溶解度如下:
有关物质在常温下的溶解度如下:
物质 |
|
|
| KCl |
溶解度 |
|
|
|
|
上述流程中加入KCl粉末,KCl与 ______ ![]() 填化学式
填化学式![]() 发生了复分解反应,得到
发生了复分解反应,得到![]() 晶体.你认为能得到
晶体.你认为能得到![]() 晶体的原因是 ______ .
晶体的原因是 ______ .
![]() 洗涤时,可选用下列洗涤剂 ______
洗涤时,可选用下列洗涤剂 ______ ![]() 填字母编号
填字母编号![]() .
.
A KCl饱和溶液![]() 冰水
冰水![]() 饱和
饱和![]() 溶液
溶液
Ⅱ![]() 制备超细
制备超细![]() 的流程如下
的流程如下![]() 注:加入
注:加入![]() 溶液的目的是溶解残渣中的难溶盐
溶液的目的是溶解残渣中的难溶盐![]() :
:
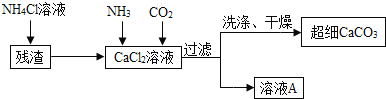
![]() 向
向![]() 溶液中通入两种气体,生成超细
溶液中通入两种气体,生成超细![]() 的化学方程式 ______
的化学方程式 ______ ![]() 检验
检验![]() 是否洗涤干净的方法是 ______ .
是否洗涤干净的方法是 ______ .
![]() 流程中溶液A可循环使用,其主要成分的化学式是 ______ .
流程中溶液A可循环使用,其主要成分的化学式是 ______ .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某干燥剂生石灰久置于空气中,测得其中Ca元素质量分数为60%。说法错误的是
A. 此包干燥剂中一定含有CaO
B. 此包干燥剂中加入盐酸可能会产生气泡
C. 此包干燥剂的组成可能有3种情况
D. 此包干燥剂可能是Ca(OH)2、CaCO3的混合物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列实验对应的图象不正确的是( )
A.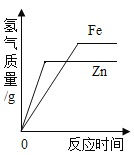 将等质量的锌和铁分别与足量的盐酸反应
将等质量的锌和铁分别与足量的盐酸反应
B.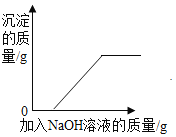 向盐酸和氯化钙的混合溶液中加入过量的碳酸钠溶液
向盐酸和氯化钙的混合溶液中加入过量的碳酸钠溶液
C.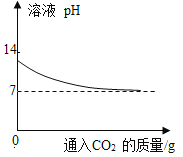 向澄清石灰水中通入适量的CO2气体至与氢氧化钙恰好完全反应
向澄清石灰水中通入适量的CO2气体至与氢氧化钙恰好完全反应
D.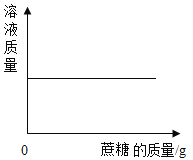 一定温度下,向一定量的饱和NaCl溶液中不断加入蔗糖晶体
一定温度下,向一定量的饱和NaCl溶液中不断加入蔗糖晶体
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】MgSO4和Na2CO3的溶解度表及溶解度曲线如下.下列说法正确的是( )
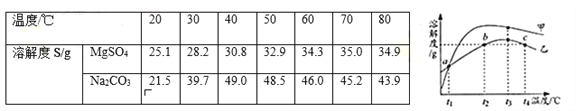
A. 甲为Na2CO3
B. 乙的饱和溶液从t1升温到t4,溶质质量分数增大
C. 等质量甲、乙饱和溶液从t3降温到t1,析出晶体的质量(不带结晶水):乙>甲
D. b、c点乙的饱和溶液溶质质量分数相等,且大于a点甲的饱和溶液溶质质量分数
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请结合下图回答问题:
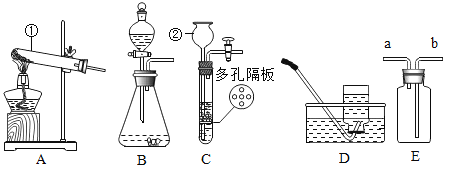
(1)仪器名称:①______,②______。
(2)用氯酸钾和二氧化锰制取氧气,可选用装置______(选填序号)和D组合,反应的化学方程式为______,二氧化锰的作用是______,当D装置出现______现象时表明氧气已经集满。
(3)实验室可用装置B或C制H2,制取氢气的化学方程式为______,C装置相对于B的优点有______。用E装置收集H2,气体应从____(选填“a”或“b”)端通入。
(4)有同学将实验室制得的CO2通入澄清石灰水,石灰水未变浑浊,于是作如图探究:
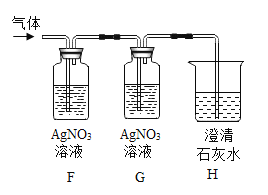
①实验室制CO2反应的化学方程式______。
②装置F、H中溶液变浑浊,G中溶液不变浑浊,则原石灰水未变浑浊的原因是______。
③装置G的作用是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】科学家研发出一种以铝镓(镓:Ga)合金和水为原料制取氢气的新工艺,流程如图所示:
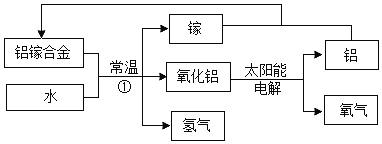
(1)铝镓合金是_______。(填“纯净物”或“混合物”)
(2)反应①中镓的作用可能是_____,与电解水制取氢气相比,该方法的优点是:_____(答一条)。
(3)请写出电解氧化铝的化学反应方程式:_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室用辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2)制备碱式碳酸铜的主要实验流程如下。已知:二氧化硅不溶于水,也不溶于酸。
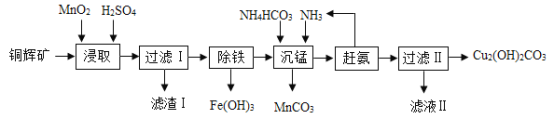
(1)浸取前辉铜矿粉碎成细颗粒,目的是________;
(2)硫酸浸取时,Cu2S被MnO2氧化的化学方程式为2MnO2 + Cu2S + 4H2SO4 = 2MnSO4 + 2CuSO4 +S+4______。滤渣Ⅰ的成分为MnO2、单质S和______(写化学式);
(3)浸取时,Fe2O3溶于硫酸反应的化学方程式为____;研究发现若先除铁再浸取,浸取速率明显变慢,其可能原因是_____;
(4)沉锰时温度不宜过高,除了防止氨水挥发外,还能______;
(5)“赶氨”时,最适宜的操作方法是____,以减小氨气的溶解度;
(6)滤液Ⅱ中溶质主要是(NH4)2SO4,要得到其晶体可采用蒸发浓缩、______、过滤晾干;
(7)经过滤得到的产品碱式碳酸铜需要洗涤、烘干,其中洗涤的方法是向盛有碱式碳酸铜固体的过滤器中加入______,(填字母序号)重复几次即可洗净;
a Na2CO3溶液
b 蒸馏水
c 稀盐酸
(8)检验产品是否洗涤干净的方法:取最后一次洗涤液,__(①滴加稀盐酸、② 滴加Na2SO4 溶液、③ 滴加BaCl2溶液,填写序号),如果无明显的现象,说明已经洗涤干净。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com