
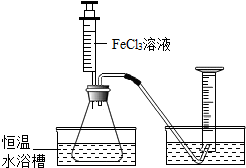
 FeCl3溶液对过氧化氢的分解起催化作用,某小组拟在相同浓度FeCl3溶液的催化下,探究过氧化氢浓度对过氧化氢分解速率的影响.
FeCl3溶液对过氧化氢的分解起催化作用,某小组拟在相同浓度FeCl3溶液的催化下,探究过氧化氢浓度对过氧化氢分解速率的影响.| 序号 | H2O2溶液的体积/mL | H2O2溶液的浓度/% | 2%FeCl3溶液的体积/mL | 反应的时间/min | 生成O2的体积m/L |
| 1 | 10 | 30 | x | 5 | V1 |
| 2 | 10 | 15 | 3 | y | V2 |
分析 根据已有的知识进行分析解答,从定性的方面,观察反应速率就可知过氧化氢浓度对过氧化氢分解速率的影响;根据方案一,得出方案二探究的内容;根据实验目的和方案得出xy的值以及实验结论.
解答 解:【定性探究】要定性比较二者的反应速率,可以分别取相同体积、不同浓度的过氧化氢溶液于锥形瓶中,注入相同体积、相同浓度的FeCl3溶液,根据反应产生气泡的快慢就可得出结论;故填:产生气泡的快慢;
【方案二】在不同过氧化氢浓度下,可以测定相同时间收集气体的体积;故填:相同时间收集气体体积的多少;
分析方案二的实验测量结果,可得控制变量x=3,y=5;故填:3,5;
实验结论:通过测量,若V1>V2,可得出结论:在其他条件相同的情况下过氧化氢溶液浓度越大反应速率越快.故填:>;在其他条件相同的情况下过氧化氢溶液浓度越大反应速率越快.
点评 培养观察记录实验现象,分析实验结果和处理实验数据,得出正确结论的能力;学会归纳总结、对比分析.


 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:初中化学 来源: 题型:填空题
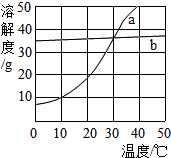 如图为a、b两种物质在水中的溶解度曲线.
如图为a、b两种物质在水中的溶解度曲线.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 18g | B. | 24 g | C. | 28 g | D. | 50 g |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验 编号 | 温度 | 盐酸 浓度 | 铝片消失的时间/s |
| ① | 20℃ | 5% | 60 |
| ② | 20℃ | 10% | 42 |
| ③ | 40℃ | 10% | 30 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
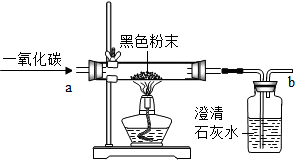 在探究课上,老师给同学们一包黑色粉末,该粉末是由铁粉和氧化铜粉末中的一种或两种组成,为了确定该粉末的成分,同学们进行如下探究,请回答下列问题:
在探究课上,老师给同学们一包黑色粉末,该粉末是由铁粉和氧化铜粉末中的一种或两种组成,为了确定该粉末的成分,同学们进行如下探究,请回答下列问题:| 实验中可能出现的现象 | 结论 |
| 黑色粉末不变红,澄清的石灰水不变浑浊 | 猜想(1)成立 |
| 黑色粉末全部变红,澄清的石灰水变浑浊 | 猜想(2)成立(填成立或不成立) |
| 黑色粉末部分变红,澄清的石灰水变浑浊 | 猜想(3)成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
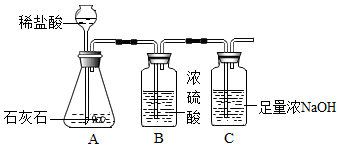
| 时间/分 | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 |
| 大理石碎屑生成的CO2质量/克 | 0 | 1.45 | 1.75 | 1.98 | 2.18 | 2.30 | 2.36 | 2.40 | 2.40 | 2.40 |
| 块状大理石生成的CO2质量/克 | 0 | 0.45 | 0.80 | 1.10 | 1.36 | 1.60 | 1.81 | 1.98 | 2.11 | 2.20 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
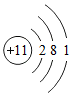 ,下列说法正确的是( )
,下列说法正确的是( )| A. | 该原子属于非金属元素的原子 | B. | 该原子形成离子后电子层数不变 | ||
| C. | 该原子的核外电子数为1 | D. | 该原子在化学反应中易失去电子 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 地球上水量丰富,水资源是取之不尽用之不竭的 | |
| B. | 过滤可以除去水中不溶性的固体杂质 | |
| C. | 净化水的操作中,净化程度最高的是蒸馏 | |
| D. | 向水中加入吸附剂(如活性炭等)可以除去水中的部分杂质,但不能降低水的硬度 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com