
【题目】用“侯氏制碱法”值得的纯碱常含有少量的氯化钠(假定只含有氯化钠杂质).称量某纯碱样品12g,全部溶解在100g水中,所得溶液与160g氯化钙溶液混合,恰好完全反应.过滤干燥后,称得沉淀质量为10g.请计算:
(1)纯碱样品中碳酸钠的质量分数____.
(2)反应后所得滤液中溶质的质量分数____.
科目:初中化学 来源: 题型:
【题目】利用如图所示装置进行实验。从A或B中任选一个作答,若均作答,按A计分。
A | B |
A处观察到的现象为________,产生该现象的原因为________。 |
A处观察到的现象为_______,产生该现象的原因为________。 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某元素的离子结构示意图如图所示,该元素的离子符号为Br﹣。
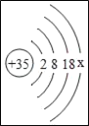
(1)图中x=_____,Br属于_____元素(填“金属”或“非金属”),
(2)如图表示的微粒中,具有相似化学性质的几种微粒是_____。(填序号)以下微粒中与溴元素化学性质相似的是_____。(填序号)
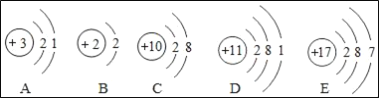
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是
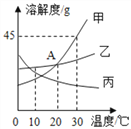
A. A点表示20℃时甲、乙溶解度相等
B. 30℃时,30g甲物质中加入50g水,充分溶解后得到72.5g溶液
C. 甲中混有少量丙,可用冷却热饱和溶液的的方法提纯甲
D. 将30℃时甲、乙、丙三种物质的饱和溶液分别降温到10℃,它们的溶质质量分数都发生改变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某实验小组欲配制200g溶质质量分数为10%的氢氧化钠溶液,按下述步骤操作,请填空:
(1)计算:需要氢氧化钠___g,水___mL.
(2)称量:调节天平平衡后称量所需的氢氧化钠时,发现托盘天平的指针偏右,此时应___(填序号).
A 增加适量的氢氧化钠 B 减少适量的氢氧化钠 C 调节天平的平衡螺母
(3)配制溶液:用量筒量取所需的水,倒入盛有氢氧化钠的烧杯中,用玻璃棒搅拌其目的是____.这样得到200g 10%的所需溶液.
(4)若要使溶液的溶质质量分数增加一倍,应向此溶液中加入氢氧化钠__g,或蒸发掉水___g.
(5)氢氧化钠溶液的pH>7,要减小其pH值可以采取哪些不同的措施,请列举三项:___;___;___.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】废旧电路板中主要含有塑料、铜和锡(Sn)等,为实现对其中锡的绿色回收,某工艺流程如下。已知:Sn+SnCl4=2SnCl2。
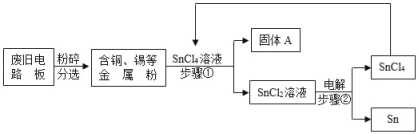
(1)步骤①的操作是_____。
(2)固体A中一定含有的金属元素是_____(填元素符号)。
(3)写出步骤②发生反应的化学方程式_____,该流程中可以循环利用的物质是_____。
(4)相比于直接焚烧废旧电路板回收金属,该工艺主要优点是_____(回答一点即可)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】推断题
A~H是初中化学常见的物质。其中A为黑色固体,H为红色固体,E为生活中最常用的金属单质,B、C、D均为无色气体,F为石灰石的主要成分,G为蓝色溶液。他们之间有下图的转化关系且均可一步完成(部分生成物已省去)
请根据图示回答下列问题
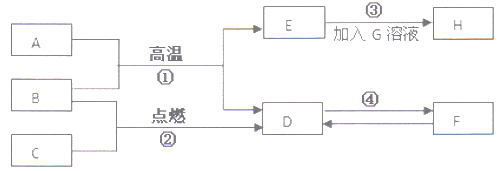
(1)A的化学式为____________,③的反应类型为____________。
(2)反应③的化学方程式____________。
(3)反应④的化学方程式____________。
(4)实验室制取D时,为什么不能用碳酸钠? ____________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学兴趣小组为验证质量守恒定律,他们在老师指导下,做了镁条在空气中燃烧的实验。
(1)写出镁条与氧气反应的化学方程式:_____。
(2)小华发现燃烧所得固体的质量大于消耗的镁条质量,他据此认为该反应不遵循质量守恒定律。你_____(同意”或“不同意”)小华的观点,理由是_____。
(3)小红按如图装置进行实验,验证了质量守恒定律,却发现产物中还有少量黄色固体。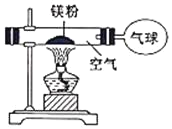
(提出问题)黄色固体是什么物质?
(查阅资料)①镁与氮气反应生成黄色的氮化镁(Mg3N2)固体;②氮化镁可与水剧烈反应产生氨气。
(做出猜想)黄色固体为氮化镁。
(实验探究)请你设计实验,验证猜想:
实验操作 | 实验现象 | 实验结论 |
取足量的黄色固体加入试管,然后滴入适量的_____,并将_____放在试管口 | _____ | 猜想正确 |
(反思与交流)
①通过上述探究活动,你对燃烧有什么新认识:_____。
②空气中氮气的含量远大于氧气的含量,而镁条在空气中燃烧生成的氧化镁却远多于氮化镁,这是因为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com