
【题目】某实验小组欲配制200g溶质质量分数为10%的氢氧化钠溶液,按下述步骤操作,请填空:
(1)计算:需要氢氧化钠___g,水___mL.
(2)称量:调节天平平衡后称量所需的氢氧化钠时,发现托盘天平的指针偏右,此时应___(填序号).
A 增加适量的氢氧化钠 B 减少适量的氢氧化钠 C 调节天平的平衡螺母
(3)配制溶液:用量筒量取所需的水,倒入盛有氢氧化钠的烧杯中,用玻璃棒搅拌其目的是____.这样得到200g 10%的所需溶液.
(4)若要使溶液的溶质质量分数增加一倍,应向此溶液中加入氢氧化钠__g,或蒸发掉水___g.
(5)氢氧化钠溶液的pH>7,要减小其pH值可以采取哪些不同的措施,请列举三项:___;___;___.
【答案】20 180 A 搅拌,加速溶解 25 100 加水稀释 加盐酸 加硫酸铜溶液
【解析】
(1)200g10%的氢氧化钠溶液中氢氧化钠的质量为:200g×10%=20g,该溶液中溶剂水的质量为:200g﹣20g=180g;
(2)用托盘天平称量10克药品的步骤是:调节天平平衡,放上砝码,再向左盘加入药品,在称量中发现指针向右偏,说明药品不足,所以要增加药品,故选:A;
(3)溶解氢氧化钠要用玻璃棒搅拌,目的是加快氢氧化钠的溶解速度;
(4)若要使溶液的溶质质量分数增加一倍,设应向此溶液中加入氢氧化钠的质量为x,
![]()
x=25g
蒸发掉水的质量为:200g﹣![]() =100g;
=100g;
(5)要减小碱性溶液的pH值,可以稀释溶液,也可以消耗氢氧根离子,所以可以采取的措施有:加水稀释,加盐酸,加硫酸铜溶液。


科目:初中化学 来源: 题型:
【题目】阅读下面科普短文。
2019年为“国际化学元素周期表年”。我国青年学者姜雪峰教授被IUPAC遴选为硫元素代言人。
说起硫,大家想到最多的是SO2和酸雨,实际上生活中硫和硫的化合物应用很广泛。单质硫是一种黄色晶体,所以又称作硫磺,难溶于水,易溶于二硫化碳。硫磺有杀菌作用,还能杀螨和杀虫,常加工成胶悬剂,防治病虫害。在药物中,硫元素扮演着重要角色,其仅位列于碳、氢、氧、氮之后。含硫化合物也存在于许多食物中,如大蒜中的大蒜素(C6H10S2O),虽然气味不太令人愉快,但其对一些病毒和细菌有独特的抑制和杀灭作用。含硫化合物在材料科学中也有广泛用途,其中聚苯硫醚是含硫材料的杰出代表之一,它具有良好耐热性,可作烟道气过滤材料。含硫化合物还有很多其他用途,如某些硫醇的气味极臭,可用于煤气泄露的“臭味报警”。甲(或乙)硫醇在空气中的浓度达到500亿分之一时,即可闻到臭味。因此,煤气和液化石油气里会掺进每立方米20 mg的甲硫醇或者乙硫醇,充当报警员,防止灾害的发生。
硫元素在自然界中以硫化物、硫酸盐或单质形式存在,其循环如图1所示。硫矿是一种很重要的资源,世界各国硫矿资源分布不均(见图2)。随着科学的发展,硫元素的神奇性质将会被进一步发展和应用。
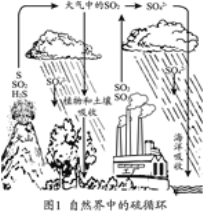

(原文作者范巧玲、姜雪峰,有删改)
依据文章内容回答下列问题。
(1)单质硫的物理性质有________(写出1条即可)。
(2)大蒜素中硫元素的质量分数为________(写出计算式即可)。
(3)大气中二氧化硫的来源主要有_________。
(4) 甲硫醇或者乙硫醇掺进煤气和液化石油气里,可充当报警员,利用的性质是_______。
(5)下列说法正确的是_______(填序号)。
A.硫元素属于金属元素
B.硫磺能杀菌、杀螨、杀虫
C.中国硫矿资源占有量为世界第二
D.硫元素在药物、食品、材料等方面扮演重要角色
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硫酸钾和碳酸钾的混合物5g,其中碳元素的质量分数为4.8%。一定温度下,向盛有该混合物的烧杯中加入一定量稀硫酸,恰好完全反应,得到该温度下硫酸钾不饱和溶液102g。请计算:
(1)所得溶液中溶质的质量;
(2)所用硫酸溶液的质量。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在探究铁、铜、锌、银的金属活动性顺序时,小组同学设计了如下实验:(所用金属的形状与大小和稀盐酸的用量及浓度均相同)。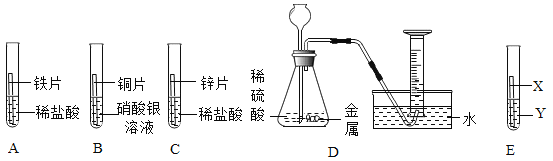
①一段时间后,可明显观察到实验B的现象是_____,反应的化学方程式是_____。
②甲同学认为通过观察A和C中_____实验现象来比较锌与铁的金属活动性;乙同学拟用定量的方法测定锌和铁的活动性强弱,设计如图D,可以测定_____来确定。
③丙同学认为上述实验方案不足以得出4种金属活动性顺序,需要在上述实验基础上,补充实验E,其中X金属是_____,Y溶液是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有A、B、C、D、E、F、G七种物质,C、F是生活中最常见的金属,E的浓溶液有吸水性,B是气体单质,D为浅绿色溶液,G为蓝色溶液,它们之间存在如下关系:
(1)推测下列物质的化学式:B_____,F_____。
(2)写出下列转化的化学方程式:C→A_____;C+E→:_____。
(3)在上述关系图中,所发生的反应属于置换反应类型的共有_____个(填数字)。

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用“侯氏制碱法”值得的纯碱常含有少量的氯化钠(假定只含有氯化钠杂质).称量某纯碱样品12g,全部溶解在100g水中,所得溶液与160g氯化钙溶液混合,恰好完全反应.过滤干燥后,称得沉淀质量为10g.请计算:
(1)纯碱样品中碳酸钠的质量分数____.
(2)反应后所得滤液中溶质的质量分数____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图象不能正确反映其对应变化关系的是( )
A.  向等质量的氧化镁、氢氧化镁中,分别加入质量分数相同的稀盐酸至过量
向等质量的氧化镁、氢氧化镁中,分别加入质量分数相同的稀盐酸至过量
B.  某温度时,向一定量的饱和石灰水中加入足量的生石灰
某温度时,向一定量的饱和石灰水中加入足量的生石灰
C. 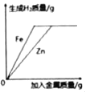 向两份完全相同的稀盐酸中分别加入过量Zn粉、Fe粉
向两份完全相同的稀盐酸中分别加入过量Zn粉、Fe粉
D. 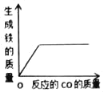 一氧化碳还原一定质量的氧化铁
一氧化碳还原一定质量的氧化铁
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列化学用语表达正确的是( )
A. 2Na:“2”表示两个钠元素
B. 氯化银的化学式为AgCl2
C. ![]() :“+2”表示一个镁离子带两个单位的正电荷
:“+2”表示一个镁离子带两个单位的正电荷
D. SO2:“2”表示一个二氧化硫分子中含有两个氧原子
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】丁基锂( C4H9Li)是橡胶合成工业中的常用试剂,它是白色粉末熔点﹣95℃、沸点80℃,遇水或空气易自燃。下列关于丁基锂的说法正确的是( )
A. 丁基锂是由4个碳原子、9个氢原子、1个锂原子构成的
B. 丁基锂运输或使用过程中如果发生燃烧,可以用水浇灭
C. 丁基锂中碳元素质量分数为75%
D. 丁基锂中碳氢元素质量比为4:9
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com