
【题目】硫酸和盐酸是实验室常用的试剂。请回答下列问题:

(1)A组试管中都产生H2,若要制得较纯的H2,选稀硫酸而不选盐酸的原因是:_____。
(2)B组试管中实验现象相同,该现象是_____。右侧试管的反应的化学方程式为_____。
(3)鉴别稀硫酸和盐酸的试剂是_____。
【答案】盐酸有挥发性(或盐酸挥发出氯化氢气体使制得的氢气中混有氯化氢气体) 红色固体逐渐溶解,溶液由无色变成黄色 Fe2O3+3H2SO4=Fe2(SO4)3+3H2O 硝酸钡溶液(合理即可)
【解析】
(1)盐酸有挥发性,挥发出来的氯化氢气体使制得的氢气中混有氯化氢气体,会影响氢气的纯度,故填盐酸有挥发性(或盐酸挥发出的氯化氢气体使制得的氢气中混有氯化氢气体)。
(2)氧化铁与盐酸反应生成氯化铁和水,与硫酸反应生成硫酸铁和水,氯化铁与硫酸铁均溶于水,且水溶液均呈黄色,所以观察到的现象是红色固体逐渐溶解,溶液由无色变成黄色,故填红色固体逐渐溶解,溶液由无色变成黄色;
右侧试管中的反应是氧化铁与硫酸反应生成硫酸铁与水,故反应的化学方程式写为:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O。
(3)稀硫酸和盐酸中的酸根离子不同,区别两种溶液时,可向两种溶液中滴加硝酸钡溶液,产生白色沉淀的是稀硫酸,无明显变化的是盐酸,故填硝酸钡溶液。


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:初中化学 来源: 题型:
【题目】向CuSO4溶液中加入一定量NaHCO3,产生大量气泡和绿色固体,溶液逐渐变为无色。
(1)将产生的气体通入澄清石灰水,变浑浊,则该气体为__________。
(2)某同学经过滤、洗涤等操作得到绿色固体和无色溶液,并进行如下探究。
[资料]常见绿色固体有碱式碳酸铜[Cu2(OH)2CO3]和碱式硫酸铜[Cu4(OH)6SO4],都不溶于水,但能与酸反应。Na2SO4固体受热不易分解。
I.绿色固体成分的探究
[实验1]取洗净后的绿色固体,加入足量的_________溶液,产生大量气泡,振荡后滴加___________,无现象,则该固体只含碱式碳酸铜。
II.溶液成分的探究
[猜测]取一定量溶液经蒸发、低温干燥等操作得到白色固体,作如下猜测:白色固体可能是:①Na2SO4 ②NaHCO3 ③Na2SO4和NaHCO3
[实验2]取该白色固体8.4g充分加热至质量不再改变为止,测得剩余固体的质量_______( 选填“<”、“=”或“>”)5.3g,则猜测①、②、③都不成立。
[实验3]有同学查阅资料得知上述固体应为Na2SO410H2O和NaHCO3的混合物。为进一步确定白色固体的组成,该同学取适量白色固体,充分加热至质量不再改变,并使产生的气体全部缓缓通过下图_______(选填 “甲”或“乙”)装置,测定生成气体的质量。

[数据]①浓硫酸增重2.7g;②碱石灰增重2.2g。则固体中各成分的质量比为_____________。
[结论]写出CuSO4溶液和NaHCO3溶液反应的化学方程式_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】回答下列与金属有关的问题。
(1)黄铜片与铜片互相刻划目的是_____;
(2)铝比铁活泼,但抗腐蚀性能却更强,用化学方程式解释其原因_____;
(3)工业上,把赤铁矿冶炼成铁的主要反应原理是3CO+Fe2O3![]() 2Fe+3CO2,其中_____发生了氧化反应。
2Fe+3CO2,其中_____发生了氧化反应。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请按要求用符号完成下面问题:
(1)标出硫酸铵中氮元素的化合价__________________________。
(2) 由H、C、O、Na四种元素组成的一种盐的化学式_____________________。
(3)由60个碳原子构成的单质分子_____________________。
(4) 黄铜的主要成分_____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙有如图所示的转化关系(“→”表示反应一步实现,部分物质和反应条件已略去),下列各组物质按照甲、乙、丙的顺序不符合要求的是
![]()
A.C、CO、CO2
B.Fe2O3、 FeCl3、 Fe (OH)3
C.H2O2、 H2O、O2
D.KOH、 K2CO3、 KNO3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用化学方程式解释生活或生产中的现象,下列方程式符合题意且书写正确的是()
A.用硫酸铜配制波尔多液农药会损坏铁桶:![]()
B.服用含Al(OH)2的药物治疗胃酸过多: ![]()
C.利用盐酸除去铁制品表面的铁锈:![]()
D.把含盐酸的洁厕灵滴到大理石地面有气泡:![]()
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】做完加热铜片的实验后,小明同学对其成分进行分析。取10g此样品,向其中分五次加入相同溶质质量分数的稀硫酸,使之充分反应,每次所用稀硫酸的质量及剩余固体的质量记录于下表:
第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
加入稀硫酸的质量/g | 20 | 20 | 20 | 20 | 20 |
充分反应后剩余固体的质量/g | 9.2 | 8.4 | 7.6 | 7 | 7 |
试回答下列问题:
(1)10g样品中氧化铜的质量为__________g。
(2)计算所加入稀硫酸中溶质的质量分数____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C三种不含结晶水的固体物质的溶解度曲线如图所示,下列说法中不正确的是( )
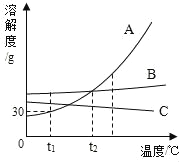
A. t1℃时,A的饱和溶液65g中含有溶剂50g
B. 将t2℃A、B、C三种物质的饱和溶液降温至t1℃时,C溶液中溶质的质量分数保持不变
C. 在t2℃时,A、B两种溶液中溶质的质量分数相同
D. 接近饱和的A溶液中含有少量的杂质B,通常可采用降温结晶的方法来提纯A
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下面的实验过程和提供的数据,回答下列问题。(不考虑反应中水分的蒸发,假设生成的气体全部逸出)
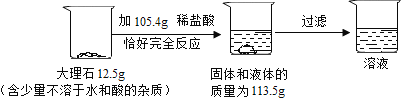
(1)生成的二氧化碳的质量_____g。
(2)过滤后所得溶液中溶质CaCl2 的质量分数_____(精确至0.1%)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com