
【题目】汽车是现代生活中不可缺少的代步工具.请回答下列问题:
(1)汽车电路中的导线多数是用铜制做的,这是利用了金属铜的导电性和性.
(2)下列汽车配件及用品中,用合金制做的是(填字母) . 
(3)铁在潮湿的空气中容易锈蚀. ①汽车表面喷漆,可以延缓汽车的锈蚀,其防锈原理是隔绝空气(氧气)和 .
②喷漆前需将铁制品放人稀盐酸中除锈(铁锈主要成分是Fe2O3),反应初期可观察到溶液由无色变为黄色,这是因为生成了(填化学式)的缘故;反应进行一会儿,又可以观察到有无色气泡产生,该反应的化学方程式是 .
【答案】
(1)延展
(2)a
(3)水;FeCl3;Fe+2HCl═FeCl2 +H2↑
【解析】解:(1)汽车电路中的导线多数是用铜制做的,这是利用了金属铜的导电性和延展性,故填:延展;(2)钢铁的主要成分是铁,还含有碳等物质,属于合金,故填:a;(3)①汽车表面喷漆,可以延缓汽车的锈蚀,其防锈原理是隔绝空气(氧气)和水,故填:水; ②铁锈的主要成分是氧化铁,氧化铁能和稀盐酸反应生成氯化铁和水,氯化铁溶液是黄色的,反应初期可观察到溶液由无色变为黄色,这是因为生成了氯化铁,故填:FeCl3;
铁能和稀盐酸反应生成氯化亚铁和氢气,反应的化学方程式为:Fe+2HCl═FeCl2 +H2↑.
【考点精析】本题主要考查了常见金属的特性及其应用的相关知识点,需要掌握铝:地壳中含量最多的金属元素;钙:人体中含量最多的金属元素;铁:目前世界年产量最多的金属(铁>铝>铜);银:导电、导热性最好的金属(银>铜>金>铝);铬:硬度最高的金属;钨:熔点最高的金属;汞:熔点最低的金属;锇:密度最大的金属;锂 :密度最小的金属才能正确解答此题.


科目:初中化学 来源: 题型:
【题目】最近,科学家找到一种能“记”住四种形状的材料。这种材料是由很多彼此重复或类似的分子组成的聚合物,仅通过改变温度就可改变其形状。则该材料( )
A. 是一种热敏感材料 B. 是一种形状记忆合金
C. 是一种小分子材料 D. 宜用于制造厨房灶具
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】经过一年的初中化学学习,我们认识了许多化学实验仪器,也知道了不少实验操作的要求. 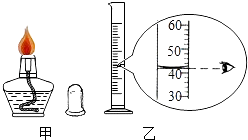
(1)图中,甲是一个燃着的(填仪器名称),用它来进行加热操作时,应使用火焰的焰,当实验结束需停止加热时,应用盖灭.
(2)图中,乙的仪器名称是 , 在量取液体体积时,视线要与仪器内液体的保持水平.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知浓硫酸与焦炭在加热的条件下能发生反应,生成三种氧化物.某校研究性学习小组对此进行以下一系列的探究活动.
【提出猜想】浓硫酸与焦炭在加热条件下反应,生成H2O、SO2和CO2 .
【查阅资料】经查阅资料得知:①CO2、SO2均可使澄清石灰水变浑浊;②SO2可使品红溶液的红色褪去,而CO2不能;③SO2可与酸性的KMnO4溶液反应使其褪色,而CO2不能;④无水CuSO4为白色粉末,遇水可生成蓝色胆矾.
【实验探究】用以下A﹣D四个装置组装成一套完整的实验装置,然后进行实验,验证猜想.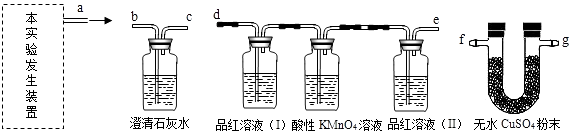
(1)本实验的发生装置应选用如图所示三种装置中的装置(填序号).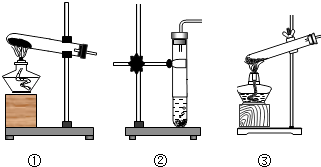
(2)为了验证三种产物,达到预期的实验目的,整套实验装置的正确组装顺序是(按导管口连接的先后顺序) :发生装置导管口![]()
实验过程中,同学们观察到装置D中的无水CuSO4变为蓝色,由此得出产物中有 的结论;同时还观察到以下实验现象:装置C中品红溶液( I)和酸性高锰酸钾溶液都褪色,品红溶液(Ⅱ)不褪色;装置B中澄清石灰水变浑浊.装置C中品红溶液( I)褪色,说明产物中有 ,酸性KMnO4溶液的作用是 ,品红溶液(Ⅱ)不褪色,说明 ;装置B中发生反应的化学方程式是
(3)能确认反应产物中有CO2的实验现象是 .
(4)【实验结论】本实验提出的猜想(填“成立”或“不成立”);
浓硫酸与木炭反应的化学方程式是 .
【交流讨论】实验结束后,同学们针对本实验进行讨论,其中张辉同学提出了“反应产物中可能还有一氧化碳”这样的一个观点.你是否支持张辉同学的观点?(填“支持”或“不支持”),请你说出两点理由:①;② .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】属于置换反应的是( )
A.2H2O2 ![]() 2H2O+O2↑
2H2O+O2↑
B.C+O2 ![]() CO2
CO2
C.Fe+CuSO4═FeSO4+Cu
D.H2SO4+2NaOH═Na2SO4+2H2O
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某课外活动小组为研究由锌和铜组成的黄铜样品中各成分含量,做了以下实验.取黄铜样品粉末20g于烧杯中,将100g19.6%的稀硫酸分2次加入烧杯中(假设每次均充分反应),得到以下数据:
加入稀硫酸的次数 | 第1次 | 第2次 |
加入稀硫酸质量/g | 50 | 50 |
生成气体的质量/g | 0.20 | 0.10 |
已知:锌与稀硫酸反应的化学方程式为Zn+H2SO4=ZnSO4+H2↑,计算:
(1)生成气体的总质量为g.
(2)样品中铜(Cu)的质量为多少?(请写出计算过程)
(3)完全反应后所得溶液总质量为 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列化学方程式符合题意,且书写正确的是( )
A.氢气在空气中燃烧?????????? H2+O2 ![]() H2O
H2O
B.用熟石灰处理污水中的硫酸?? Ca(OH)2+H2SO4═CaSO4+H2O
C.用碳酸钠溶液制烧碱???????? Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
D.用稀硫酸除铁锈???????????? 2H2SO4+Fe2O3═2FeSO4+2H2O
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有一包固体粉末,可能由CaCO3、CaO、Na2CO3中的一种或几种组成.为确定其组成,进行了如图所示的实验(假设实验过程无损耗). 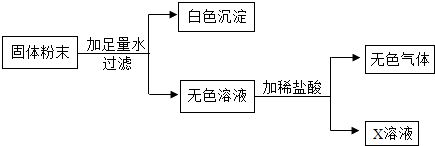
请回答:
(1)根据实验可以确定白色沉淀是;原固体粉末中一定含有 , 它的可能组成有种.
(2)若实验取固体粉末20g,生成白色沉淀10g,最后得到溶质质量分数为5.85%的X溶液200g(只含一种溶质),则X溶液中溶质的质量是g,固体粉末由(填化学式,下同)组成,其中质量小于10g的是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com