
【题目】目前使用的燃料大多来自化石燃料。
(1)写出天然气中甲烷完全燃烧的化学方程式______。
(2)分析下表,与煤相比,用天然气作燃料的优点有______。
1g物质完全燃烧 | ||
产生二氧化碳的质量/g | 放出的热量/kJ | |
甲烷 | 2.75 | 56 |
煤碳 | 3.67 | 32 |
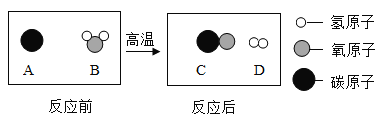
(3)为提高煤的利用率,可将其转化为可燃性气体,该反应的微观示意图如下,则生成物的分子个数比为_____。
科目:初中化学 来源: 题型:
【题目】某兴趣小组同学从实验室中收集到一桶废液,他们想从中回收金属铜和硫酸亚铁,于是设计了以下流程图
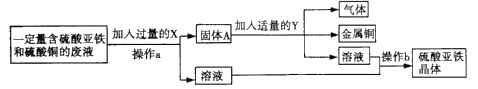
(1)固体A的成分为______;操作a和操作b都要用到一种玻璃仪器,该仪器在操作a中的作用是_______。
(2)加入Y时发生反应的化学方程式为________。
(3)理论上所得硫酸亚铁晶体的质量_________(填“>”“<”或“=”)原废液中硫酸亚铁的质量。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列说法正确的是( )
A.质量和质量分数均相等的氢氧化钠溶液与稀硫酸充分反应,所得溶液呈酸性
B.等质量的二氧化硫和三氧化硫,二氧化硫和三氧化硫中硫元素的质量比为4:5
C.硝酸镁样品(含有一种杂质)14.8g,溶于水,与足量的NaOH溶液充分反应生成沉淀5.5g,则样品中可能含有的杂质是MgSO4
D.向一定量的氧化铁与氧化铜的混合物中加入100g质量分数为9.8%稀硫酸,恰好完全反应,则原混合物中氧元素的质量是1.6g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将100g含有少量碳酸钾的氯化钾样品加入50g盐酸中完全反应且溶解,气体全部逸出,得到145.6g溶液.则:
(1)产生的气体质量为________g.
(2)样品中氯化钾的质量分数_______;
(3)所得溶液中溶质质量分数_______(计算结果精确到0.1%).
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有一包粉末,已知由CaCO3、CuSO4、MgCl2、Na2SO4、NaOH、NaNO3中的几种组成,为确定其组成,现进行以下实验(各步骤均充分反应):
①取一定质量的粉末,加水搅拌后过滤,得到沉淀和无色溶液A;
②向①步得到的沉淀中加入足量稀硝酸,得到无色气体和蓝色溶液;
③将①步得到的无色溶液A进行如图所示的实验: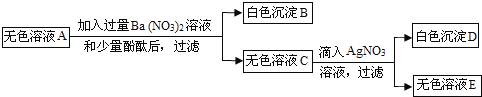
回答下列问题:
(1)D 的化学式是_______;
(2)A中一定存在的溶质的化学式是_______;
(3)生成白色沉淀B 的化学方程式是_______;
(4)这包粉末中可能含有的物质的化学式是_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室常利用下图部分装置制取氧气。
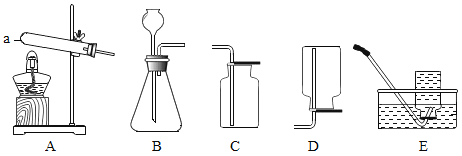
(1)仪器a的名称是_____。
(2)实验室用A装置制备氧气时,反应的化学方程式为_____。
(3)为了获得较干燥的氧气,应选用的收集装置是____(填字母序号)。验满的方法是___。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“侯氏制碱法”是我国著名科学家侯德榜发明的一种连续生产纯碱与氯化铵的联合制碱工艺。
①生产原理:反应Ⅰ:NaCl(饱和溶液)+NH3+CO2+H2O=NaHCO3(固体)↓+NH4Cl
②主要生产流程如图所示:
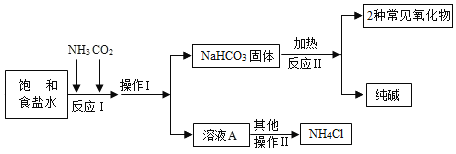
下列叙述错误的是( )
A.生产流程中,操作I的名称是过滤
B.反应I中,涉及的物质氮元素的化合价发生了改变
C.反应I中,碳酸氢钠晶体析出后,剩余的液体中不会含有碳酸氢钠
D.反应Ⅱ的化学方程式是2NaHCO3![]() Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学是一门以实验为基础的科学,请结合如图回答问题:
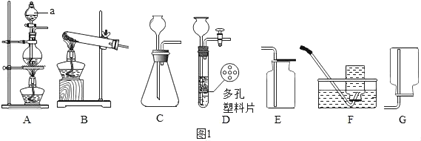
(1)仪器a的名称是___。
(2)在确定实验室制取氧气的化学反应时,不需要考虑的因素是___(填字母)。
a.原料中是否含有氧元素b.原料的产地c.实验装置是否容易装配
d.实验条件是否容易控制e.实验操作是否安全可靠
(3)实验室制取二氧化碳的化学方程式为__。可选用如图中C、D发生装置,D与C相比优点是__,收集二氧化碳可选择__(填装置序号)。
(4)实验室制取氯气。
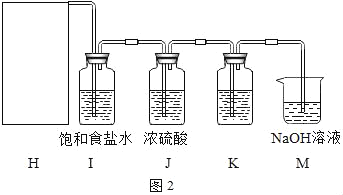
资料:通常情况下,氯气是黄绿色有刺激性气味的有毒气体,可溶于水,密度比空气大;能与金属、非金属、水、氢氧化钠溶液等反应。实验室常用二氧化锰固体和浓盐酸加热制取氯气。
①如图中H处为制备氯气的装置,应该选择如图中的___(填装置序号)。
②M装置的作用是___。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铅蓄电池在生产、生活中使用广泛,其构造如图所示
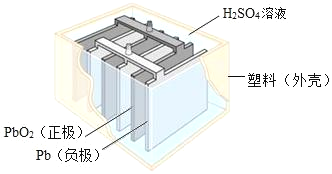
(1)铅蓄电池充电时是将电能转化为____(填序号)
a 机械能 b 热能 c 化学能
(2)用98%的浓硫酸配制5%的稀硫酸100克,为准确量取浓硫 酸的体积,还需查阅的数据是__;稀释浓硫酸的操作是____;
(3)铅蓄电池的工作原理可以表示为:2PbSO4+2H2O![]() Pb+PbO2+2H2SO4据此可知,铅蓄电池在放电时,溶液 pH 将不断_____(填“增大”“减小”或“不变”)。
Pb+PbO2+2H2SO4据此可知,铅蓄电池在放电时,溶液 pH 将不断_____(填“增大”“减小”或“不变”)。
(4)硫酸在工业上有着重要的用途。以黄铁矿(主要成分为FeS2)为原料生产硫酸的原理及工艺流程可简示如下:
(原理)FeS2![]() SO2
SO2![]() SO3
SO3![]() H2SO4
H2SO4
(工艺流程)
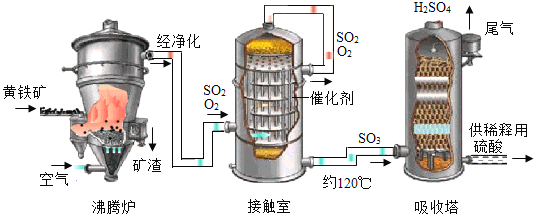
①黄铁矿是_____(填“纯净物”或“混合物”),与氧气反应可生成二氧化硫和氧化铁。
②工业上常用石灰乳来吸收尾气中的二氧化硫,反应的化学方程式是____。
③下列有关说法中,不正确的是_____(填序号)。
A 将黄铁矿粉碎的目的是增大与反应物(氧气)之间的接触面积
B 在原料质量一定的条件下,使用催化剂能多生成SO3
C 生产过程中向空气里排放含较多SO2、SO3的尾气,可能会引发酸雨
D 排出的矿渣可用做工业炼铁的原料
(5)钢铁工业是国家工业的基础。工业上常用CO还原氧化铁来制取铁。现有100t含氧化铁80%的赤铁矿石,理论上可以冶炼出铁的质量是______?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com