
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 将带火星的木条伸入装有氧化氢溶液的试管 | 木条不燃 | 常温下过氧化氢溶液分解很缓慢 |
| 实验二 | 在装有过氧化氢溶液的试管中加入少量Al2O3,然后将带火星的木条伸入试管中 | 木条复燃 | 因为Al2O3能加快过氧化氢的分解速率,所以Al2O3能作为过氧化氢分解的催化剂. |
分析 在化学反应里能改变其他物质的化学反应速率,而本身的质量和化学性质在反应前后都没有发生变化的物质叫做催化剂.要探究一种物质能否作为化学反应的催化剂,一般要注意从三个方面入手进行:一是探究加入该物质能否改变化学反应速率;二是探究反应前后该物质的质量是否改变;三是探究化学反应前后该物质的化学性质是否改变.
解答 解:通过实验一探究Al2O3对过氧化氢分解速率的影响.实验1的步骤是:取过氧化氢溶液,然后将带火星的木条伸入装有过氧化氢溶液的试管中,带火星的木条不复燃,可见常温下过氧化氢分解速率很慢.
实验二在装有过氧化氢溶液的试管中加入少量Al2O3,带火星的木条复燃,可见,Al2O3能加快过氧化氢的分解速率.但不能说Al2O3就是过氧化氢的催化剂.
实验三:通过实验前后两次称量,可知实验三是探究Al2O3在反应前后质量是否改变.将实验二反应后的物质进行过滤可得到Al2O3,必须经过洗涤、烘干后才称量,减少实验数据的误差.
最后,还必须在增加一个实验:探究Al2O3的化学性质在反应后是否改变.只有Al2O3具备既能改变化学反应速率,其质量和化学性质在反应前后又保持不变,才能作为过氧化氢分解的催化剂.
故答案为:Al2O3能加快过氧化氢的分解速率
(2)Al2O3在反应前后质量是否改变;
(3)Al2O3的化学性质在反应前后是否改变.
点评 此题探究Al2O3是不是过氧化氢分解反应的催化剂.中考有关催化剂的考查主要集中在催化剂的作用和探究某物质是不是过氧化氢或氯酸钾分解反应的催化剂.催化剂的特点可以概括为“一变二不变”,一变是能够改变化学反应速率,二不变是指质量和化学性质在化学反应前后保持不变.要探究一种物质能否作为化学反应的催化剂,必须同时具备上述特点.


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案科目:初中化学 来源: 题型:选择题
| A. | 用赤铁矿高炉炼铁Fe2O3+3CO $\frac{\underline{\;高温\;}}{\;}$ 2Fe+3CO2 置换反应 | |
| B. | 拉瓦锡用定量的方法研究空气的成分4P+50$\frac{\underline{\;燃烧\;}}{\;}$ 2P2O5 化合反应 | |
| C. | 加热混有二氧化锰的氯酸钾制取氧气2KC103$\frac{\underline{MnO_2}}{△}$2KC1+302↑ 分解反应 | |
| D. | 用稀硫酸洗去附着在试管壁上的铜:Cu+H2SO4═CuSO4+H2↑ 置换反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
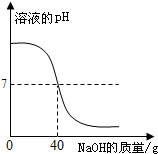 中和反应在工农业生产中应用广泛.现将溶质质量分数为10%的氢氧化钠溶液滴加到60g稀硫酸中,测得溶液pH与加入的氢氧化钠溶液的质量关系如图所示.
中和反应在工农业生产中应用广泛.现将溶质质量分数为10%的氢氧化钠溶液滴加到60g稀硫酸中,测得溶液pH与加入的氢氧化钠溶液的质量关系如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 只有① | B. | 只有①②③ | C. | 只有②③④ | D. | ①②③④ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
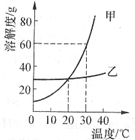
| A. | 乙的溶解度比甲的溶解度小 | |
| B. | 20℃时甲、乙两溶液的质量分数相等 | |
| C. | 30℃时甲的饱和溶液的质量分数为60% | |
| D. | 若甲中混有少量乙,可采用冷却热饱和溶液的方法提纯甲 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
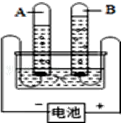 如图所示是一种电解水的装置,请回答下列问题
如图所示是一种电解水的装置,请回答下列问题查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com