
【题目】某课外活动小组对失去标签的稀硫酸浓度进行测定:取稀硫酸50 g于烧杯中,逐滴滴加3.42%的氢氧化钡溶液,烧杯内溶质质量与滴加氢氧化钡溶液质量关系如图所示。( 结果保留两位小数)
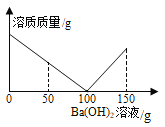
(1)参加反应的Ba(OH)2质量共有_______g。当滴加Ba(OH)2溶液50g时,烧杯内溶液的pH__________7(填“>”“<”或“=”)。
(2)求该硫酸溶液的溶质质量分数 ( 写出答题过程,结果保留0.01%)。
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案科目:初中化学 来源: 题型:
【题目】为探究金属的化学性质,某化学探究小组进行如下实验活动。
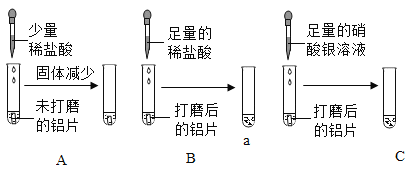
[提出问题]铝具有什么化学性质?
[实验探究1]小松和小雷分别用一片未打磨的铝片和打磨过的铝片进行实验A、B。实验B中观察到的现象是_____,得出铝与稀盐酸反应产生气体的结论。
[反思与评价]据现象小松认为铝与稀盐酸反应不产生气体,请评价小松的实验和结论______。经过思考,小松向试管中继续滴加足量的盐酸,一会儿后观察到和B中相同的现象,小松据此推测出铝具有的另一条化学性质是_____(用化学方程式表示)。
[实验探究2]小雷进行了如图C实验没有观察到明显现象,是否发生了化学反应呢?过滤后称量滤出的固体,发现固体质量增加,借助小松的实验得出的结论,小雷向滤出固体中加入足量稀盐酸,无明显现象,可知滤渣中不含_____,而是____。 据此可知C中发生反应的化学方程式为____________。于是又得出一条铝具有的化学性质。
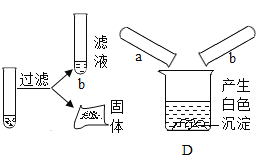
[发现新问题]同学们又对a、b中溶质的成分产生兴趣。
[实验探究]根据对溶质成分的猜想,结合实验探究I的探究成果,小松取少量a、b样品通过混合的方法鉴别a、b中溶质的成分。
[分析与结论]小雷对小松的实验提出质疑,他认为通过实验D,能推测b中溶质的成分,却无法确定a中溶质的成分。根据现象和实验事实,能推测出b中溶质含有的离子是____ ( 填离子符号)。无法确定a中溶质的成分是因为____。
[实验与结论]经过思考,为确定a中溶质,小组同学取少量a样品,加入___(填化合物)观察到明显现象,最终确定了a中溶质的成分。
[归纳与总结]通过上述实验可以总结出;在探究物质的性质时,我们要排除物质具有的性质和生成的物质对探究其他性质可能产生的干扰。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学设计了如图所示装置,用于实验室制取CO2并对它的部分性质进行探究,按要求回答:
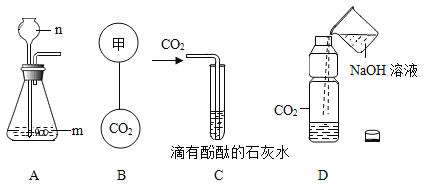
(1)指出仪器名称:m_____,n_____。
(2)图A中发生的反应化学方程式是_____。
(3)若要图B中两个气球悬浮在空气中,则气体甲可能是_____(填序号)。
a.空气 b.氧气 c.氢气
(4)当图C中出现_____现象,表明石灰水的溶质刚好完全沉淀。
(5)向图D塑料软瓶中倒入一定量的NaOH溶液,迅速拧紧瓶盖,振荡,可观察到_____,反应的化学方程式_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】尿素是一种常用的化肥,图1是工业生产尿素[CO(NH2)]的微观示意图,图2是尿素中各元素质量分数的示意图,下列说法正确的是( )
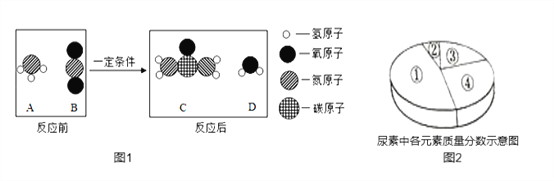
A. 图1中的四种物质有3种属于氧化物
B. 生产尿素的反应属于复分解反应
C. 图2中表示氮元素质量分数的是④
D. 生产尿素的反应中,A与B的粒子个数比为2:1
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】无水氯化镁是制备某种催化剂的中间体。某研究性学习小组设计实验方案进行制取无水氯化镁等实验。请填写下列空白。
(1)[实验一]
利用下图实验装置(夹持和加热装置省略) , 在HCl气流中小心加热MgCl2. 6H2O晶体制取无水氯化镁(无水氯化镁易吸水)。烧瓶中发生的反应为:![]() 。
。
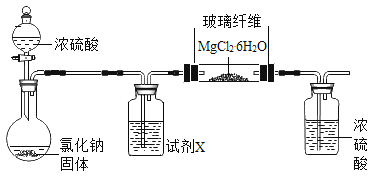
①试剂X是____。第二个洗气瓶中的浓硫酸的作用是_____。
②该实验装置存在一个缺陷是___。
(2)[实验二]
通过下列步骤,测定实验一所得产物中氯元素含量以确定产物是否含有结晶水:
称取m1 g样品置于烧杯中,充分溶解;加入足量硝酸银溶液,充分反应后,过滤;洗涤沉淀,干燥至恒重,称得沉淀质量为m2 g。
①若步骤③的操作中未洗涤沉淀,将导致测得的氯元素含量___ ( 填“偏高”或“偏低”)。
②若测得m1=10.40,m2=28.70,则所得产品MgCl2.nH2O中n的值为___。
(3)[实验三]
一定条件下,氯化镁与四氯化钛的混合物可作烯烃聚合反应的催化剂。为了探究温度、氯化镁固体的含水量以及粉碎方式对该催化剂催化效果的影响,设计如下对比实验:
实验序号 | 氯化镁固体中氯元素含量/% | 温度/°C | 粉碎方式 | 催化效果/g.g-1 |
1 | 70.97 | 20 | 滚动球磨 |
|
2 | 74.45 | 20 | 滚动球磨 |
|
3 | 74.45 | 20 | 振动球磨 |
|
4 | ω | 100 | 振动球磨 |
注:催化效果用单位时间内每克催化剂得到产品的质量来表示
①表中ω=_____。
②从实验1、2可以得出的结论是_______。
③设计实验2、3的目的是___。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】材料有着广泛的应用,根据下列信息回答问题。
应用 | “鸟巢”钢结构 | “水立方”墙面 | 羽毛球拍 |
用到的材料 | 高强度钢 | 含氟塑料 | 铝合金 |
(1)上述材料中属于合金的是________(写一种即可),属于有机合成材料的是_______。
(2)羽毛球拍由铝合金制成,其优点是强度大、质轻且_______。用化学方程式表示铝表面形成氧化物的原理:_________。
(3)为防止金属锈蚀,常在表面涂一层漆 ,其防锈原理是_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用甲乙丙三套装置进行H、C、CO还原CuO的实验并检验产物(已知白色粉末无水硫酸铜遇水变蓝色)。分析上述三个实验,下列说法错误的是
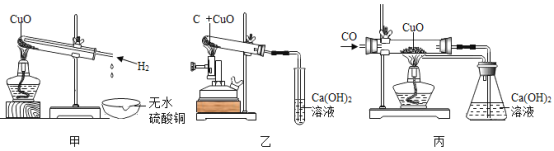
A.甲乙丙三个实验都能观察到黑色粉末变红色的现象,并能成功检验产物
B.甲乙丙三个反应中,反应前后Cu元素的化合价都降低,O元素的化合价都不变
C.甲乙丙三个实验能说明H、C、CO都具有还原性,且三个反应都是置换反应
D.若反应前称量丙中硬质玻璃管及氧化铜的总质量为60g,通入一氧化碳反应一段时间后,冷却称量硬质玻璃管及其中物质的总质量为58.4g,则参加反应的氧化铜的质量为8g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】SrCl2·6H2O具有很高的经济价值,以工业碳酸锶(SrCO3质量分数为98.5%,极少量Ba2+,微量Fe2+)为原料制备SrCl2·6H2O的工艺流程如下:
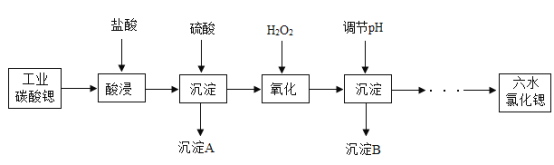
已知:
①SrCl2难溶于酒精,SrCl2·6H2O在61.5℃会失去结晶水,生成SrCl2·2H2O。
②降温结晶速率太快,会导致晶体细碎,夹带溶液,导致晶体不纯。
③SrCl2溶解度曲线及结晶装置图如下:
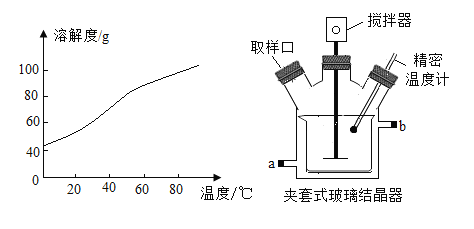
(1)酸浸时,搅拌的作用是____。发生反应的化学方程式主要为____,属于____反应(填基本反应类型)。能否用稀硫酸代替稀盐酸,__(填“能”或“否”)理由是___。
(2)沉淀A为____(填化学式),沉淀B为红褐色,是____(填化学式)。调节pH时,最好选用的试剂是____。
A NaOH
B Ca(OH)2
C Sr(OH)2
(3)流程中,“……”为一系列操作,分别为蒸发浓缩→____→过滤→洗涤→烘干。实验室完成过滤操作所需的玻璃仪器有烧杯、玻璃棒、____。夹套式玻璃结晶器的夹套内是冷却水,可由外接计算机程序精确控制进水的温度,进水口为____(填“a”或“b”)。
(4)洗涤SrCl2·6H2O晶体适宜选用的试剂是____。
A 0℃时蒸馏水
B 常温SrCl2饱和溶液
C 热水
D 无水酒精
(5)SrCl2·6H2O晶体烘干的适宜温度为___。
A 50 ~ 60℃
B 70 ~ 80℃
C 80 ~ 100℃
D 100℃以上
(6)常用锶转化率衡量工艺水准,本工艺使用100吨工业碳酸锶,最终得到176.9吨SrCl2·6H2O,则本工艺中的锶转化率约为___。(精确到小数点后一位)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是a、b、c三种物质的溶解度曲线,下列说法中正确的是( )
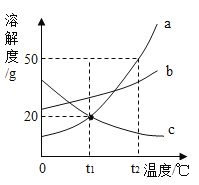
A.在t1℃时,a的饱和溶液的溶质质量分数等于c溶液的溶质质量分数
B.当b物质中混有少量a物质时,可以采用降温结晶的方法提纯b
C.a、b两种物质的饱和溶液,从t1℃升温至t2℃,所得溶液溶质质量分数a<b
D.等质量a、b、c三种物质的饱和溶液,从t2℃降温至0℃,所得溶液溶剂质量最少的是c
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com