

分析 根据氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质,除去碳酸根离子和硫酸根离子,需要加入过量的氯化钡溶液,然后过滤后得到氯化钡、氯化钾的混合溶液A,然后加入过量的碳酸钾溶液,除去氯化钡,过滤得到氯化钾和碳酸钾的混合溶液,再加入过量的盐酸,除去碳酸钾,最后经过加热浓缩,蒸发结晶,过滤得到氯化钾晶体进行分析.
解答 解:氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质,除去碳酸根离子和硫酸根离子,需要加入过量的氯化钡溶液,然后过滤后得到氯化钡、氯化钾的混合溶液A,然后加入过量的碳酸钾溶液,除去氯化钡,过滤得到氯化钾和碳酸钾的混合溶液,再加入过量的盐酸,除去碳酸钾,最后经过加热浓缩,蒸发结晶,过滤得到氯化钾晶体,所以
(1)①中发生的所有反应是硫酸钾和氯化钡反应生成硫酸钡沉淀和氯化钾,碳酸钾和氯化钡反应生成碳酸钡沉淀和氯化钾,化学方程式为:K2SO4+BaCl2=BaSO4↓+2KCl,K2CO3+BaCl2=BaCO3↓+2KCl;
(2))②中加入试剂2的目的是除过量BaCl2;
(3)在加入试剂3之前必须进行过滤的原因是碳酸钡与盐酸会反应;
(4)E之后需要进行蒸发,蒸发的作用之一是得到KCl晶体,另一作用是:除去多余的盐酸.
故答案为:(1)K2SO4+BaCl2=BaSO4↓+2KCl,K2CO3+BaCl2=BaCO3↓+2KCl;
(2)除过量BaCl2;
(3)碳酸钡与盐酸会反应;
(4)除去多余的盐酸.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.


科目:初中化学 来源: 题型:解答题
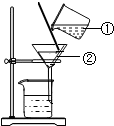 如图为精制粗盐的某个步骤的示意图,回答:
如图为精制粗盐的某个步骤的示意图,回答:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 二氧化碳是一种温室气体 | |
| B. | 减少二氧化碳排放最好是禁止使用石油等燃料 | |
| C. | 固体二氧化碳称为冰 | |
| D. | 大量排放二氧化碳是引起大气污染的主要因素 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
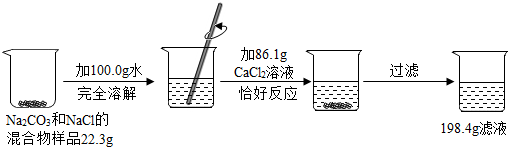
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. |  大办酒席 | B. |  鲜花扫墓 | C. |  工业排污 | D. |  燃放爆竹 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
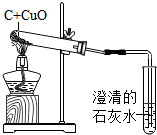 某中学化学兴趣小组按照课本实验方法,做木炭与氧化铜反应实验时,发现很难观察到紫红色铜的生成,却往往有暗红色固体出现.他们决定对这个实验进行探究和改进.
某中学化学兴趣小组按照课本实验方法,做木炭与氧化铜反应实验时,发现很难观察到紫红色铜的生成,却往往有暗红色固体出现.他们决定对这个实验进行探究和改进.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 不同元素间的本质区别是粒子的核外电子数不同 | |
| B. | 元素的化学性质主要取决于原子的核外电子数 | |
| C. | 空气、海水、地壳中含量最多的元素都是氧元素 | |
| D. | 硒(Se)属于人体的必需微量元素,应合理摄入 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com