
分析 (1)浓盐酸具有挥发性;
(2)根据将氢氧化钠溶液逐滴滴入盐酸和氯化铜的混合溶液中,氢氧化钠溶液先和盐酸反应生成氯化钠和水,当盐酸反应完后氢氧化钠溶液再和氯化铜反应生成氢氧化铜沉淀和氯化钠进行解答;
(3)①根据碳酸钠能和稀盐酸反应生成氯化钠、水和二氧化碳分析现象;
②氢氧化钠、碳酸钠的水溶液都显碱性,都能够使酚酞试液变红色,因此要想检验氢氧化钠部分变质,应先除去碳酸钠再证明溶液显碱性,才能说明部分变质;
③前后溶液质量差为沉淀的质量,根据沉淀的质量可求出氯化钙的质量,进而求质量分数.
解答 解:(1)浓盐酸具有挥发性,打开浓盐酸的试剂瓶,观察到瓶口有白雾产生;故填:白雾;
(2)将氢氧化钠溶液逐滴滴入盐酸和氯化铜的混合溶液中,氢氧化钠溶液先和盐酸反应生成氯化钠和水,当盐酸反应完后氢氧化钠溶液再和氯化铜反应生成氢氧化铜沉淀和氯化钠.
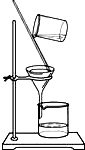
A点没有沉淀生成,说明氢氧化钠溶液只和盐酸反应生成氯化钠和水,而氯化铜还没有反应,所以此处溶液的溶质是氯化钠和氯化铜.故填:氯化钠和氯化铜;
C点处是氢氧化钠溶液过量,所以此时溶液呈碱性,溶液的pH大于7;
AB段是氢氧化钠溶液和氯化铜反应生成氢氧化铜沉淀和氯化钠,发生反应的化学方程式CuCl2+2NaOH═Cu(OH)2↓+2NaCl.故填:CuCl2+2NaOH═Cu(OH)2↓+2NaCl;
(3)①氢氧化钠和二氧化碳发生反应生成碳酸钠和水,取少量样品于试管中,加入足量稀盐酸,如果观察到有气泡产生,说明样品中含有碳酸钠,说明假设1不成立;
故填:有气泡冒出;
②为了排除碳酸钠对实验结果的影响,应该加入足量CaCl2溶液把碳酸钠除去,如果向溶液B中滴加酚酞试液时,酚酞试液变红色,说明样品中含有氢氧化钠;
③沉淀的质量为:50g+50g-95g=5g
设氯化钙的质量为x
CaCl2+Na2CO3═CaCO3↓+2NaCl
111 100
x 5g
$\frac{111}{100}=\frac{x}{5g}$
x=5.55g
所用CaCl2溶液的质量分数为:$\frac{5.55g}{50g}×100%$=11.1%
答:所用CaCl2溶液的质量分数为11.1%.
点评 此题考查对一瓶没有密闭保存的氢氧化钠固体进行实验探究过程,在证明氢氧化钠部分变质时,先除去氢氧化钠中的碳酸钠,然后再证明剩余溶液显碱性,才能说明氢氧化钠部分变质.


科目:初中化学 来源: 题型:选择题
| A. | FeCl3、CuSO4、NaCl | B. | BaCI2、Na2SO4、NaOH | ||
| C. | CaCl2、Na2CO3、AgNO3 | D. | K2SO4、NaNO3、HCl |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 完全反应得到无色溶液,样品中一定没有铁 | |
| B. | 反应后过滤,一定会有滤渣 | |
| C. | 所加稀盐酸中溶质的质量分数为7.3% | |
| D. | 反应后过滤,得到溶液中溶质只有氯化镁 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 根据图回答相关问题:
根据图回答相关问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | FeO>Fe3O4>Fe2O3 | B. | Fe3O4>Fe2O3>FeO | C. | Fe2O3>Fe3O4>FeO | D. | FeO>Fe2O3>Fe3O4 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 原子不能再分 | |
| B. | 原子核都是由质子和中子构成的 | |
| C. | 相对原子质量只是一个比,没有单位 | |
| D. | 原子可以构成分子,也可以直接构成物质 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 淘米水用来浇花 | B. | 开发利用地下水 | ||
| C. | 使用节水龙头 | D. | 用喷灌、滴灌方法给农作物浇水 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | H2 | B. | Cl2 | C. | Na2CO3 | D. | NaOH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com