
【题目】同学们在帮助老师整理实验室时,发现半瓶久置的氢氧化钙粉末[Ca(OH)2],大家决定用实验的方法探究这瓶粉末的组成。(资料:室温时,Ca(OH)2的溶解度是0.165g)
实验一:样品溶于水
取一药匙的样品,加入20mL水中充分溶解后,有沉淀物。
(1)有同学认为,该沉淀物可能是氢氧化钙,其推断的理由应该是_____。
(2)要证明样品已经变质生成碳酸钙,可往分离出的沉淀物中滴加稀盐酸,反应的化学方程式为_____。
实验二:测定样品中碳酸钙的质量分数
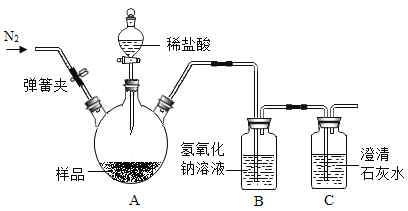
如图:打开弹簧夹,先通入N2一会儿,以排尽装置中含有的CO2.关闭弹簧夹,在A的样品中加入足量的稀盐酸。通过测定反应产生的二氧化碳气体的质量,可计算碳酸钙的质量分数(装置气密性已检验,夹持装置已省略)。
(3)装置B中发生反应的化学方程式是_____。
(4)实验结束后,还要再通一会儿N2,目的是_____。
(5)若C中无变化,经测定B瓶增重m g,要计算样品中碳酸钙的质量分数,还要预先测定_____的质量。
(6)若C中石灰水变浑浊,则测得的样品中CaCO3 的质量分数值将_____(填“偏高”、“偏低”或“不变”)。
【答案】室温时![]() 的溶解度是0.165g,溶解度很小
的溶解度是0.165g,溶解度很小 ![]()
![]() 使反应产生的二氧化碳全部被氢氧化钠溶液吸收 样品A 偏低
使反应产生的二氧化碳全部被氢氧化钠溶液吸收 样品A 偏低
【解析】
(1)由题干数据可知,室温时![]() 的溶解度是0.165g,溶解度很小,一药匙的氢氧化钙不能全部溶解在20mL水中,因此该沉淀物可能是氢氧化钙。
的溶解度是0.165g,溶解度很小,一药匙的氢氧化钙不能全部溶解在20mL水中,因此该沉淀物可能是氢氧化钙。
(2)碳酸钙和稀盐酸反应生成氯化钙、二氧化碳和水,反应的化学方程式为![]() 。
。
(3)装置B用来吸收二氧化碳,装置B中二氧化碳和氢氧化钠发生反应生成碳酸钠和水,反应的化学方程式为![]() 。
。
(4)若装置中残留有二氧化碳会影响到最终的结果,实验结束后,还要再通一会儿N2,目的是使反应产生的二氧化碳全部被氢氧化钠溶液吸收。
(5)B瓶增重的质量为碳酸钙与稀盐酸反应生成的二氧化碳的质量,根据方程式可以计算出碳酸钙的质量,样品中碳酸钙的质量分数=![]() ,要计算样品中碳酸钙的质量分数,还要预先测定样品A的质量。
,要计算样品中碳酸钙的质量分数,还要预先测定样品A的质量。
(6)若C中石灰水变浑浊,说明有二氧化碳没有被氢氧化钠溶液吸收,会导致计算出的碳酸钙质量偏小,由碳酸钙的质量分数=![]() ,可知会导致测得的样品中CaCO3 的质量分数偏低。
,可知会导致测得的样品中CaCO3 的质量分数偏低。


科目:初中化学 来源: 题型:
【题目】某化学兴趣小组的同学在做酸碱中和反应时,将稀盐酸滴加到盛有氢氧化钠溶液的试管中,没有观察到明显现象(氢氧化钠未变质),小组同学对氢氧化钠溶液与稀盐酸是否发生了化学反应产生了兴趣,他们做了如下实验
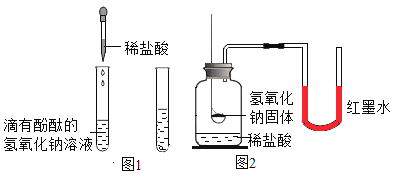
(实验一)酚酞溶液在酸和碱溶液中显示不同的颜色,可借助指示剂的颜色变化判断酸碱是否发生了反应,如图 1所示
(1)可说明试管中两种物质发生反应的现象是_____,该反应的化学方程式为_____
(实验二)化学反应通常伴随能量的变化,可借助反应前后的温度变化来判断酸碱是否发生了反应,如图2所示
(2)将盛有氢氧化钠固体的燃烧匙伸入稀盐酸中,观察到U形管中右侧红墨水液面上升,该现象_____(填“能”或“不能”)证明氢氧化钠与稀盐酸发生了化学反应,理由是_____
(3)小组同学利用温度传感器测定了盐酸与氢氧化钠反应的时间 -温度曲线如图3所示
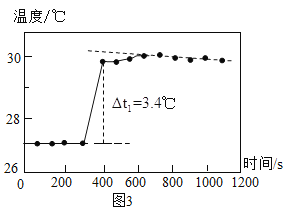
①由曲线变化情况分析可知,稀盐酸与氢氧化钠溶液发生反应并_____(填 “放出”或“吸收”)热量
② 400秒后,曲线开始呈下降趋势的原因是_____
(实验三)有同学提出还可利用 pH的变化判断酸碱是否发生了反应,图 4所示是小组同学利用 pH传感器探究氢氧化钠溶液与稀盐酸反应的 pH变化曲线

(4)该反应是将_____(填序号),M 点溶液中溶质为_____(填化学式)
a.稀盐酸加入氢氧化钠溶液 b.氢氧化钠溶液加入稀盐酸
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是一组用于研究可燃物燃烧条件的对比实验,对有关实验现象和结论的判断错误的是( )

A.实验1中红磷未燃烧,说明红磷的着火点高于白磷
B.实验2中白磷燃烧,说明实验2中的热水温度高于实验1
C.实验2中如果停止通入氧气,燃着的白磷会熄灭
D.可燃物燃烧需要氧气(或空气),并达到着火点
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】天然气的主要成分是甲烷(CH4),实验室将固体醋酸钠(CH3COONa)与碱石灰(NaOH和CaO的混合物)共热来制取甲烷气体,反应的原理是:CH3COONa+NaOH![]() Na2CO3+CH4↑结合如图回答下列问题:
Na2CO3+CH4↑结合如图回答下列问题:
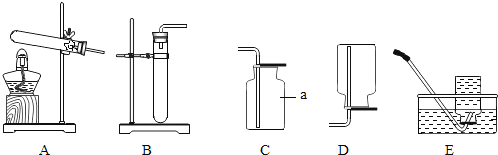
(1)仪器a的名称是_____;制取甲烷的发生装置是_____(填字母序号),理由是____.
(2)甲烷是无色、无味的气体,可采用D或E的装置来收集甲烷,请补充完整甲烷的物理性质___.
(3)甲烷像氢气一样是易燃气体,点燃前应该进行的操作是___,写出甲烷燃烧的化学方程式____.
(4)要产生32g甲烷气体,至少需要醋酸钠粉末的质量是____g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】砷化镓是节能光源材料,镓元素在周期表的信息如图。下列有关镓的说法正确的是( )
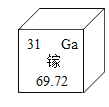
A.原子的核电荷数是31B.原子的中子数是31
C.属于非金属元素D.相对原子质量为69.72g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)自然界中吸收大气中CO2的最重要环节是_____.
(2)科学家研究得到:海洋是吸收大量CO2的地方.如果CO2排放量继续增加,海洋将被“酸化”.请写出海洋酸化原因的化学方程式________.
(3)科学家目前正在研究将空气中过量的CO2和H2在催化剂和适量条件下转化成液态甲醇和水,反应的化学方程式:CO2+3H2 甲醇+H2O.则甲醇的化学式是______.
甲醇+H2O.则甲醇的化学式是______.
(4)已知20℃时,KCl的溶解度为34克,50℃时的溶解度为42.6克.通过以下实验操作得到溶液①至⑤:
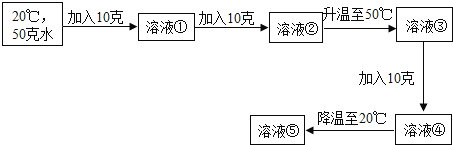
Ⅰ、上述实验所得溶液中,属于饱和溶液的是____;
Ⅱ、溶液④的质量为____克;
Ⅲ、溶液⑤中,溶质的质量分数为_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小聪同学家新换了水龙头,从说明书上了解到该水龙头是铜质镀铬.好奇的小聪想探究铬(Cr)与常见金属铁、铜的活动性强弱,请把以下探究过程补充完全.
(作出猜想):1.Cr>Fe>Cu 2. Fe>Cu>Cr 3.________.
(查阅资料)(1)铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜.
(2)铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液.
(设计与实验)小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种浓度的稀硫酸.
实验 | 试管1 | 试管2 | 试管3 |
实验操作 |
|
|
|
实验现象 | 铁片表面产生气泡较慢,溶液变为浅绿色 | 铬片表面产生气泡较快,溶液变为蓝色 | 无明显现象 |
(结论与解释)(1)小聪得到的结论是猜想________ 正确.
(2)实验前用砂纸打磨金属片的目的是________.
(知识运用)如果将光洁的铬片投入到CuSO4溶液中,反应的现象为______.反应的化学方程式为_______.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】维生素C的化学式为C6H8O6主要存在于蔬菜、水果中,它能促进人体生长发育,增强人体对疾病的抵抗力。下列有关维生素C的说法中正确的是
A.维生素C中C、H、O三种元素的质量比为9:1:12
B.1个维生素C分子由6个碳原子、8个氢原子、6个氧原子构成
C.维生素C的相对分子质量为174
D.维生素C中氢元素的质量分数为4.5%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】宏观辨识和微观剖析是化学核心素养之一。下列说法不正确的是
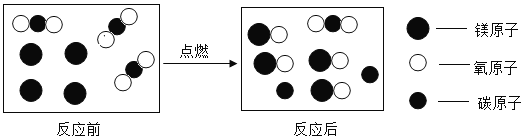
A.该反应属于置换反应
B.该反应中“![]() ”和“
”和“![]() ”的微粒个数比是2:1
”的微粒个数比是2:1
C.该反应前后元素的种类及化合价均未发生改变
D.该反应涉及的物质中,有两种氧化物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com