
| 物质 | 杂质 | 除杂质应选用的试剂和操作方法 | |
| A | CO2 | CO | 通入O2,点燃 |
| B | NaOH固体 | Na2CO3固体 | 加入过量盐酸,蒸发 |
| C | Cu(NO3)2溶液 | AgNO3溶液 | 加入过量的铜粉,过滤 |
| D | CuO固体 | Cu固体 | 加入适量的稀硫酸溶液,过滤 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、除去二氧化碳中的一氧化碳不能够通氧气点燃,这是因为除去气体中的气体杂质不能使用气体,否则会引入新的气体杂质,故选项所采取的方法错误.
B、NaOH固体和Na2CO3固体均能与稀盐酸反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
C、过量的铜粉能与AgNO3溶液反应生成硝酸铜溶液和银,再过滤,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
D、CuO固体与适量的稀硫酸溶液反应生成硫酸铜和水,铜不与稀硫酸反应,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
故选:C.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.


 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案科目:初中化学 来源: 题型:多选题
| A. | 在空气中点燃硫粉,产生明亮的蓝紫色火焰,放出热量 | |
| B. | 镁在空气中燃烧,发出强光,放出热量,产生大量的白雾 | |
| C. | 向硫酸铜溶液中加入铁钉:铁钉表面有一层红色物质,溶液变成浅绿色 | |
| D. | 硝酸铵与熟石灰混合研磨:白色固体中产生刺激性气味气体 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 图中的A-G表示几种初中化学常见的纯净物,其中A用于改良酸性土壤,B、C是氧化物,E俗称小苏打,人的胃液中含有F、E、G分别与足量F反应的生成物相同,图中“-”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系,部分反应物或生成物已略去.
图中的A-G表示几种初中化学常见的纯净物,其中A用于改良酸性土壤,B、C是氧化物,E俗称小苏打,人的胃液中含有F、E、G分别与足量F反应的生成物相同,图中“-”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系,部分反应物或生成物已略去.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
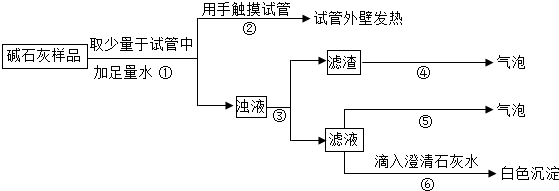
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
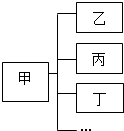 如图,小军对所学知识进行了归纳,其中甲与乙、丙、丁…不是都能反应的一组是( )
如图,小军对所学知识进行了归纳,其中甲与乙、丙、丁…不是都能反应的一组是( )| 甲 | 乙、丙、丁… | |
| A | O2 | Cu、H2、CO |
| B | CuO | C、CO、H2SO4 |
| C | CO2 | Ba(OH)2、H2O、C |
| D | CuSO4 | Fe、HCl、Ca(OH)2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
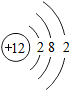
| A. | 核电荷数为12 | |
| B. | 核外有3个电子层 | |
| C. | 带12个单位正电荷 | |
| D. | 在化学反应中,易失去最外层上的2个电子 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
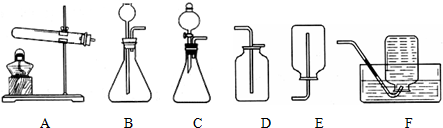
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com