
| 单质 | 氧化物 | 氢化物 | 酸 | 碱 | 盐 |
分析 写出含有氮元素,且物质类别分别是单质、氧化物、酸、碱、盐的物质的化学式,这就需要一是了解常见氮元素的化合物,且明确物质的属性,而是根据化合价写出对应化学式.
解答 解:单质中元素的化合价为零;单质:只有氮气,由于是非金属气态单质,所以化学式有下标,下标为2,故化学式为:N2.
氧化物:氮元素的化合价有+1、+2、+3、+4、+5价,而氧为-2价,所以对应化合物有N2O、NO、N2O3、
NO2、N2O5等.
氢化物:只有氨气,氢元素显+1价,氮元素的化合价是+3价,可得NH3
酸:只有硝酸,氢元素显+1价,硝酸根显-1价,可得HNO3.其中氮元素显+5价;
碱:只是氨水,两种书写形式NH4OH或者NH3•H2O.其中氮元素显-3价
盐:硝酸盐和铵盐都可以,如NH4NO3等.其中氮元素分别显-3价和+5价.
故答案为:$\stackrel{0}{N}$2;$\stackrel{+1}{N}$2O、$\stackrel{+2}{N}$O、$\stackrel{+3}{N}$2O3、$\stackrel{+4}{N}$O2、$\stackrel{+5}{N}$2O5;$\stackrel{-3}{N}$H3;H$\stackrel{+5}{N}$O3;$\stackrel{-3}{N}$H3•H2O;$\stackrel{-3}{N}$H4$\stackrel{+5}{N}$O3.
点评 这样题目的答案可能是不唯一的,在平时练习中要尽量多想,多练,以便在解答物质推断题目时灵活运用.


 习题精选系列答案
习题精选系列答案科目:初中化学 来源: 题型:选择题
| 气体 | H2 | CO2 | SO2 |
| 密度g/L | 0.0899 | 1.977 | 2.716 |
| 溶解度/g | 0.0001603 | 0.1688 | 11.28 |
| A. | 排水集气法 | B. | 向下排空气法 | ||
| C. | 向上排空气法 | D. | 向上排空气法或排水集气法 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
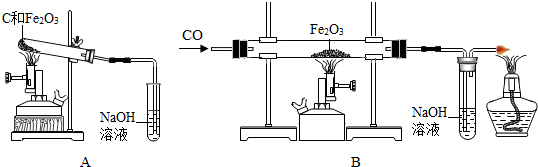
查看答案和解析>>
科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | Na2O+H2O═2NaOH | B. | Na2SO4+4C═Na2S+4CO↑ | ||
| C. | Fe2O3+3CO═2Fe+3CO2 | D. | 2Al(OH)3═Al2O3+3H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com