
【题目】如图所示进行有关碳及其氧化物的性质实验(图中固定玻璃管的仪器已略去),下列说法正确的是
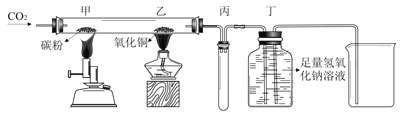
A. 将丁处氢氧化钠溶液改为澄清石灰水,可检验乙处反应生成的二氧化碳
B. 乙处发生的反应属于置换反应
C. 丙装置的作用是收集二氧化碳
D. 甲处发生的反应中,二氧化碳作氧化剂
科目:初中化学 来源: 题型:
【题目】下列图象分别与选项中的实验现象及结果相对应,其中正确的是( )
A. 电解水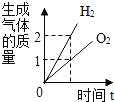
B. 将等质量的镁和铁分别投入到盛有足量同种稀硫酸的两个容器中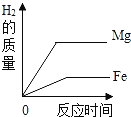
C. 等体积、等溶质质量分数的过氧化氢溶液制取氧气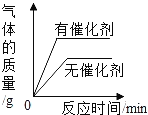
D. 服用胃舒平[主要成分是【Al(OH)3】治疗胃酸过多,胃液pH的变化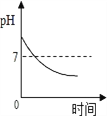
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“宏观——微观——符号”三重表征是化学独特的表示物质及其变化的方法。请结合下图所示的氢氧化钠溶液和稀硫酸反应的微观示意图,回答下列问题。

(1)写出氢氧化钠溶液和稀硫酸反应的化学方程式___________________________。
(2)写出图中C方框内乙粒子的符号:______________。
(3)从微观的角度分析,上述反应的实质是_____(填粒子符号,下同)和_____结合成H2O。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列有关化学史的说法不正确的是
A.道尔顿和阿伏加德罗提出了原子论和分子学说
B.门捷列夫发现了元素周期律并编制出了元素周期表
C.我国古代的炼丹术和炼金术对化学发展没有任何贡献
D.法国化学家拉瓦锡用定量的方法研究空气的成分
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请结合下列图回答问题:

(1)写出有标号仪器的名称:①_____,② _____。
(2)用氯酸钾和二氧化锰制取O2,选用发生装置是_____(填字母),该反应化学方程式是_______;若要收集相对纯度较高的O2可用______(填字母)装置收集。
(3)实验室制取CO2的化学方程式是_______,若用F装置代替B装置进行实验,其优点为_______。
①要获得纯净、干燥的CO2,除杂装置(如下图)的导管按气流方向连接顺序是______(选填字母)。
A.a→b→d→c B.d→c→a→b C.b→a→c→d D.c→d→b→a

②用化学方程式表示饱和碳酸氢钠溶液的作用______。
(4)硫化氢气体有毒,溶于水形成酸,用下图收集H2S。说明其密度比空气______(填“大”或“小”)。

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A~G均为初中常见的化学物质(“→”表示物质间的转化关系,“—”表示两端的物质能发生化学反应),其中A、F是初中阶段常见的两种氧化物;B、D是同种类别的物质; G是一种常见的建筑材料,E是人体胃液中的一种酸,它们之间有如下图的相互转化关系(图中部分生成物已略去)。请回答下列问题:

(1)B物质的化学式为________,
(2)C的俗称是________。
(3)写出化学反应①的化学方程式:①_________;
(4)反应②属于基本反应类型是_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】侯德榜是我国著名的化学家,为纯碱和氮肥工业技术的发展做出了杰出的贡献,他发明的侯氏制碱法大大提高了原料的利用率,其工艺流程大致如下图所示:

(1)上述流程中,用到的原料有空气、焦炭、水、二氧化碳、___________等;
(2)上述流程中,可循环利用的物质是_____________;
(3)上述流程中,“一种氮肥”的化学式是____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为测定某大理石样品中碳酸钙(杂质不溶于水也不参与反应)的质量分数,某小组的同学进行了如下实验(水和氯化氢的挥发忽略不计):取12.5g样品研碎放入烧杯中,每次加入20.8g稀盐酸后并用电子天平称量,记录实验数据如下。
加入稀盐酸次数 | 1 | 2 | 3 | 4 | 5 |
烧杯及所称物质总质量/g | 72.2 | 91.9 | 111.6 | 131.3 | 152.1 |
请计算:
⑴大理石样品中碳酸钙的质量分数;
⑵恰好完全反应时烧杯内溶液的溶质质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在工业上,碳酸钠广泛用于玻璃、造纸、纺织和洗涤剂的生产等。
【资料卡片】
(1)碳酸钠俗称纯碱、____。以纯碱和熟石灰为原料可以制烧碱,化学方程式为________。
(2)1921年,_______(填字母)发明了将制碱与制氨结合起来的联合制碱法,大大提高了原料的利用率。
A.拉瓦锡 B.道尔顿 C.侯德榜 D.张青莲
【定性实验】食盐是联合制碱法的主要原料之一,因此制得的纯碱中含有少量氯化钠。为了检验纯碱样品中存在氯离子,需要用到的药品是__________(填字母)。
A.氯化钡溶液 B.硝酸银溶液 C.稀硝酸 D.稀盐酸
【定量实验】将12.0g纯碱样品溶于水,加入足量氯化钡溶液,充分反应后,过滤、洗涤、低温干燥,得到19.7g沉淀。计算纯碱样品中碳酸钠的质量分数。__________(写出计算过程,结果保留一位小数)
【实验设计与评价】甲同学设计了如图实验装置,通过测量一定质量的纯碱样品与足量稀硫酸反应后产生二氧化碳的体积,进一步计算纯碱样品中碳酸钠的质量分数。

(1)检查装置的气密性时,起始状态量气管和水准管中液面相平,提高量气管,__________,证明该装置的气密性良好。
(2)乙同学认为该装置测得的二氧化碳的体积会偏小(不考虑操作上的失误),他的理由是______________________。
(3)丙同学认为该装置测得的二氧化碳的体积会偏大(不考虑操作上的失误),他的理由是______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com