
【题目】合金是由两种或两种以上的金属(或金属与非金属)熔合而成的具有金属特征的物质。一般来说,合金的熔点低于任何一种组分金属的熔点。 下表是一些金属的熔点数据。
金属 | 铜 | 锌 | 锡 | 铅 | 铋 | 镉 |
熔点/℃ | 1 083 | 419.6 | 231.9 | 327.5 | 271.3 | 320.9 |
(1)铅锡合金中某种金属的质量分数与合金的熔点有如图所示的关系,其中横坐标表示的是________的质量分数;当合金熔点最低时,合金中铅与锡的质量比为________。
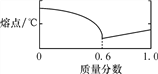
(2)保险丝由铋、铅、锡、镉等金属组成,其熔点约为________。
A.20~40 ℃ B.60~80 ℃ C.230~250 ℃ D.300~320 ℃
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案科目:初中化学 来源: 题型:
【题目】小明选择“铝丝和盐酸反应的快慢与什么因素有关”的课题开展探究。下表是他分别用相同质量的铝丝和足量稀盐酸反应的三组实验数据:
实验编号 | 盐酸的浓度/% | 反应温度/℃ | 铝丝消失 的时间/s |
① | 3 | 20 | 500 |
② | 6 | 20 | 300 |
③ | 6 | 30 | 80 |
(1)写出铝和盐酸反应的化学方程式:________________________________。
(2)实验②和③表明:该反应的快慢与__________有关。
(3)能表明盐酸浓度对反应快慢有影响的实验编号是________和________。
(4)如果把实验①中盐酸的浓度改为4%,请你推出铝丝消失的时间(用t表示)的取值范围:________________。
(5)该实验除了用铝丝消失的时间来衡量反应的快慢外,你还能提出新的方法来衡量该反应的快慢吗?
方法:_____________________________________________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小金制作了一个如图甲所示的简易酸碱灭火器,并进行了如图乙所示的灭火操作,结束后对瓶中残留液进行了如下实验:①取少量残留液于试管中,滴加2滴紫色石蕊试液,变红色;②另取少量残留液于试管中滴加适量氯化钡溶液,有白色沉淀,则残留液中有大量的( )

A.硫酸钠 B.碳酸钠 C.盐酸 D.氯化钠
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验小组探究盐酸和氢氧化钠反应过程中溶液pH的变化规律,得到如图所示曲线.下列有关该实验事实的说法正确的是( )
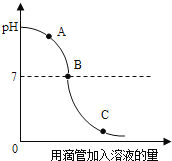
A.该实验是将氢氧化钠溶液滴入盐酸中
B.B点表示盐酸和氢氧化钠恰好完全反应
C.A点时的溶液能使酚酞试液变红
D.C点时,溶液中的溶质只有氯化钠
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如下图(夹持仪器已略),某兴趣小组在老师指导下,探究铁与水蒸气的反应,请回答。
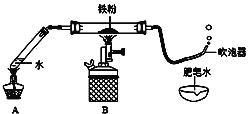
【实验初探】
(1)连接装置,并___________。
(2)装好药品。
(3)加热一段时间后,吹泡器连续吹出气泡,且气泡向上飞起,用燃着的木条靠近气泡,能产生爆鸣。
该气体燃烧的化学方程式为________。
【查阅资料】铁有三种氧化物(FeO、Fe2O3、Fe3O4)。
①它们都不溶于水,其中铁粉、Fe3O4能被磁铁吸引;②FeO接触到空气会立即由黑色变为红棕色;③三种氧化物都不与硫酸铜溶液反应,但能与酸反应生成可溶性物质。
【实验探究】实验小组同学对反应后的剩余固体进行探究。
(1)小梅发现固体为黑色,由此判断:固体中肯定不存在Fe2O3 ,理由是_______。
(2)小宇发现固体均能被磁铁吸引,大家倒出玻璃管中黑色固体,平铺于白纸上。观察现象是__________,判断黑色固体中一定没有FeO。
讨论:铁与水蒸气反应生成的固体是“铁的一种氧化物”,玻璃管内的黑色固体中还可能含有“过量的铁”。
【提出猜想】玻璃管中黑色固体成分有什么?
猜想Ⅰ:Fe; 猜想Ⅱ:Fe3O4; 猜想Ⅲ:______________
实验步骤 | 实验现象 | 实验结论 |
取上述固体少许,加入足量 _________________ | 出现红色固体,且有黑色固体残留 | 黑色固体中一定含有 ________________ |
【结论反思】(1)铁与水蒸气发生置换反应,反应的方程式是________________。
(2)出现红色固体的化学方程式是_______,加入的溶液必须足量的原因是______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】t2 ℃时,将甲,乙各80 g分别放到盛有100 g水的两个烧杯中,充分溶解后,恢复到t2 ℃,现象如图一。甲和乙的溶解度曲线如图二。请结合图示回答下列问题:

(1)固体甲对应的溶解度曲线是________(填“a”或“b”)。
(2)M点的含义________________________________________。
(3)向烧杯①的溶液中继续加入15 g甲物质,充分搅拌,发现固体先全部溶解,一段时间后又有部分固体甲析出。你认为“全部溶解”的原因是______________________________________。
(4)将t2 ℃等质量的甲、乙饱和溶液分别降温到t1 ℃时,所得溶液的有关说法正确的是________(填字母)。
a.甲溶液仍为饱和溶液
b.两溶液质量甲<乙
c.两溶液中溶剂质量甲=乙
d.两溶液溶质质量甲>乙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向装有等量水的A、B、C烧杯中分别加入10 g、25 g、25 g NaNO3固体,充分溶解后,现象如图一所示。
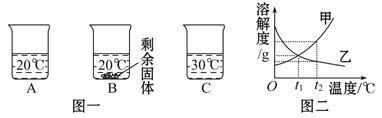
(1)烧杯中的溶液一定属于饱和溶液的是___________(填序号);
(2)图二中能表示NaNO3溶解度曲线的是___________(填“甲”或“乙”);
(3)要使B烧杯中剩余固体继续溶解,可采用的方法是_________________;
(4)由图二分析,若分别将100 g甲、乙的饱和溶液从t2 ℃降温到t1 ℃,对所得溶液的叙述正确的是______________(填序号)。
A.甲、乙都是饱和溶液 B.所含溶剂质量:甲<乙
C.溶液质量:甲>乙 D.溶质质量分数:甲>乙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2017年5月5日,中国首架无人机C919客机在浦东机场首飞成功。回答问题:
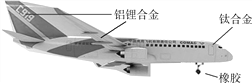
(1)图中标示的材料中,含有金属元素的是___________(写出一种即可)。
(2)飞机大量使用合金材料,原因是__________。铝的金属活动性比铁的________(填“强”或“弱”),空气中铝比铁具有更好的抗腐蚀性,原因是_____________(用化学方程式解释)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】粗盐中含有少量不溶性杂质(泥沙),还含有少量可溶性杂质(Na2SO4、CaCl2、MgCl2)。现以粗盐为原料制取精盐,生产过程如图所示
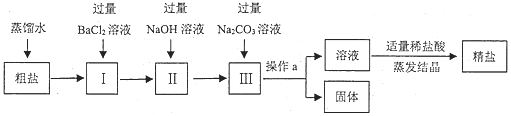
(1)写出I中发生反应的化学方程式__________;
(2)操作a的名称是_____,该操作需要用到的玻璃仪器主要有:烧杯、___、玻璃棒;
(3)加入适量稀盐酸的作用是除去溶液中的_______________(填化学式);
(4)在加热蒸发过程中,要用玻璃棒不断地搅拌,其目的是_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com