
【题目】教材中说到治病所用的药品,其实就是化学药品,用于治病,保护身体健康。如图是一种常见的止血药氨基乙酸的部分信息。请根据信息回答问题:

(1)氨基乙酸的相对分子质量是 。
(2)氨基乙酸中碳、氢、氮、氧元素的质量比是 。
(3)氨基乙酸中氮元素的质量分数是 。(结果保留到0.1%)
【答案】(1)131;(2)72:13:14:32;(3)10.7%
【解析】
(1)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答;
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答;
(3)根据化合物中元素的质量分数= ![]() ×100%,进行分析解答。
×100%,进行分析解答。
(1)氨基乙酸的相对分子质量是12×6+1×13+14+16×2=131,故填写:131;
(2)氨基乙酸中碳、氢、氮、氧元素的质量比是(12×6):(1×13):14:(16×2)=72:13:14:32,故填写:72:13:14:32;
(3)氨基乙酸中氮元素的质量分数是![]() ×100%≈10.7%,故填写:10.7%。
×100%≈10.7%,故填写:10.7%。


科目:初中化学 来源: 题型:
【题目】如图所示进行有关碳及其氧化物的性质实验,有关该实验说法正确的是( )
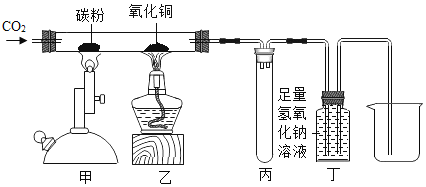
A.乙处固体减少的质量等于消耗的氧化铜中氧元素质量
B.丙装置的作用是收集未反应的一氧化碳
C.丁处氢氧化钠溶液改为澄清石灰水,可检验乙处生成的二氧化碳
D.该装置的不足之处是未进行尾气处理
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有两种物质在一定条件下能发生的反应(如下图所示),则下列说法正确的是( )

A.该反应属于分解反应
B.图中反应物均为化合物
C.该图示符合质量守恒定律
D.反应物和生成物的分子个数比为 1:1
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请根据下列实验装置图,回答有关问题:
Ⅰ.如图是初中化学中常见的实验。
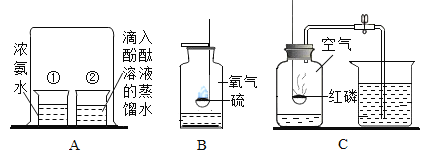
(1)A中现象:烧杯②中溶液变红。请用分子的知识解释“变红”的原因_________________。
(2)B中集气瓶底部有少量水,其作用是______________。
(3)C实验完毕,集气瓶内水面上升到一定高度后,不能继续上升,这种现象说明氮气具有________________的性质;若从烧杯中进入集气瓶内水的体积明显小于瓶内原空气体积的1/5,可能存在的原因是___________(写出一条即可)。
Ⅱ.实验室制取、收集、干燥气体的常用装置如图所示。请回答下列问题:
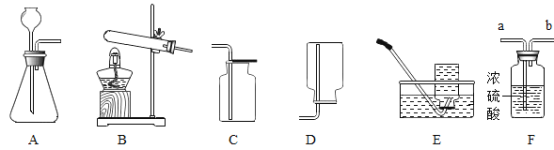
(1)实验室制取二氧化碳所选用的收集装置是_______________,反应的化学方程式是_________________。
(2)若用高锰酸钾制取氧气,并用排水法收集,实验操作步骤如下:①点燃酒精灯并收集气体②熄灭酒精灯 ③加入药品 并固定仪器④检查装置的气密性⑤从水槽中撒出导管。正确的操作顺序是_______(填字母 )
A③④①②⑤ B④③①②⑤ C④③①⑤② D①②③④⑤
(3)若要除去氧气中混有的水蒸气,气体应从F装置的____(填 a或b)端进入。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C、D、E分别是锌、硫酸、氢氧化钡、硫酸铜和碳酸钠五种物质中的一种,如图所示:

“﹣”表示相连的两种物质能够发生反应,其中D的溶液呈蓝色,A与B反应生成的气体是光合作用的原料之一。
(1)D的化学式是 。
(2)A与B反应的化学方程式 。
(3)C与D反应的化学方程式 ,属于基本反应类型中的 。
(4)下列可以替代E的是 (填序号)。
①氯化铜 ②氢氧化钾 ③银
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】20℃时,将等质量不含结晶水的甲、乙固体分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,加热到50℃时现象如图2(不考虑水分蒸发),甲、乙固体的溶解曲线如图3。下列说法错误的是()
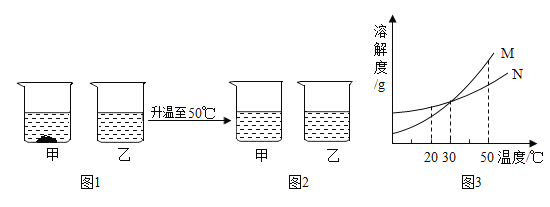
A.图1中,甲一定是饱和溶液B.图2中,两溶液中溶质的质量分数一定相等
C.图3中,M表示甲的溶解度曲线D.图2中,两溶液降温至30℃一定都不会析出晶体
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氯化钙在生活中常用作干燥剂、融雪剂,在工业上可用于制造防冻液等。某工厂以石灰石为原料生产二水合氯化钙(CaCl2·2H2O)流程如下。原料石灰石中含有的杂质主要是MgCO3、SiO2和Fe2O3。
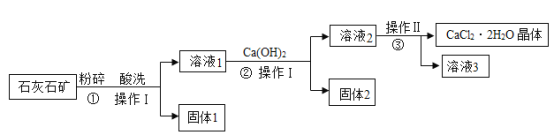
(1)第①步酸洗所用的酸是____________(填编号)。
A 稀盐酸 B 稀硫酸 C 浓硫酸 D 稀硝酸
(2)酸洗时酸与Fe2O3反应的化学方程式是______________。
(3)固体1的名称是__________。
(4)实验室中操作Ⅰ所用到的玻璃仪器有:玻璃棒、烧杯、__________。
(5)操作Ⅱ的名称是:蒸发浓缩、__________、__________。
(6)该流程中可循环利用的物质是__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】CaCO3在生产生活中有广泛的用途。
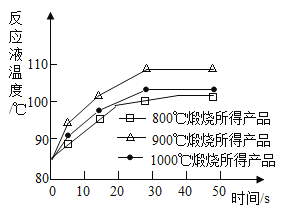
(1)烧石灰石可制得活性CaO,反应的化学方程式为_________________________。为测定不同煅烧温度对CaO活性的影响,取石灰石样品分为三等份,在同一设备中分别于800℃、900℃和1000℃条件下煅烧,所得固体分别与等质量的水完全反应,测得反应液温度随时间的变化如图所示。由此可知:CaO与水反应会__________热量(填“放出”或“吸收”),上述温度中,_________℃煅烧所得CaO活性最高。
(2)以电石渣[主要成分为Ca(OH)2还含有少量MgO等杂质]为原料制备高纯CaCO3的流程如下:
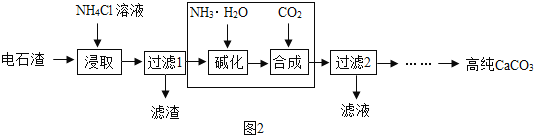

①上图为NH4Cl浓度对钙、镁浸出率的影响(![]() ),为进一步提升CaCO3的产量和纯度,据图分析,较适宜的NH4Cl溶液的质量分数为_______,浸取时主要反应的化学方程式为______________________________。
),为进一步提升CaCO3的产量和纯度,据图分析,较适宜的NH4Cl溶液的质量分数为_______,浸取时主要反应的化学方程式为______________________________。
②流程中框线内若改用溶液_________________(填化学式),可一步得到与原流程完全相同的生成物。
③流程中框线内若改用Na2CO3溶液,也能得到高纯CaCO3。试从生成物的角度分析原流程的优点:a.NH3可循环利用;b._______;
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图象与对应实验完全吻合的是
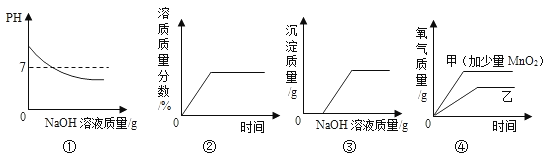
A.①往一定量的盐酸中滴加NaOH溶液至过量
B.②将一定量的不饱和KNO3溶液恒温蒸发水
C.③向一定量CuSO4溶液和稀硫酸的混合溶液中滴加NaOH溶液
D.④用两份等质量等溶质质量分数的过氧化氢溶液制取氧气(甲加少量MnO2)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com