




| 反应前 | 反应后 |  | ||
| A | B | C | D | |
 |  |  |  | |
分析 (1)①根据化学变化的实质:反应前后原子的种类和个数都不变进行分析;
②根据复分解反应的实质是产生难电离的物质进行分析;
(2)根据分子式前面的数字表示分子的个数,根据元素符号右上角的数字表示离子所带电荷数进行解答;
(3)首先要对模型图进行观察,分析物质的微观构成、物质的类别,再找出物质之间的微粒数目关系,然后再对题中各问加以分析解答;
(4)根据酸碱中和反应、氢离子与碳酸根离子反应等方面进行分析;
(5)①根据单质化合价为零进行分析;
②根据化学式的写法写出化学式;
③根据方程式的写法写出化学方程式;
(6)根据在化学变化中,分子分解成原子,原子再重新结合成新的分子进行分析;
(7)根据氧化物是指由两种元素组成且一种是氧元素的化合物进行分析.
解答 解:(1)①根据质量守恒定律分析可知,电解水时,每两个水分子会产生两个氢分子和一个氧分子,故缺少一个氢分子,选B;
②稀盐酸与硝酸银溶液反应属于复分解反应,根据反应实质可知,盐酸中的氯离子与硝酸银中的银离子结合成氯化银白色沉淀.
(2)根据化学式前的数字表示分子子的个数,故“2”表示2个分子子的是①;根据元素符号右上角的数字表示离子所带电荷数可知,表示每个微粒带2个单位电荷的是②;
(3)依据图示的分子结构可知该反应的化学方程式为:4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O;依据图示的分子结构可知该反应的化学方程式为:4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O;
A、由方程式可知,反应前后一共有3种原子,故A错误;
B、由方程式可知,该反应有单质氮气生成,故B正确;
C、该反应有单质氮气生成,元素在单质中化合价为零,故反应前后一定有化合价的变化,故C错误;
D、由微粒的变化可知,化学变化中分子可再分,原子不可再分.故D错误;
E、由方程式可知,甲、丁两种分子的个数比是2:3,故E正确;
故选:BE;
(4)胃酸的主要成分为盐酸,①Mg(OH)2中氢氧根离子能与胃酸中的盐酸中的氢离子发生中和反应生成水,从而起到中和胃酸的作用.②AlMg(OH)3CO3中的OH-、CO32-都能中和胃酸中的氢离子;
(5)①单质化合价为零,由图示可知A点物质的化合价是零,所以物质类别是单质;
②B点是铁的氧化物,铁的化合价是2,所以物质是氧化亚铁,化学式是FeO;
③由于C点是铁的+2价的碱,属于氢氧化亚铁,D是+3价铁的碱,即氢氧化铁,由题给信息可知,反应物是氢氧化亚铁、氧气和水,生成物是氢氧化铁,用观察法配平,化学方程式是:4Fe(OH)2+O2+2H2O=4Fe(OH)3;
④铵根的化合价是+1价,硫酸根的化合价是-2价,设铁元素化合价是x则:(+1)×2+x+(-2)×2=0,解得x=+2,该物质属于盐,所以是E点;
(6)水电解的过程可用下列图示表示,微粒运动变化的先后顺序是:水分子分解成氢原子和氧原子,氢原子和氢原子结合成氢分子,氧原子和氧原子结合成氧分子,所以正确的顺序是:④③①②;
(7)通过分析图示可知,A是二氧化碳,B是氢气,C是水,d是甲烷,所以属于氧化物的化学式是:H2O、CO2,根据反应和生成物的关系可以得出反应的化学方程式为 CO2+4H2═CH4+2H2O,所以A、C两种物质的质量比是44:36=11:9.
故答案为:(1)①B;
②AgCl;
(2)①,②;
(3)BE;
(4)OH-、CO32-;
(5)①单质;
②FeO;
③4Fe(OH)2+O2+2H2O=4Fe(OH)3;
④E;
(6)④③①②;
(7)H2O、CO2,11:9.
点评 本题对微粒的结构、微观反应过程、化学变化的实质及复分解反应的条件的考查,难度不大,依据相关的知识解决.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 红磷 | B. | 硫 | C. | 木炭粉 | D. | 铝粉 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 事实 | 解释 | |
| A | 氧气用于金属切割 | 氧气具有可燃性 |
| B | 二氧化碳能灭火 | 二氧化碳不燃烧,也不支持燃烧 |
| C | 墨汁写的字或作的画可永久保存 | 碳的化学性质在任何条件都不活泼 |
| D | 做铁丝燃烧实验时的集气瓶底部预先留少量水 | 吸收铁燃烧生成的有害气体 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 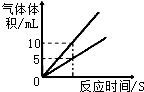 将水通电一段时间 | |
| B. | 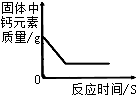 20℃时把少量氧化钙放入饱和氢氧化钙溶液中 | |
| C. | 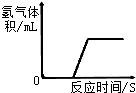 将未打磨过的铝片放入足量的稀盐酸中 | |
| D. | 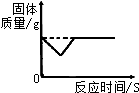 加热一定量高锰酸钾制氧气 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 Ⅰ.用化学用语表示:
Ⅰ.用化学用语表示:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com