
【题目】某兴趣小组利用实验室制CO2的废液得到CaCO3和NaCl晶体,过程如下:
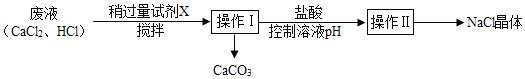
下列说法中正确的是( )
A. 试剂X可选用Na2CO3溶液
B. 操作Ⅰ、Ⅱ的名称都是过滤
C. 操作I需要用到的玻璃仪器有玻璃棒、漏斗和量筒
D. 稍过量的试剂X加入到废液中观察到的现象是先有沉淀后有气泡
 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:初中化学 来源: 题型:
【题目】下列各图是 O2、CO2 的实验室制取和有关性质的实验装置。

(1)写出标号 a 的仪器名称:_____。
(2)用氯酸钾和二氧化锰固体制取 O2,应选用上图中的_____装置(填字母);反应的化学方程式为_____。
(3)用稀盐酸和大理石在 B 装置中反应制取 CO2 并检验其有关性质,观察到烧杯中导管口有气泡冒出,但无其它明显现象。若证明 CO2 与 NaOH 溶液发生了化学反应,以下方案合理的是_____(填序号)。
I、取少量烧杯中液体滴加足量稀盐酸
II、取少量烧杯中液体滴加无色酚酞
III、取少量烧杯中液体滴加氯化钡溶液
(4)C 装置_____(填“具有”或“不具有”)启普发生器功能。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示,在小烧杯A中装入30mL蒸馏水,再滴入3滴酚酞,在小烧杯B中装入30mL浓氨水。用一大烧杯把A、B两个烧杯罩在一起,过一段时间后看到的现象是_____________,该实验说明_______________________。该实验采用了_____________实验方法。大家对实验现象产生不同看法:
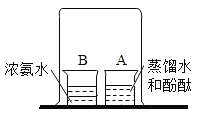
(1)有人认为是A烧杯中的蒸馏水使酚酞试液变红;
(2)又有人认为B烧杯中的浓氨水挥发出氨气,扩散到A烧杯的溶液中使酚酞试液变红。你认可看法是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某校化学兴趣小组利用数字化传感器探究稀盐酸和氢氧化钠溶液的反应过程,测得烧杯中溶液的pH随滴加液体体积变化的曲线如图所示。下列说法正确的是

A.图中a点所示溶液中,含有的溶质是NaCl和Na0H
B.由a点到b点的pH变化过程证明酸和碱发生了中和反应
C.向图中c点所示溶液中滴加无色酚酞,溶液不变色
D.该实验是将盐酸逐滴滴入到盛有氢氧化钠溶液的烧杯中
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列装置常用于实验室制取气体。根据给出的装置回答下列问题。
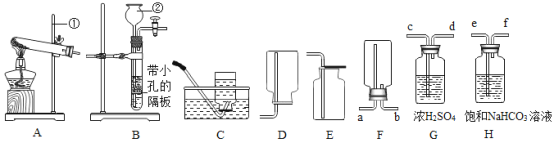
(1)指出编号仪器名称:①_____,②_____。
(2)实验室利用A装置制取氧气,反应原理用化学方程式表示为_____。
(3)制取并收集二氧化碳应选择的装置是_____(从A-E中选择),使用该套装置制取气体的突出优点是_____,该反应原理用化学方程式表示为_____。改用F装置收集二氧化碳,则气体应从_____端进入。制得的二氧化碳中常含有少量的氯化氢气体与水蒸气,欲使用G、H装置将以上杂质气体除去则装置正确的连接顺序是:混合气体→_____(用端口字母表示)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图象能正确反映对应变化关系的是
A.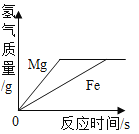 足量的铁片与镁条分别与等质量、等质量分数的稀硫酸反应
足量的铁片与镁条分别与等质量、等质量分数的稀硫酸反应
B.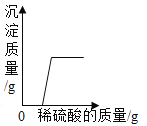 向氢氧化钠和氯化钡的混合溶液中逐滴加入稀硫酸
向氢氧化钠和氯化钡的混合溶液中逐滴加入稀硫酸
C.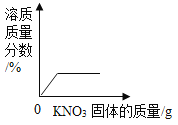 在一定温度下向接近饱和的KNO3溶液中加入KNO3固体
在一定温度下向接近饱和的KNO3溶液中加入KNO3固体
D.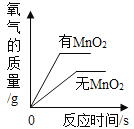 等质量的氯酸钾在有、无MnO2的情况下加热产生氧气
等质量的氯酸钾在有、无MnO2的情况下加热产生氧气
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】往200克含有稀硝酸和硝酸钙的混合溶液中,加入21.2%的碳酸钠溶液,所得溶液的pH变化与加入碳酸钠溶液的质量关系如图(假设生成的气体全部逸出),试分析计算:
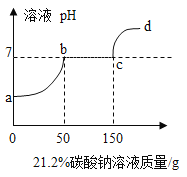
(1)a→b段发生反应的化学方程式为_____;
(2)反应到c点时,所得溶液的溶质质量分数是多少?_____(写出计算过程,精确到0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室中分别用高锰酸钾、过氧化氢、氯酸钾制取比较纯净的氧气。请结合图回答问题:
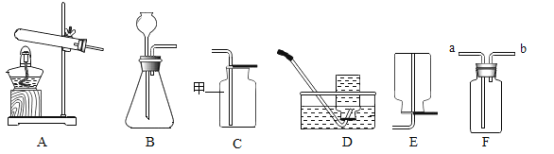
(1)写出甲所指仪器名称:_____;组装A装置时,固定试管应在放置酒精灯之_____(选填“前”或“后”)进行。
(2)欲用高锰酸钾制取比较纯净的氧气,则应选择的装置组合是_____,反应的化学方程式为_____,该反应属于_____反应。若用该装置收集的氧气也不纯,原因可能是_____。
(3)查阅资料知,高铁酸钾(K2FeO4)固体可用于制取氧气。
方案一:4K2FeO4![]() 2Fe2O3+4K2O+3O2↑
2Fe2O3+4K2O+3O2↑
方案二:4 K2FeO4+10H2O=4Fe(OH)3↓+8KOH+3O2↑
①若用方案二制取氧气,应该选用的发生装置是_____(填装置序号)。选用图F装置用排空气法收集氧气时,氧气应该从_____(填“a”或“b”)端通入。
②下列关于以上两种方案制取氧气的说法正确的是_____(填序号)
a.方案一发生的是分解反应
b.方案二更简便、节能
c.制取等质量的氧气,两种方案所需高铁酸钾的质量相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】胃舒平(含Al(OH)3)、小苏打片(含NaHCO3)、胃酸抑制剂(主要含CaCO3、Mg(OH)2)都是常用的中和胃酸的药物。
(1)胃舒平与胃酸发生反应的化学方程式为:_____。
(2)为了探究工业小苏打中是否含少量的NaCl,设计如下实验:(假设小苏打片中其他物质均不含Cl-)
实验步骤 | 实验现象 | 实验结论 |
第一步:取1片小苏打于试管中,加入适量水充分溶解,再滴加足量的稀HNO3。 | 有_____产生 | 说明小苏打片中含有NaHCO3。 |
第二步:再往上述溶液中滴加少量_____溶液。(写化学式) | 有_____产生 | 说明小苏打片中含有NaCl。 |
(3)胃酸抑制剂每片lg,取10片于烧杯中,再加入50g稀HCl,烧杯中剩余物的质量与时间的关系如下表:(已知其他物质不与稀盐酸反应)
时间/s | 0 | 10 | 20 | 30 | 40 | 50 |
剩余物的质量/g | 60 | 59.12 | 58.24 | 57.36 | 56.48 | 56.48 |
求每片胃酸抑制剂中CaCO3的质量分数_____(写出计算过程)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com