
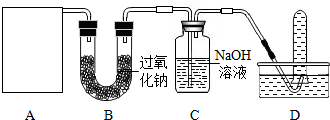
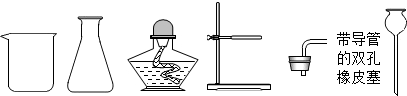
| 实验步骤 | 实验现象 | 实验结论及方程式 |
| ①取少量B中反应后的固体于试管中; ② ③将生成的气体通入澄清的石灰水中. | ②有气泡产生 ③ | 反应后生成的固体是碳酸钠 |
| 实验步骤 | 实验现象 |
| ②滴加稀盐酸 ③将生成的气体通入澄清石灰水中 | ②有气泡产生 ③澄清石灰水变浑浊 |


科目:初中化学 来源: 题型:
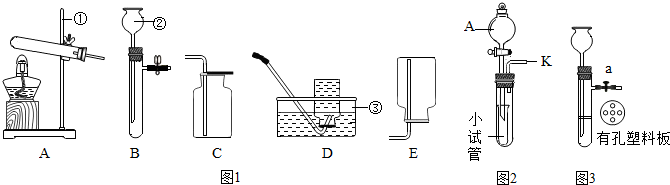
| 仪器名称 | 分液漏斗 | 小试管 | 大试管 |
| 装置内的药品 | ① | ② | 紫色石蕊试液 |
| 大试管中产生的现象及发生反应的化学方程式 | 现象 ③ | ||
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
A、H2O2
| ||||
B、2H2O
| ||||
| C、H2SO4+NaOH═NaSO4+H2O | ||||
D、4P+5O2
|
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、用完酒精灯后用嘴去吹灭 |
| B、过滤时将待滤液直接倒入漏斗里 |
| C、实验剩余药品不要随意丢弃,应放回原瓶 |
| D、使用量筒量液读数时,视线应与量筒内液体凹液面的最低处保持水平 |
查看答案和解析>>
科目:初中化学 来源: 题型:
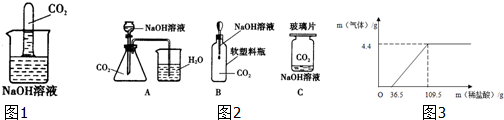
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com