
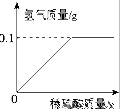
 为研究黄铜(铜锌合金)的组成,某学习小组称取该样品10g,向其中逐滴加稀硫酸至刚好不再产生气体为止.生成的气体与所用硫酸溶液的质量关系如图所示,请计算:10g样品中铜的质量是多少克?
为研究黄铜(铜锌合金)的组成,某学习小组称取该样品10g,向其中逐滴加稀硫酸至刚好不再产生气体为止.生成的气体与所用硫酸溶液的质量关系如图所示,请计算:10g样品中铜的质量是多少克? 科目:初中化学 来源: 题型:实验探究题
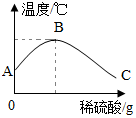 学习酸碱中和反应时,很多同学对其产生了探究兴趣.
学习酸碱中和反应时,很多同学对其产生了探究兴趣.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
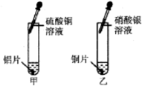
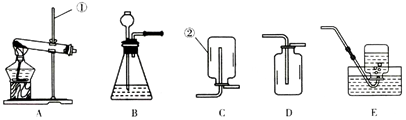
| A. | 胶头滴管的使用方法操作正确 | |
| B. | 该实验能得出金属活动性顺序为银>铜>铝 | |
| C. | 甲、乙中观察到的实验现象相同 | |
| D. | 甲、乙中发生的反应都属于置换反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com