
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写;再根据反应特征确定反应类型.
解答 解:(1)硫在氧气中燃烧生成二氧化硫,反应的化学方程式为S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2;该反应符合“多变一”的特征,属于化合反应.
(2)过氧化氢溶液中加入硫酸铜,硫酸铜作催化剂,反应的化学方程式为2H2O2$\frac{\underline{\;CuSO_{4}\;}}{\;}$2H2O+O2↑;该反应符合“一变多”的特征,属于分解反应.
(3)氢气与氧化铜在加热条件下反应生成铜和水,反应的化学方程式为:H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O.
故答案为:(1)S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2;化合;(2)2H2O2$\frac{\underline{\;CuSO_{4}\;}}{\;}$2H2O+O2↑;分解;(3)H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O.
点评 本题难度不大,考查学生根据反应原理书写化学方程式、判定反应类型的能力,掌握化学方程式的书写方法(写、配、注、等)、四种基本反应类型的特征即可正确解答本题.


科目:初中化学 来源: 题型:选择题
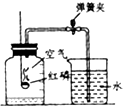 某同学用燃烧红磷的方法测定空气中氧气体积分数,实验后发现测得氧气的体积分数小于$\frac{1}{5}$.下列关于该实验的分析及后续做法不合理的是( )
某同学用燃烧红磷的方法测定空气中氧气体积分数,实验后发现测得氧气的体积分数小于$\frac{1}{5}$.下列关于该实验的分析及后续做法不合理的是( )| A. | 可能红磷的量不足,没有除尽氧气 | |
| B. | 可能没有冷却至室温就打开止水夹,进入瓶内的水减少 | |
| C. | 检查确认实验装置不漏气后,重新实验 | |
| D. | 将红磷改成足量的木炭,重新实验 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 钛属于非金属元素 | B. | 钛的原子序数为22 | ||
| C. | 钛原子的相对原子质量为47.87 | D. | 钛原子核内质子数为22 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com