
【题目】甲、乙两种固体物质的溶解度曲线如图所示。下列叙述正确的是()
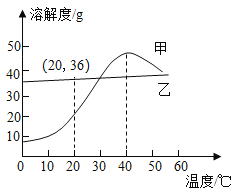
A.甲的溶解度随温度的升高而增大
B.40°C时,使甲的饱和溶液析出晶体可用升温、降温和蒸发溶剂三种方法
C.20°C时,向125g溶质质量分数为20%的乙溶液中加入15g乙固体并振荡,固体全部溶解
D.将相同质量的甲和乙的饱和溶液分别从40°C降温至10°C,乙没有晶体析出
【答案】B
【解析】
由甲、乙两种固体物质的溶解度曲线图可知,甲的溶解度在0~40°C时,随温度的升高而增大,40°C以后,溶解度随温度的升高而减小,乙的溶解度受温度的影响较小。
A、由溶解度曲线图可知,甲的溶解度在0~40°C时,随温度的升高而增大,故A不正确;
B、甲的溶解度在0~40°C时,随温度的升高而增大,40°C以后,甲的溶解度随温度的升高而减小,40°C时,使甲的饱和溶液析出晶体可用升温、降温和蒸发溶剂三种方法,故B正确;
C、由溶解度曲线图可知,20°C时,乙物质的溶解度为36g,125g溶质质量分数为20%的乙溶液中乙固体的质量为![]() ,则向125g溶质质量分数为20%的乙溶液中加入15g乙固体并振荡,固体部分溶解,故C不正确;
,则向125g溶质质量分数为20%的乙溶液中加入15g乙固体并振荡,固体部分溶解,故C不正确;
D、甲乙的溶解度均随温度的升高而增大,乙的溶解度受温度的影响较小,将相同质量的甲和乙的饱和溶液分别从40°C降温至10°C,乙有少量的晶体析出,故D不正确。故选B。


科目:初中化学 来源: 题型:
【题目】脐橙含有丰富的维生素C和维生素P(化学式为C27H30O16),可以增加体内高密度脂蛋白(HDL)的含量,从而降低患心脏病的可能性。下列有关说法正确的是
A.维生素P的相对分子质量为610 g
B.维生素P中H的质量分数为4.92%
C.维生素P中三种元素的质量比为27:30:16
D.维生素P是由27个碳原子、30个氢原子和16个氧原子构成
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在实验室制取二氧化碳气体后,小明向反应后滤液甲中逐滴加入碳酸钠溶液,测得滤液 pH随加入碳酸钠溶液质量的变化曲线如图所示。通过分析该图可推理出的结论正确的是( )
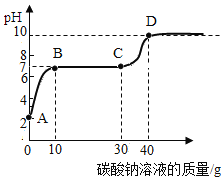
A.滤液甲中只有一种溶质
B.BC段反应过程中无明显现象
C.CD段没有新物质生成
D.最终溶液的pH将接近14
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】儿童缺锌会引起食欲不振、发育不良等症状。如图为某补锌口服液说明书的部分信息,回答下列问题:

(1)葡萄糖酸锌的相对分子质量为 ;
(2)葡萄糖酸锌中碳、氢、氧元素的原子个数最简比为 ;
(3)要满足儿童身体正常发育的需要,在某一时间段需要适量补锌。
若儿童1千克体重每日需要0.5毫克锌,每天从食物中只能摄入所需锌的一半。体重为20千克的儿童,理论上一天还需服该口服液多少支?(请写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】芯片的核心材料是高纯硅,下图是利用石英砂(主要成分SiO2)制取高纯硅的流程图,请回 答下列问题:
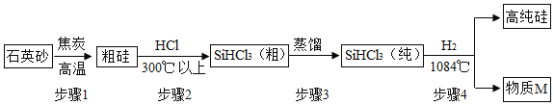
(1)SiO2与金刚石结构相似,则构成SiO2的粒子是__(填“分子”、“原子”或“离子”)。
(2)步骤 1 发生的反应为:SiO2+ 2C![]() Si + 2X↑,上述反应中 X 是______(填化学式),其中SiO2发生了______(填“氧化”或“还原”)反应。
Si + 2X↑,上述反应中 X 是______(填化学式),其中SiO2发生了______(填“氧化”或“还原”)反应。
(3)步骤 3 中“蒸馏”属于__(填“物理”或“化学”)变化。
(4)步骤 4 中物质 M 在该生产过程中可循环使用,写出步骤 4 反应的化学方程式:______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】的输化输机大显身手,多次向武汉空医疗队员和物资,驰援湖北。制造运输机的过程中使用金属材料。回答问题:
(1)金属的存在:金以单质形式存在于自然界,原因是______。
(2)金属的冶炼:高炉炼铁以赤铁矿(主要成分是Fe2O3) 为原料,其原理为______ (写化学方程式)。
(3)金属的利用:利用铁炭混合物(铁屑和活性炭的混合物)处理含有Cu(NO3)2、Pb(NO3)2的废水。相同条件下,测量总质量相同、铁的质量分数不同的铁炭混合物对水中重金属离子的去除率,实验结果如图所示。铁炭混合物中为铁的质量分数50%时,水中的Cu2+、Pb2+能被有效除去,用文字和化学方程式说明除去Pb2+的原因_______。
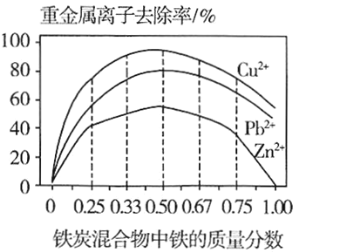
(4)金属的保护:下列钢铁制品的防护措施不合理的是______(填字母序号)。
A 车船的表面喷涂油漆
B 使用后的菜刀用布擦干
C 铁制品表面镀一层铬
D 使用洗涤剂把铁制品表面的油污洗净
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有一种在古籍里称为“鋈”的银白色铜合金,是古代云南、四川地区的特产,其主要成分是铜、锌、镍等金属单质,炼制时需要黑铜矿(主要成分是CuO)、硫化镍矿(主要成分是Ni2S3)等多种矿物。下列有关说法不正确的是
A.鋈属于金属材料
B.鋈的样品在足量稀盐酸中能全部溶解
C.Ni2S3中镍元素呈+3价
D.黑铜矿跟木炭共热能生成单质铜
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室常利用以下装置完成气体制备及性质实验。请回答:
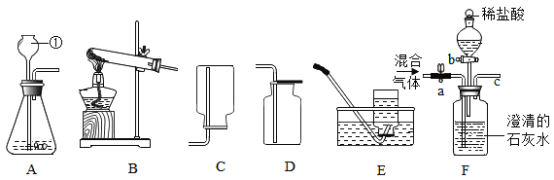
(1)写出图中标号①的仪器名称:_________________。
(2)欲使用高锰酸钾制取氧气,应选择的发生装置是________________(填标号),写出反应化学方程式_________________。若使用E装置收集氧气,实验结束时,应先从水槽中移出导气管,再熄灭酒精灯,原因是_________________。
(3)将CO2和CO的混合气体通过F装置(液体药品均足量)
①实验开始时关闭活塞b,打开活塞a,广口瓶中观察到的现象是_________________。
②待充分反应后,再关闭活塞a,打开活塞b,将分液漏斗中的稀盐酸滴入广口瓶中,一段时间后,用燃着的木条放c处发现木条熄灭,则此时逸出的气体主要成分是_________________, 写出 该反应的化学方程式_________________,欲收集该气体,最适合选择的装置是________________(填标号)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属在生活、生产中应用广泛。
(1)从微观角度分析,水银温度计测量体温的原理是____________________________。
(2)写出工业上用赤铁矿石炼铁的化学方程式____________________________________。
(3)下图是光亮铁钉的一系列变化。
![]()
①中铁钉锈蚀主要是铁与空气中的____________发生化学反应。
②中稀盐酸除铁锈的化学方程式为____________________________。
③中所用的溶液X中的金属阳离子为 _________(用符号表示)。
(4)为验证Fe、Cu、Ag三种金属的活动性顺序,下列选用的药品可行的是____(填字母)。
A Fe、CuSO4溶液、Ag B FeSO4溶液、Cu、Ag
C FeSO4溶液、Cu、AgNO3溶液D FeSO4溶液、CuSO4溶液、Ag
(5)某金属粉末可能由铁、镁、锌、铝、银中的一种或几种组成。取该样品2.4g,向其中加入100g一定溶质量分数的稀硫酸,恰好完全反应,生成0.2g氢气,得到无色溶液,固体无剩余。下列说法正确的是__________(填字母)。
A 样品中一定含有锌 B 样品中一定不含有银,可能含有铁
C 所得溶液中溶质总质量为12g D 加入的稀硫酸的溶质质量分数为9.8%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com