
| A. | 反应后液体的酸性减弱,PH减小 | B. | 反应所得的滤液,可直接排放 | ||
| C. | 滤渣中一定含有铜和铁 | D. | 发生的反应都是置换反应 |
分析 在金属活动性顺序中,铁排在铜和氢的前边,可以和稀盐酸及氯化铜溶液反应.
解答 解:A、反应后液体的酸性减弱,pH应该变大,不是变小,故此项错误.
B、实验所得滤液中至少含有硫酸亚因此不是纯水,不可直接排放,此项错误.
C、滤渣中一定含铜和铁,错误,如果铁的量比较少,没有能消耗完酸与氯化铜,滤渣中就不可能有铁,此项错误.
D、因为金属和盐、金属和酸发生的反应都是置换反应,所以铁与盐酸及氯化铜的反应均属置换反应.
故选D.
点评 本题考查的金属与混合盐溶液的反应,完成此题,可以依据金属活动性顺序以及题干提供的信息进行.所以要求同学们在平时的学习中加强基础知识的记忆,以便能够灵活应用.


科目:初中化学 来源: 题型:选择题
| 选项 | 物质(括号内为杂质) | 去除杂质的方法 |
| A | Fe(Cu) | 加过量FeSO4溶液、过滤 |
| B | CaO(CaCO3) | 加足量的水、过滤 |
| C | NaCl溶液(Na2CO3) | 加入适量的CaCl2溶液、过滤 |
| D | HNO3溶液(H2SO4) | 加适量BaCl2溶液、过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
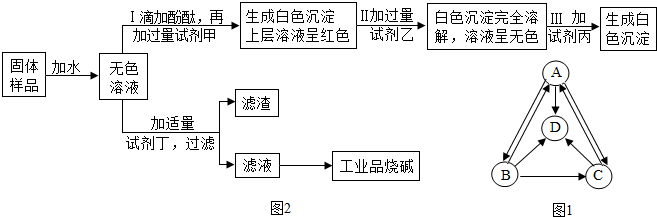
| 实验步骤 | 实验现象 |
| Ⅰ.向样品溶液中滴加酚酞溶液 | 溶液呈红色 |
| Ⅱ.向样品溶液中滴加稀硫酸, 并用玻璃棒搅拌 | 滴加一定量稀硫酸后溶液中开始产生气泡 溶液仍呈红色 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 红磷燃烧产生大量的白烟 | |
| B. | 镁条燃烧发出白光,生成黑色固体 | |
| C. | 铁丝在氧气中剧烈燃烧、火星四射、产生白色固体 | |
| D. | 分别点燃一小块棉纤维和羊毛纤维,都产生了烧焦羽毛的气味 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 2012年4月15日,央视《每周质量报告》报道了部分药品生产企业使用铬超标胶囊生产药品的问题.铬虽然是人体必需的一种微量元素,但过量的摄入会对人体造成危害,影响人体的抗氧化系统,溶液得糖尿病、高血压、肿瘤等多种疾病.请回答下列问题:
2012年4月15日,央视《每周质量报告》报道了部分药品生产企业使用铬超标胶囊生产药品的问题.铬虽然是人体必需的一种微量元素,但过量的摄入会对人体造成危害,影响人体的抗氧化系统,溶液得糖尿病、高血压、肿瘤等多种疾病.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
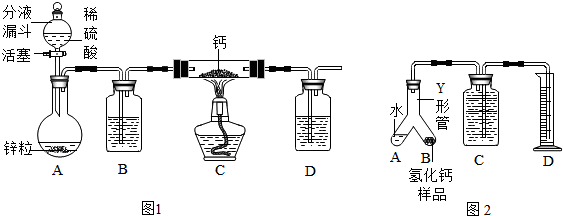
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com