
【题目】如图是一氧化碳还原氧化铁的装置,
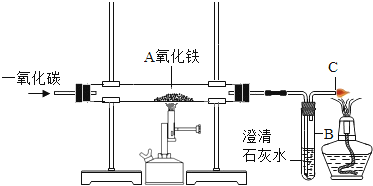
(1)该实验过程中A玻璃管内发生的现象是_____,反应的化学方程式_____。B试管中观察到的现象是_____,反应的化学方程式_____。
(2)酒精灯的作用是_____。
【答案】红棕色固体粉末变黑 3CO+Fe2O3![]() 2Fe+3CO2 澄清石灰水变浑浊 Ca(OH)2+CO2═CaCO3↓+H2O 将未参加反应的一氧化碳点燃,防止污染空气
2Fe+3CO2 澄清石灰水变浑浊 Ca(OH)2+CO2═CaCO3↓+H2O 将未参加反应的一氧化碳点燃,防止污染空气
【解析】
(1)A中,氧化铁在高温的条件下反应生成铁和二氧化碳,观察到红棕色固体慢慢变成黑色;二氧化碳与氢氧化该反应生成碳酸钙沉淀和水,所以观察到澄清的石灰水变浑浊;故填:红棕色固体粉末变黑;3CO+Fe2O3![]() 2Fe+3CO2;澄清石灰水变浑浊;Ca(OH)2+CO2═CaCO3↓+H2O;
2Fe+3CO2;澄清石灰水变浑浊;Ca(OH)2+CO2═CaCO3↓+H2O;
(2)最后的尾气中还含有一氧化碳,它有毒,不能直接排入大气中,可以把它燃烧,使其转化为二氧化碳再排入大气中;故填:将未参加反应的一氧化碳点燃,防止污染空气。


 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:初中化学 来源: 题型:
【题目】请用化学方程式解释下列现象:
(1)可以服用小苏打治疗胃酸过多_____。
(2)铝制品不易锈蚀_____。
(3)铁桶不能盛放波尔多液_____。
(4)常用稀盐酸除铁锈_____。
(5)石灰浆粉刷墙壁,干燥后墙面变硬_____。
(6)氢气作为最理想的燃料_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据图回答问题。
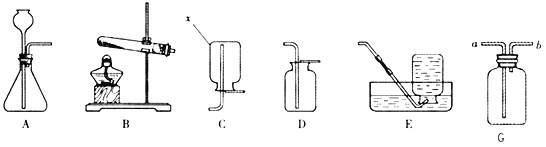
(1)仪器x的名称是_____。
(2)实验室制取氧气、二氧化碳和氢气都可以选用_____。(填字母序号)作为发生装置;收集二氧化碳选用D装置的原因是_____。
(3)如图G装置可用于气体的收集、检验、除杂等,用该装置能完成的实验是_____(填字母序号)。
A.气体从b端通入,收集氢气
B.瓶内装满水,氧气从a端通入,收集氧气
C.瓶内装有澄清石灰水,气体从a端通入,检验氧气中是否混有二氧化碳
D.瓶内装有浓硫酸,气体从b端通入,吸收氢气中混有的水蒸气
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某混合气体可能含有CO、H2、CO2中的两种或三种。某兴趣小组通过实验探究其成分。
(查阅资料)无水硫酸铜为白色粉末,遇水变蓝色。
(提出问题)混合气体由哪些气体组成?
(提出猜想)猜想一:混合气体是CO、CO2; 猜想二:混合气体是CO、H2;
猜想三:混合气体是_______; 猜想四:混合气体是CO、H2、CO2。
(设计实验)将混合气体依次通过下列装置。
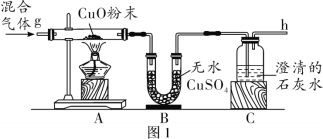
(观察现象)A中黑色固体变红色,B中无水硫酸铜变蓝色,C中澄清石灰水变浑浊。
(讨论交流)
(1)无水硫酸铜变蓝色,则猜想_______不成立;
(2)小华认为澄清石灰水变浑浊,原混合气体中一定含有CO2,小军认为小华的说法不正确,理由是_______;
(3)小丽认为在A装置前连接如图2三个装置就可以确定气体成分,则各仪器的接口连接顺序为:_______→g→h,其中NaOH溶液的作用是_______,按小丽改进后的装 置重新实验,观察到的现象是:A中黑色固体变红色,B中无水硫酸铜变蓝色,_______。则猜想四成立,写出C中反应的化学方程式_______。
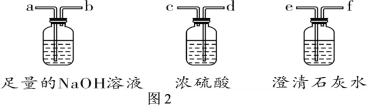
(4)指导老师指出小丽改进后的实验装置还存在一处不足,你的改进措施是_______。
(5)碳酸氢钙[Ca(HCO3)2]的水溶液遇热时,碳酸氢钙会分解生成碳酸钙、二氧化碳和水,将一定质量的Ca(HCO3)2溶液加热使Ca(HCO3)2完全分解,冷却后分离混合物,称得沉淀的质量为10g,所得液体的质量 为185.6g(不考虑CO2的溶解,忽略加热、分离过程中液体的质量损失)。请计算加热前原溶液中钙元素的质量分数为_______(写出计算过程)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据如图所示的实验回答问题。
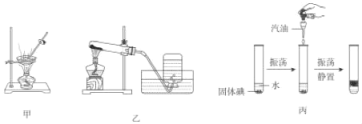
(1)甲实验时必须边加热边搅拌,等到_____时停止加热。
(2)乙实验中当观察到_____才开始收集氧气;使用乙装置制取的气体应满足的条件是_____。
(3)丙实验是某同学所做的物质溶解实验,该实验的目的是_____,对加入汽油量的要求是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】生活中常遇见铜制品生锈的情况.活动课上,同学们设计实验对铜锈进行了如下探究活动.
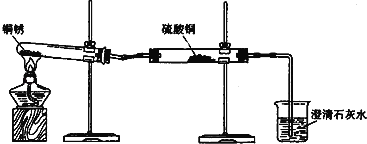
探究活动一:验证铜锈的组成
【査阅资料】①铜锈为绿色,其主要成分是Cu2(OH)2CO3.②白色的硫酸铜粉末遇水能变为蓝色.③碳不与稀硫酸反应.④氧化铜为黑色固体,能与稀硫酸反应生成硫酸铜溶液.
【进行实验1】同学们设计了如图所示装置并进行实验.
实验橾作 | 实验现象 | 实验结论 |
①按如图组装仪器,装入药品. ②加热铜锈,直至不再有气体产生,停止加热. | 绿色固体变为黑色;硫酸铜粉末变为蓝色;烧杯中液体变浑浊. | 加热铜锈生成的物质有 ; 铜绣由 元素组成; 烧杯中发生反应的化学方程式为 . |
③冷却后,向试管中固体 加入适量稀硫酸,稍加热. | 黑色固体溶解,溶液变 为蓝色. |
【进行实验2】同学们进行了下面的4个实验,每天观察一次现象,一段时间后,发现只有实验4中的铜丝生锈了,且与水接触的部分生锈更明显.
序号 | 实验内容 | 实验结论 | 实验反思 |
实验1 |
| 在干燥环境中,铜不易生锈 | (1)实验2和3中使用的是经煮沸后迅速冷却的蒸馏水,其原因是 . (2)如果要证明铜生锈的快慢是否与二氧化碳的浓度有关,还需要补充的一个实验内容是 |
实验2 |
| ||
实验3 |
| ||
实验4 |
| 铜生锈的条件是
|
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某纯碱样品中含有少量NaCl,小丽同学取该样品23g全部溶解于150g水中,再逐滴加入160g稀盐酸,反应中产生的气体的质量与盐酸的用量关系如图所示。(提示:相关反应为Na2CO3+2HCl=2NaCl+H2O+CO2↑)计算当恰好完全反应时:
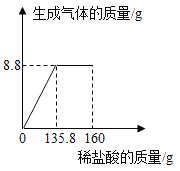
(1)产生的二氧化碳的质量是 克。
(2)此时所得到的溶液中溶质的质量分数(写出必要的计算过程,结果保留到0.1%)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某课外活动小组同学用图中装置(固定装置未画出)测定含有杂质的镁带中镁单质的质量分数(杂质与酸接触不产生气体)。实验过程如下:
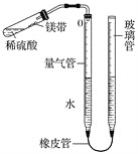
①取一段镁带样品,准确称得其质量为0.030 g;
②往量气管内装水至低于刻度“0”的位置,如图所示,(未装药品)装配好仪器;
③_________________________;
④在试管中加入足量的稀硫酸,稍倾斜试管,将用水湿润的镁带小心贴在试管壁上,塞紧橡皮塞;
⑤调整量气管液面,使两边的液面保持同一水平,记录量气管中液面位置;
⑥把试管底部略为抬高,使镁带与稀硫酸接触完全反应;
⑦待冷却至室温后,再次记录量气管中液面位置;
⑧算出量气管中增加的气体体积为23.96 mL;
已知:同温同压下,不同气体混合后体积等于混合前各气体体积之和。
请回答下列问题:
(1)写出镁与稀硫酸反应的化学方程式:____________________。
(2)能否用托盘天平称量0.030 g镁带样品________(填“能”或“不能”)。
(3)操作③是_________________________。
(4)实验过程⑦中再次记录量气管的液面位置时,试管中留有氢气,是否会影响实验最终结果________(填“是”或“否”),理由是_______________________。
(5)若实际测得氢气的体积与理论值相比偏大,则可能的原因是________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】结合下列实验装置回答相关问题:
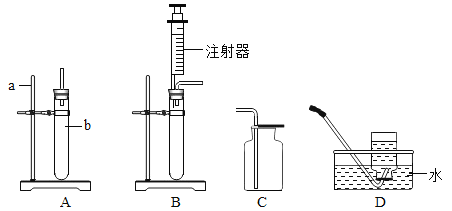
(1)写出A装置中a、b仪器的名称:a ___________b _______________。
(2)用石灰石与盐酸反应制CO2的化学方程式为_____________,收集装应选C____________(填编号)用双氧水制O2的化学方程式为___________________。
(3)若用B作制气装置,与A相比,其优点是_______________(写一点)
(4)用KClO3和MnO2制O2,若选用A作发生装置,则还要增加_____________(填仪器名称),并把A作如下改动: ________________。
(5)用排水法开始收集氧气的适宜时刻是__________________,用排水法收集氧气你是怎样确定集气瓶已收集满气体? _________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com