
【题目】请用化学方程式解释下列现象:
(1)可以服用小苏打治疗胃酸过多_____。
(2)铝制品不易锈蚀_____。
(3)铁桶不能盛放波尔多液_____。
(4)常用稀盐酸除铁锈_____。
(5)石灰浆粉刷墙壁,干燥后墙面变硬_____。
(6)氢气作为最理想的燃料_____。
【答案】NaHCO3+HCl=NaCl+H2O+CO2↑ 4Al+3O2=2Al2O3 Fe+CuSO4=FeSO4+Cu Fe2O3+6HCl═2FeCl3+3H2O Ca(OH)2+CO2═CaCO3↓+H2O 2H2+O2![]() 2H2O
2H2O
【解析】
首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可。
(1)小苏打与胃酸中的盐酸反应生成氯化钠、水和二氧化碳气体,反应的化学方程式为:NaHCO3+HCl=NaCl+H2O+CO2↑。故填:NaHCO3+HCl=NaCl+H2O+CO2↑
(2)铝制品不易锈蚀的原因是铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,反应的化学方程式为:4Al+3O2=2Al2O3。故填:4Al+3O2=2Al2O3
(3)铁的活动性比铜强,铁和硫酸铜反应会生成硫酸亚铁和铜,铁桶不能盛放波尔多液,反应的化学方程式为:Fe+CuSO4=FeSO4+Cu。故填:Fe+CuSO4=FeSO4+Cu
(4)铁锈的主要成分是氧化铁,与盐酸反应生成氯化铁和水,反应的化学方程式是:Fe2O3+6HCl═2FeCl3+3H2O。故填:Fe2O3+6HCl═2FeCl3+3H2O
(5)用石灰浆粉刷墙壁,干燥后墙面变硬,是因为氢氧化钙和空气中的二氧化碳反应生成了碳酸钙和水,反应的化学方程式是:Ca(OH)2+CO2═CaCO3↓+H2O。故填:Ca(OH)2+CO2═CaCO3↓+H2O
(6)氢气与氧气在点燃的条件下反应生成水,方程式为:2H2+O2![]() 2H2O;故填:2H2+O2
2H2O;故填:2H2+O2![]() 2H2O。
2H2O。


 百年学典课时学练测系列答案
百年学典课时学练测系列答案科目:初中化学 来源: 题型:
【题目】NSR 技术通过 BaO 和 Ba(NO3)2 的相互转化实现 NOx(氮氧化物)的储存和还原,能有效降低柴油发动机在空气过量条件下的 NOx 排放。其工作原理如图所示。下列说法不正确的是
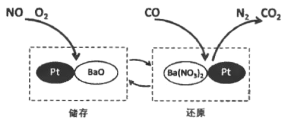
A. 降低 NOx 排放可以减少空气中酸雨的形成
B. 储存时,吸收 NOx (如 NO, NO2)的物质是 Pt
C. 还原时,发生的反应是: ![]()
D. 若有 28 g CO 参与反应,则生成 CO2 的质量为 44g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】K2SO4是无氯优质钾肥,Mn3O4是生产软磁铁氧体材料的主要原料。某研究性小组对K2SO4和Mn3O4的制备展开了系列研究。
(一)以硫酸工业的尾气SO2制备K2SO4的工艺流程如下:
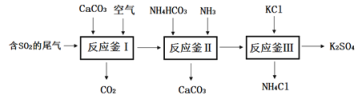
⑴钾肥K2SO4对农作物生长的作用是___________。
A.促进植物茎、叶生长,使叶色浓绿;
B.增强植物的抗寒、抗旱能力
C.增强植物的抗病虫害、抗倒伏能力
⑵反应釜I中发生的反应包括:①碳酸钙高温分解的化学方程式为________;
②CaO + SO2==CaSO3 ③ 2CaSO3+O2==2CaSO4
⑶反应釜III:向反应II 所得(NH4)2SO4溶液中加入KCl溶液充分反应后,经蒸发浓缩、过滤、洗涤、干燥等操作即可制得K2SO4产品。为提高K2SO4产品纯度,过滤时应控制反应液的温度范围为____________(填字母序号,如图为几种盐的溶解度曲线)。
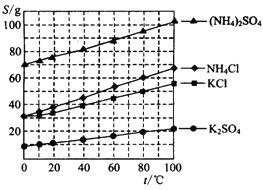
A.0℃-10℃ B. 20℃-30℃ C. 60℃-65℃ D. 80℃-90℃
⑷上述工艺流程中循环利用的物质是_______;证明产品K2SO4中不含杂质的实验方法是_______写出方法、现象)。
(二)实验室以SO2气体为原料制备少量高纯Mn3O4的操作步骤如下:
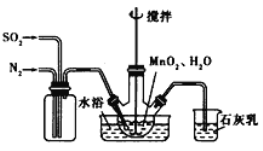
(步骤I)制备MnSO4溶液:在三颈烧瓶中(装置见图) 加入一定量MnO2和水,先通氮气,再通入SO2和N2混合气体,搅拌反应3小时。停止通SO2,继续反应片刻后过滤得MnSO4溶液。
[资料1]亚硫酸(H2SO3)在Mn2+催化作用下被O2氧化为硫酸,硫酸与MnO2在常温下不易发生反应。
⑸烧杯中石灰乳(有效成分为氢氧化钙)的作用为________。
⑹三颈烧瓶中生成MnSO4的反应化学方程式为____________。
⑺步骤I中,先通入氮气的目的是_________。为使SO2尽可能转化完全,在通入SO2和N2比例一定、不改变固液投料的条件下,可采取的合理措施有:及时搅拌反应液、_______(任写1条)。
(步骤II)制备MnSO4H2O晶体:利用硫酸锰的溶解度在100℃以上随温度升高而急剧降低的原理,采用压力釜升温加压结晶法后过滤、洗涤、低温干燥得纯净的MnSO4H2O晶体。
(步骤III)制备Mn3O4固体:准确称取101.4mg MnSO4H2O,将MnSO4H2O晶体在空气中高温煅烧,下图是用热重分析仪测定煅烧时温度与剩余固体质量变化曲线。
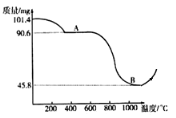
[资料2] MnSO4在空气中高温煅烧生成Mn3O4和三氧化硫,当温度超过1000℃时,Mn3O4又被氧气氧化为Mn2O3或MnO2
⑻该曲线中A段所表示物质的化学式为___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列四个图象中,能正确反映对应变化关系的是( )
|
|
|
|
A.向一定质量的氢氧化钠溶液中加入稀硫酸至过量 | B.向一定质量的稀硫酸中加入锌片 | C.常温下,足量的镁、铁分别同时放入少量等质量、等质量分数的稀盐酸中 | D.向一定质量的二氧化锰中加入过氧化氢溶液 |
A. AB. BC. CD. D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小王同学为了测定某Na2CO3溶液中溶质的质量分数,取10g该溶液于烧杯中,然后将400g澄清石灰水分四次加入,烧杯中沉淀的质量与每次加入澄清石灰水的质量关系如表。请计算:
第一次 | 第二次 | 第三次 | 第四次 | |
加入澄清石灰水的质量/g | 100 | 100 | 100 | 100 |
生成沉淀的质量/g | 0.4 | m | 1.0 | 1.0 |
(1)表中m的值为_____。
(2)Na2CO3溶液中溶质的质量分数_____(写出计算过程)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙、丁、M是初中化学常见的化合物,其中甲、乙、丙、丁分属酸、碱、盐、氧化物中不同类别的化合物,M与甲属于同种类别的化合物。甲是石灰石的主要成分,它们之间的部分转化关系如图所示(部分反应物、生成物、反应条件已略去,“一”表示物质之间能发生反应,“→”表示物质之间的转化关系)。
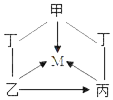
(1)甲的化学式为_____,M的化学式为_____;
(2)乙→丙的反应方程式为_____;
(3)甲→M的反应类型为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室用如图所示装置制取氧气,下列实验操作不正确的是
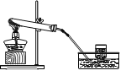
A. 加热前,先将集气瓶注满水用玻璃片盖好,再倒立在水槽中
B. 实验开始时,先将导管口伸入集气瓶,再开始加热
C. 收集O2后,先在水面下盖好玻璃片,再将集气瓶移出水槽
D. 实验结束时,先把导管移离水面,再熄灭酒精灯
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上用甲和乙反应制备燃料丙。根据微观示意图(如图)得出的结论中正确的是( )
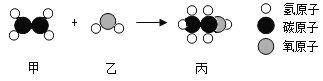
A. 丙中碳元素和氢元素的质量比为1:3
B. 丙充分燃烧生成一氧化碳和水
C. 甲、乙、丙都是有机物
D. 甲、乙、丙中的氢原子核内都是1个质子
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是一氧化碳还原氧化铁的装置,
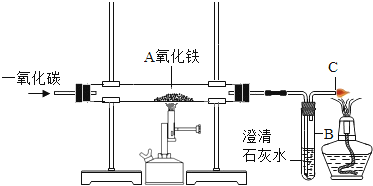
(1)该实验过程中A玻璃管内发生的现象是_____,反应的化学方程式_____。B试管中观察到的现象是_____,反应的化学方程式_____。
(2)酒精灯的作用是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com