
����Ŀ���ס������ֹ������ʵ��ܽ��������ͼ��ʾ���ش��������⣺
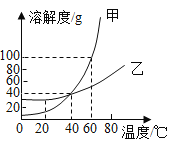
��1��20��ʱ���Ƚϼס��������ʵ��ܽ�ȣ���_____�ң��������=����������
��2��60��ʱ����100g�ļ����ʼ���50gˮ�У�����ܽ⣬�õ���Һ������Ϊ_____g��
��3��40��ʱ�������ʵı�����Һ�����ʵ���������Ϊ_____���������ȷ��0.1%��
��4����ҵ�Ͻ����ҵ��Ȼ����Һ�����߾��Ѵﱥ�ͣ���ȴ�����£��������壬���˺�õ���Һ���й���Һ��˵����ȷ����_____��
A ֻ�����ң������ף����Ҵﵽ����
B �����ң��ֺ��мף���ֻ���Ҵﵽ����
C �����ң��ֺ��мף������߶��ﵽ����
���𰸡��� 100 28.6% C
��������
��1�����ܽ������ͼ��֪��20��ʱ���Ƚϼס��������ʵ��ܽ�ȣ��ף��ҡ�
��2��60��ʱ�������ʵ��ܽ��Ϊ100g����100g�ļ����ʼ���50gˮ�У����ֻ���ܽ��50g����ף���õ���Һ������Ϊ50g+50g=100g��
��3��40��ʱ�������ʵ��ܽ��Ϊ40g���������ʵı�����Һ�����ʵ���������=![]() ��
��
��4�������ʵ��ܽ�����¶ȵ�Ӱ��ϴ������ʵ��ܽ�����¶ȵ�Ӱ���С�����º��������ʵ��ܽ�ȶ���С����ҵ�Ͻ����ҵ��Ȼ����Һ��ȴ�����£������������壬�Һ��������壬���˺�õ���Һ��Ϊ������Һ��
��ѡ��C��


 �����������һ��һ��ϵ�д�
�����������һ��һ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ˮʵ��ʱ������ˮ�м���ϡ��������ǿ�����ԣ������Ტδ�μӷ�Ӧ��
(1)С����ȡ40 mL������������Ϊ34%��������Һ(�ܶ�Ϊ1.25 g/mL)���������ʵ�����Ϊ________g��
(2)��(1)����ȡ��������Һ��ˮϡ�ͳ�5%��ϡ���ᣬӦ����ˮ������Ϊ__________g��
(3)ȡ90 g 5%��ϡ���������ˮʵ�飬ͨ��һ��ʱ����ռ�������������Ϊ2 g�����ʱ��Һ�����ʵ���������_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ס����������ʵ��ܽ��������ͼ��ʾ������˵����ȷ����

A�����ס��ҵı�����Һ��t2���ֱ��µ�t1�������������������һ�������� |
B��t1��ʱ�ס��ҵı�����Һ����������������� |
C��t2��ʱ��40g������100gˮ�У��γɱ�����Һ |
D����M��ļ���Һ��ɱ�����Һ����ȡ�ķ�����__________________________�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ȩ����ѧʽC5H8O2������Ϊ��ѧ�����������չʷ�ϵĵ�������̱����㷺Ӧ����ҽ����е������ë��ԡ����������Ҳ��Ԥ�����¹ڷ��ס�ɱ�������Ĺ��������˷dz�������á������й����ȩ��˵��������ǣ�������
A.���ȩ����Է�������Ϊ100
B.���ȩ��̼���⡢������Ԫ�����
C.�������ë�������ϴ�ɾ�����ʹ��
D.���ȩ�����к���5��̼ԭ�ӡ�8����ԭ�ӡ�2����ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ⶨCu��Zn�Ͻ�Cu��Ag�Ͻ���ͭ������������ʵ����ֻ�ṩһƿδ��������������ϡ����ͱ�Ҫ��������
��1������Ϊ�ܲ���Ͻ���ͭ��������������_____�Ͻ�
��2��ȡ�úϽ�ķ�ĩ32.5g����������ַ�Ӧ������ϡ���������ɵ�������ϵ��ͼ��ʾ��
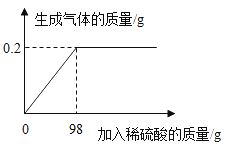
���������������Ϊ_____g��
�������úϽ���ͭ������������_____������д���ڢ��ʵ���ϸ�����̣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�ⶨһƿ����������Һ������������С��ͬѧ����������ʵ�飺
��ͼ1��ʾ�����ձ��м���5g����������Һ�����뼸�η�̪��Һ���õι���������1%��ϡ���ᣬ�����Ͻ��裬����Һ��ɫǡ�ñ�Ϊ��ɫΪֹ��
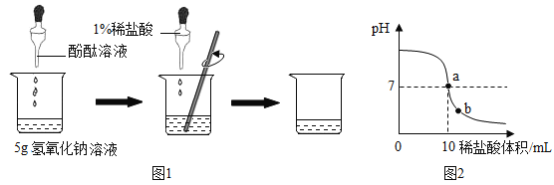
��ش�
��1������Һ��ɫǡ�ñ�Ϊ��ɫʱ������ȥϡ����7.3g���������������Һ�����ʵ���������Ϊ_____%��
��2��������ʵ������У�������μ�1%ϡ���ᣬ�����Ͻ��裬������ʵ���������ҺpH�ı仯������ͼ2��ʾ��
��a���ʾ�ĺ�����_____��
��b���ʾ����Һ�к��е���������_____�������ӷ��ţ���
��3��ʵ���õ��������ж�����;������д��һ��_____��
��4��������������������ܷ����кͷ�Ӧ����������ͼ�Ҳ�ܷ������Ʒ�Ӧ��д������ͼ��ʾ�Ļ�ѧ����ʽ��_____�����෴Ӧ��ʵ����_____��
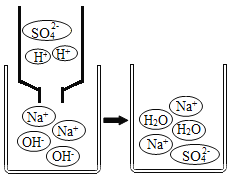
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һ�����ڣ��ϴ�ͬѧ�ͼ��˵�����ʡ�����ȥ�ιۣ����ֲ����������ͭ��Ʒ������һ����ɫ���ʡ���ɫ������ʲô�����������γɵģ���ѧ����ϣ�ͬѧ�����ʵ���������ɫ���ʽ���������̽�����
���������ϣ�
��ͭ�ڿ�����������ͭ�⣬��Ϊ��ɫ������Ҫ�ɷ���Cu2��OH��2CO3��
�ڰ�ɫ������ͭ��ĩ��ˮ�ܱ�Ϊ��ɫ��
̽���һ����֤ͭ�����ɡ�
������ʵ��1��
ͬѧ���������ͼ��ʾװ�ò�����ʵ�顣
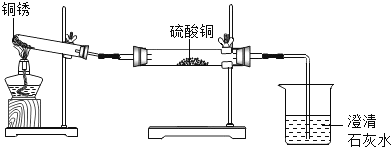
ʵ����� | ʵ������ | ʵ����� |
�ٰ���ͼ��װ������װ��ҩƷ�� �ڼ���ͭ�⣬ֱ�����������������ֹͣ���� | ��ɫ�����Ϊ��ɫ������ͭ��ĩ��Ϊ��ɫ���ձ���Һ������ | ����ͭ�����ɵ�������_____�� |
����ȴ�����Թ��й����������ϡ���ᣬ�Լ��� | ��ɫ�����ܽ⣬��Һ��Ϊ��ɫ | ������Ӧ�Ļ�ѧ����ʽΪ��_____�� |
̽�������̽��ͭ�����������
������ʵ��2��
ͬѧ�ǽ����������4��ʵ�飬ÿ��۲�һ������һ��ʱ�����ֻ��ʵ��4�е�ͭ˿�����ˣ�����ˮ�Ӵ��IJ�����������ԡ�
��� | ʵ��1 | ʵ��2 | ʵ��3 | ʵ��4 |
ʵ������ |
|
|
|
|
ʵ������ | �ڸ��ﻷ���У�ͭ������ | ͭ����������ˮ�Ӵ��������� | ͭ���������̼��ˮ�Ӵ��������� | ͭ���� |
span>
��ʵ����ۣ�ͭ�����������_____��
����˼����չ��
��1��ʵ��2��3��ʹ�õ��Ǿ���к�Ѹ����ȴ������ˮ����Ŀ����_____��
��2�����Ҫ��ȥͭ��Ʒ�����ͭ�⣬������ϡ������ݣ�д����Ӧ�Ļ�ѧ����ʽ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ʵ��װ��ͼ����Ҫ��ش��������⣺
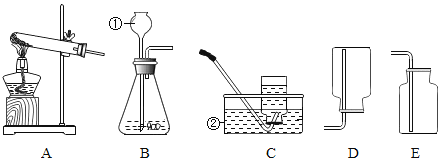
��1��д��������ŵ��������ƣ���_____����_____��
��2��ʵ������ȡCO2�Ļ�ѧ��Ӧ����ʽΪ_____����ȡ���ռ�������Ӧѡ���װ����_____������ţ�������������ˮ����_____��������Ʒ�Ӧ���ʣ����Խ���������_____���档
��3�����ѡ������ȡCO2��ͬ�ķ���װ������ȡO2��������Ӧ�Ļ�ѧ����ʽΪ_____��
��4������Aװ����Ϊ��������������ķ���װ�ã���һ����֮����Ӧ��_____��ԭ����_____���÷�Ӧ�Ļ�ѧ����ʽΪ_____���Ľ�����ȡ��������Ҫʵ�鲽���У��ټ��ȣ������Թ���װҩƷ���̶����ۼ��װ�������ԣ�������ˮ���ռ���������ֹͣ���ȣ������ܴ�ˮ����ȡ������ȷ��ʵ�����˳����_____��������ţ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���NaOH��Ca(OH)2���ܽ�����ݣ���ش��������⣮
�¶ȣ��棩 | 0 | 20 | 40 | 60 | 80 | 100 | |
�ܽ�ȣ�g�� | NaOH | 31 | 91 | 111 | 129 | 313 | 336 |
Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
��1���ӱ������ݿ��Ի�õ���Ϣ��__________��дһ������
��2����80��ʱNaOH�ı�����Һ������20�棬���Կ�����������__________����ʱ��Һ��������������Ϊ__________��������һλС����
��3��ij��ȤС��Բ��ֱ��ʵ��������ƹ�������ᴿ����������²������̣���ش�

��������м������Ca(OH)2��Ŀ����__________���漰��Ӧ�Ļ�ѧ����ʽΪ__________��
������ҺB�е�������__________��д��ѧʽ����������������ľ�������Ǽ���Ũ����__________�����ˣ�
������ʵ��ǰ�Ƶ���Ʒ������Ϊ10g��ʵ���Ƶ�������A������NaOH�������������ֱ���5g��8.7g�������Ʒ�Ĵ���Ϊ__________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com