
【题目】晶体硅是一种重要的非金属材料。制备纯硅的主要步骤如下:
①高温下用碳还原二氧化硅制得粗硅,同时得到一种可燃性气体。
②粗硅与干燥HCl气体反应制得SiHCl3:Si+3HCl![]() SiHCl3+H2
SiHCl3+H2
③SiHCl3与过量H2在1000~1100℃反应制得纯硅。
已知SiHCl3能与H2O强烈反应,在空气中易自燃。
请回答下列问题:
(1)第①步制备粗硅的化学反应方程式为_____。
(2)粗硅与HCl反应完全后,经冷凝得到的SiHCl3(沸点33.0℃)中含有少量SiCl4(沸点57.6℃)和HCl(沸点-84.7℃),提纯SiHCl3采用的方法为:_____。
(3)用SiHCl3与过量H2反应制备纯硅的装置如下(热源及夹持装置略去):
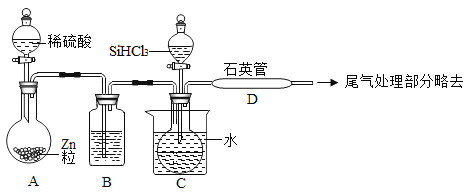
①装置B中的试剂是_____,装置C中的烧瓶需要加热,其目的是:_____。
②装置D不能采用普通玻璃管的原因是_____,装置D中发生反应的化学方程式为_____。
③为保证制备纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反应温度以及_____。
【答案】SiO2+2C![]() Si+2CO↑ 分馏(或蒸馏) 浓硫酸 使滴入烧瓶中的SiHCl3气化 在该反应温度下,普通玻璃会软化 SiHCl3+H2
Si+2CO↑ 分馏(或蒸馏) 浓硫酸 使滴入烧瓶中的SiHCl3气化 在该反应温度下,普通玻璃会软化 SiHCl3+H2![]() Si+3HCl 排尽装置中的空气
Si+3HCl 排尽装置中的空气
【解析】
高温下用碳还原二氧化硅制得粗硅和一氧化碳,锌和稀硫酸反应生成硫酸锌和氢气。
(1)高温下用碳还原二氧化硅制得粗硅和一氧化碳,第①步制备粗硅的化学反应是方程式为SiO2+2C![]() Si+2CO↑。
Si+2CO↑。
(2)粗硅与HCl反应完全后,经冷凝得到的SiHCl3(沸点33.0℃)中含有少量SiCl4(沸点57.6℃)和HCl(沸点-84.7℃),提纯SiHCl3采用的方法为:分馏(或蒸馏)。
(3)锌和稀硫酸反应生成硫酸锌和氢气,装置B是干燥氢气,故①装置B中的试剂是浓硫酸,装置C中的烧瓶需要加热,其目的是使滴入烧瓶中的SiHCl3气化。
②反应的温度为1000~1100℃,故装置D不能采用普通玻璃管的原因是在该反应温度下,普通玻璃会软化,装置D中发生反应为SiHCl3和氢气在高温下生成硅和氯化氢,反应的化学方程式为
SiHCl3+H2![]() Si+3HCl。
Si+3HCl。
③为保证制备纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反应温度以及排尽装置中的空气。


科目:初中化学 来源: 题型:
【题目】水是生命之源,“珍惜水、节约水、保护水”是每个公民的义务和责任
![]() 下列“水”属于纯净物的是______
下列“水”属于纯净物的是______![]() 填序号
填序号![]() .
.
A、蒸馏水 B、河水 C、自来水
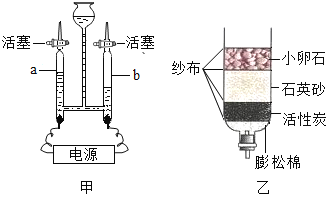
![]() 用如图甲装置进行电解水的实验,b中收集到的气体是______,该实验说明水是由______组成的.
用如图甲装置进行电解水的实验,b中收集到的气体是______,该实验说明水是由______组成的.
![]() 我国水资源丰富,但分布不均,有些村民地下水作为生活用水,人们常用______检验地下水是硬水还是软水,生活中可用______的方法降低水的硬度;某同学自制如图乙所示简易净水器,图中活性炭的主要作用是______
我国水资源丰富,但分布不均,有些村民地下水作为生活用水,人们常用______检验地下水是硬水还是软水,生活中可用______的方法降低水的硬度;某同学自制如图乙所示简易净水器,图中活性炭的主要作用是______
![]() 请举一例生活中节约用水的具体措施______.
请举一例生活中节约用水的具体措施______.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】业上生产电路板及处理废液的工艺流程如下:
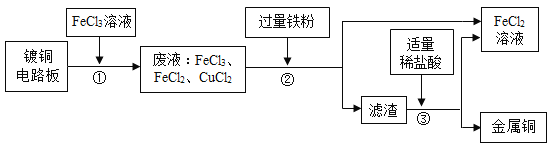
(1)由步骤①可判断FeCl3与铜反应生成的两种产物是________和________。
(2)步骤②加入过量的铁粉,除能与废液中CuCl2反应外,还可发生反应的化学方程式为_______。该反应的基本类型是:_______反应。
(3)步骤③加入稀盐酸,充分搅拌,当观察到_______________现象时,说明滤渣只剩铜。
(4)步骤②③所得FeCl2可与一种单质发生化合反应生成FeCl3,实现循环使用。根据质量守恒定律可推测该单质的化学式为Cl2,已知Cl2与H2O反应的化学方程式为:Cl2+H2O =HCl +HClO,则Cl2与氢氧化钙溶液反应的化学方程式为:__________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列有关实验原理或实验操作正确的是( )

A.用水润湿的pH试纸测量某溶液的pH,测量结果一定偏大或偏小
B.用量筒量取10 mL98%的浓硫酸溶液(密度1.84g/mL)于烧杯中,加水162 mL,配制成10%的稀H2SO4溶液
C.实验室用图1所示装置制取少量氨气
D.实验室用图2所示装置除去Cl2中的少量HCl
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人类的生活和生产都离不开金属,铁是世界产量最高且应用最广泛的金属。
(1)生活中用铁锅作炊具,是利用了铁的____性;
(2)铁制品生锈的主要条件是铁与____直接接触,铁锈的主要成分是____(填化学式);防止铁生锈的方法有____(答一种即可)。
(3)Pb的化合价有+2和+4价,Pb3O4属氧化物,也属于盐,其盐的化学式可表示为Pb2(PbO4),铁的氧化物Fe3O4也属于盐,则其盐的化学式可表示为____;
(4)取某钢样粉末50.0 g(假设只含Fe和C),在氧气流中充分反应,将产生的气体通入足量的澄清石灰水中,得到2.5 g白色沉淀。另取三份不同质量的该钢样粉末分别加入到100.0 g质量分数相同的稀H2SO4中,充分反应后,测得的实验数据如下表所示:
实验序号 | 甲 | 乙 | 丙 |
加入钢样粉末的质量(g) | 10.0 | 20.0 | 40.0 |
生成气体的质量(g) | 0.355 | 0.71 | 1.0 |
①根据表中数据可计算出稀硫酸中H2SO4的质量分数为____;
②若要使实验甲中的剩余硫酸全部消耗完,则至少需要再加入____g钢样粉末。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列说法正确的是
A. 等质量的镁与氧化镁混合,其混合物中镁、氧两种元素的质量比为![]()
B. 等质量的![]() 和
和![]() 分别与足量稀硫酸充分反应,生成
分别与足量稀硫酸充分反应,生成![]() 的质量相等
的质量相等
C. 质量和质量分数均相等的氢氧化钡溶液和稀硝酸,充分反应后,向所得溶液中滴加硫酸铜溶液,会出现蓝色沉淀
D. 将一定量的氢氧化钠和氢氧化钙的混合物溶于足量水中,再向溶液中加入过量的碳酸钠溶液,充分反应后,生成的沉淀质量与原混合物的质量相等,则原混合物中氢氧化钠的质量分数为![]()
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图像能正确反映其对应关系的是

A. ①表示向NaOH溶液中不断加水稀释
B. ②表示水电解生成氢气与氧气的质量关系
C. ③表示用等质量、等质量分数的过氧化氢溶液制取氧气
D. ④表示分别向等质量、等质量分数的稀硫酸中加入足量的镁、铝
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是生命之源
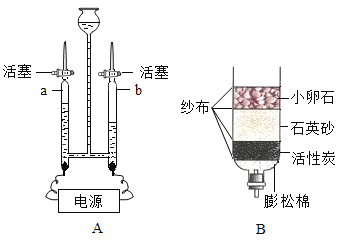
(1)用如图A装置进行电解水的实验,a、b两管中都收集到气体,体积比为_____,b中的气体是_____,与a管相连的电源是_____极,检验a管中气体的操作是_____,写出电解水反应的符号表达式_____。
(2)图B所示是净化水的简易装置,其中能起到吸附作用的是_____,小卵石和砂子起到_____作用。
(3)有些村庄打深井取用地下水。检验地下水是硬水还是软水,可用的物质是_____。如果地下水硬度大,或者坑水中病原微生物过多,生活中都可以采取_____的方法,来降低硬度和杀灭病原微生物。
(4)身处旱区的我们如何做到节约用水?_____(举一做法)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com