
【题目】阅读下面科普短文
新冠肺炎疫情防控,口罩成了每家必不可少的“保护神”。口罩通常由三层构成,图1为某种口罩的层状结构及对外在物质的阻隔效果:
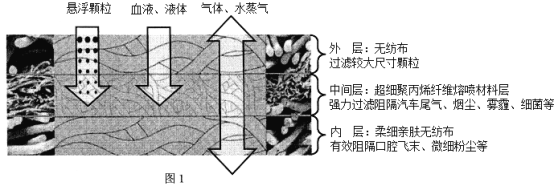
由于口罩的材质缝隙小于病毒体积,对病毒起到一定的防护作用。口罩本身的静电作用还可将部分病毒吸附在其外层。
聚丙烯纤维是以丙烯聚合得到的聚丙烯为原料纺制而成的合成纤维。丙烯常温下为无色、稍带有甜味气体,易燃。不溶于水,溶于有机溶剂。
口罩生产出来以后,采用环氧乙烷(C2H4O)灭菌。环氧乙烷是一种有机化合物,是一种有毒的致癌物质。
依据文章内容回答下列问题。
(1)利用口罩材质缝隙,起到防护作用的原理与__________的原理相似,该过程属于_______变化(填“物理”或“化学”)。
(2)丙烯完全燃烧生成二氧化碳和水,其微观示意图如下所示:
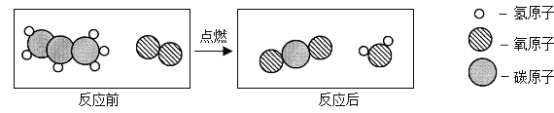
①丙烯分子中碳、氢原子的个数比为__________。
②反应物的分子个数比为__________。
(3)下列关于口罩的说法中,正确的是__________。
A、口罩可以有效阻止含有细菌、病毒的悬浮颗粒、飞沫进入人体
B、雾霾天戴口罩,可以有效防止部分有害气体以及可吸入颗粒物进入人体
C、口罩灭菌后,要使环氧乙烷残留药品释放,达到安全标准
【答案】过滤 物理 1:2 2:9(或9:2) ABC
【解析】
(1)由于口罩的材质缝隙小于病毒体积,对病毒起到一定的防护作用。起到防护作用的原理与过滤的原理相似,属于物理变化;
(2)① 从微观示意图知道一个丙烯分子中有3个碳原子和6个氢原子构成,所以碳、氢原子的个数比为3:6=1:2;
②根据微观示意图反应的化学方程式为: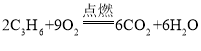 ,反应物的分子个数比为2:9(或9:2)。
,反应物的分子个数比为2:9(或9:2)。
(3)A、根据图1,口罩可以有效阻止含有细菌、病毒的悬浮颗粒、飞沫进入人体,符合题意;
B、根据图1,雾霾天戴口罩,可以有效防止部分有害气体以及可吸入颗粒物进入人体,符合题意;
C、口罩灭菌后,要使环氧乙烷残留药品释放,达到安全标准,因为环氧乙烷是一种有机化合物,是一种有毒的致癌物质,符合题意。故选ABC。


科目:初中化学 来源: 题型:
【题目】下图是教材中有关《质量守恒定律》的实验,试回答下列问题:
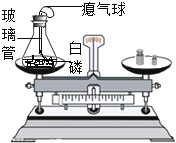
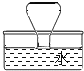
(1)反应中锥形瓶内观察到的现象是______;
(2)左盘锥形瓶口在白磷点燃后要塞紧瓶塞,原因是______;
(3)在实验设计上,玻璃管上方系一瘪气球的目的是______;
(4)实验结束后(锥形瓶已冷却到室温),发现瓶中白磷过量,为了防止白磷在空气中燃烧,将锥形瓶瓶口倒置于盛满水的水槽中(如图,瓶口贴紧水面),拔下瓶塞,发现水进入锥形瓶中,则进入瓶中的水占锥形瓶的容积的1/5,原因是:______.
某化学课外小组同学,用如图所示实验验证质量守恒定律。
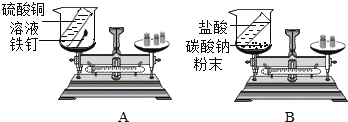
(5)某甲同学用A装置探究质量守恒定律,实验步骤如下:如图将烧杯放在天平上用砝码平衡,然后倾斜烧杯使硫酸铜溶液与铁钉接触,一段时间后,再把烧杯放在天平上。
①烧杯内反应的实验现象为___
②最后天平的指针(填序号)___(a 偏左b 偏右c 不偏转d 无法预测).
(6)①乙同学用B装置研究质量守恒定律,实验步骤如下:
将烧杯放在天平上用砝码平衡,然后倾斜烧杯使盐酸与碳酸钠粉末接触,写出反应的化学方程式___;一段时间后再把烧杯放在天平上,发现天平的指针偏右,该反应___(填符合或不符合)质量守恒定律。
②若在验证质量守恒定律时,若利用有气体参加或有气体生成的化学反应来设计实验,在装置设计方面应做到___.
③从微观角度解释化学反应都符合质量守恒定律___.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某兴趣小组对石灰石样品进行如下实验取 12g 样品放入烧杯中,将 100g 稀盐酸分 4 次加入到烧杯中,充分反应后(杂质不溶于水,也不与酸反应),测得剩余固体的质量记录如下。请计算:
次数 | 1 | 2 | 3 | 4 |
加入稀盐酸的质量/g | 25 | 25 | 25 | 25 |
剩余固体的质量/g | 8 | 4 | 2 | 2 |
求:第 4 次加入稀盐酸后所得溶液中 CaCl2的质量分数。(写出计算过程,最终结果保留 0.1%)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】生命的孕育和维系需要水,人类的日常生活和工农业生产也离不开水。
(1)下列有关“水”的说法正确的是_____(填字母)。
A 经常饮用蒸馏水对身体有益
B 用洗完衣服的水冲马桶
C 家中尽量使用节水龙头
D 淡水是取之不尽、用之不竭的
(2)简易净水器中活性炭的作用是_____,生活中常用_____检验水的硬度。
(3)电解水时,正极和负极产生气体的体积比约为_____。
(4)如图是甲、乙两种物质的溶解度曲线。请根据图像信息回答:
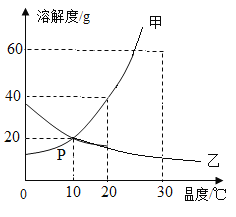
②P点表示的含义_____。
②30 °C时,把35 g甲物质加入到50 g水中,充分搅拌,溶解,所得溶液的质量为_____。
③将乙的不饱和溶液转化为饱和溶液的方法是_____。
④将30°C时的甲、乙两物质的饱和溶液降温到10°C,所得溶液的溶质质量分数为甲_____乙(填“>”、“<”或“=”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】无水硫酸铜(CuSO4)是一种白色固体,吸水后可变成蓝色晶体。某气体由H2、CO2、CO、HCl中的一种或几种组成。为探究该气体组成,某化学兴趣小组的同学把该气体依次通过如图所示的试剂(试剂均足量)。观察到的实验现象为:I中澄清石灰水没有变浑浊,Ⅳ中黑色固体变红,V中白色固体变蓝,Ⅵ中澄清石灰水变浑浊。

关于该气体的组成,下列说法正确的是( )
①I中澄清石灰水没有变浑浊,说明原气体中一定不含CO2
②气体通过Ⅱ后,溶液中一定有氯化钠
③Ⅳ中的黑色固体变红,说明原气体中一定含有CO和H2
④V中白色固体变蓝,说明原气体中一定含有H2
⑤原气体中可能含有CO2、HCl
A.①④B.②③C.③④D.④⑤
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请从1或2两题中任选1个作答。
O2的实验室制取与性质 | CO2的实验室制取与性质 |
(1)A中加热高锰酸钾,发生反应的化学方程式为___________。 (2)B中可观察到的现象是__________。 |
(1)A中向大理石中加入稀盐酸,发生反应的化学方程式为__________。 (2)B中可观察到的现象是__________。 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用化学用语填空:
(1)氦气________
(2)两个铵根离子_________
(3)相对分子质量最小的氧化物___________
(4)标出氢氧化镁中镁元素的化合价________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国某科研团队以软锰矿(主要成分是MnO2,含有SiO2、Fe2O3等少量杂质)为主要原料,制取高纯碳酸锰,工艺流程如下图:
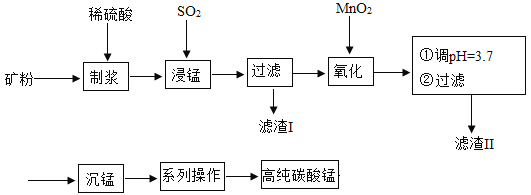
已知:①SiO2不溶于水,不与稀H2SO4、SO2反应;②MnO2能将Fe2+氧化成Fe3+;③溶液中的Fe3+在 pH 大于或等于 3.2 时将完全转化为Fe(OH)3沉淀。
请回答:(1)滤渣Ⅰ、Ⅱ分别为_____、_____(写化学式) ;
(2)浸锰过程中发生了 2 个化学反应,其中一个为Fe2O3与SO2反应,该反应的化学方 程式为Fe2O3+ SO2+H2SO4=2FeSO4+ H2O,另一个为MnO2和SO2按化学计量数为 1:1 发生化合反应,请写出该反应的化学方程式:_____, 该反应中共有_____种元素的化合价发生了改变。
(3)“沉锰”:加入NH4HCO3溶液后,生成了 4 种产物,其中含有MnCO3沉淀和某种气 体,写出该反应的化学方程式:_____。
(4)取所得的高纯MnCO311.7g溶于足量的盐酸中,将产生的气体用足量的Ba(OH)2浓 溶液吸收,得到白色沉淀 19.7g,则所得产品的纯度为_____%(保留一位小数)
(5)某研究小组用稀H2SO4与菱锰矿(含有MnCO3)反应来浸出Mn2+,该研究小组选 定两个因素作为研究条件进行对比实验,数据如下:
矿酸比 | 温度/(℃) | 浸出率/(%) | |
1 | 1:0.5 | 60 | 80.2 |
2 | 1:0.5 | 80 | 83.8 |
3 | 1:0.6 | 60 | X |
4 | 1:0.6 | 80 | 91.8 |
表中 X 最有可能的数值为_____。
a.79.7 b.80.8 c.87.6 d.92.8
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将一定量的锌粉加入到硝酸铝、硝酸铜、硝酸银的混合溶液中。充分反应后过滤。则所得溶液的质量与原混合溶液的质量相等。
(1)滤渣中一定含有:____。
(2)写出可能发生的一个化学方程式___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com