
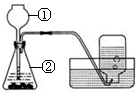
 右图是实验室用过氧化氢和二氧化锰制取氧气的装置.
右图是实验室用过氧化氢和二氧化锰制取氧气的装置.
| ||
| ||
| ||
| ||


 备战中考寒假系列答案
备战中考寒假系列答案科目:初中化学 来源: 题型:阅读理解
 (2012?江宁区一模)过氧化钙(CaO2)广泛应用于水产养殖、污水处理等领域,是优良的供养剂.
(2012?江宁区一模)过氧化钙(CaO2)广泛应用于水产养殖、污水处理等领域,是优良的供养剂.| 120℃ |
| 120℃ |
| 9m-n |
| 2w |
查看答案和解析>>
科目:初中化学 来源:2011-2012学年江苏省南京市江宁区中考一模化学试卷(解析版) 题型:计算题
过氧化钙(CaO2)广泛应用于水产养殖、污水处理等领域,是优良的供养剂。
制备CaO2:工业制备过氧化钙的一种方法是氢氧化钙法。
(1)Ca(OH)2和H2O2在有水存在的条件下生成CaO2·8H2O,它在120℃时完全分解为CaO2等。有关化学反应方程式为: , 。
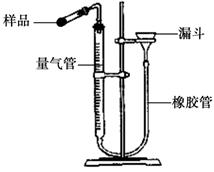
测定CaO2纯度:CaO2在350℃时能迅速分解,生成CaO和O2。右图是实验室测定产品中CaO2含量的装置。
(2)检查装置气密性的方法是:连接好装置,从漏斗注水,量气管两边形成高度差,做好标记,一段时间后,高度差 ,说明气密性良好。
(3)正确读取量气管内液面的初始、最终读数前都需进行的操作是 。
(4)加热小试管时,随着过氧化钙分解,量气管内的 液面逐渐下降,为防止试管和量气管内气体压强过大,可将漏斗 (填“上提”或“下移”)。
(5)计算含量需要测定的数据有 。(填字母序号)
A. 氧气的体积 B. 样品的质量 C. 反应的时间
(6)若样品质量为0.20 g,反应前量气管读数为2.10 mL,反应后量气管读数为24.50 mL(常温下氧气的密度为1.429g/L)。实验中量气管的最佳规格是 。(填字母序号)
A.50 mL B.100 mL C.1 L
(7)样品中CaO2含量为 。
(8)若样品质量用w表示,反应前称量药品和小试管总质量为m g,反应后在空气中冷却,称量药品和小试管总质量为n g,则CaO2含量=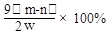 。此方案测定结果偏小的原因可能是 。
。此方案测定结果偏小的原因可能是 。
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
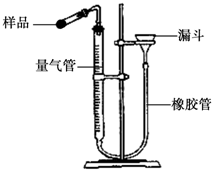 过氧化钙(CaO2)广泛应用于水产养殖、污水处理等领域,是优良的供养剂.
过氧化钙(CaO2)广泛应用于水产养殖、污水处理等领域,是优良的供养剂.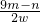 ×100%.此方案测定结果偏小的原因可能是________.
×100%.此方案测定结果偏小的原因可能是________.查看答案和解析>>
科目:初中化学 来源: 题型:
过氧化钙(CaO2)广泛应用于水产养殖、污水处理等领域,是优良的供养剂。
【制备CaO2】工业制备过氧化钙的一种![]() 方法是氢氧化钙法。
方法是氢氧化钙法。
(1)Ca(OH)2和H2O2在有水存在的条件下生成Ca![]() O2·8H2O,它在120℃时完全分解为CaO2等。有关化学反应方程式为: , 。
O2·8H2O,它在120℃时完全分解为CaO2等。有关化学反应方程式为: , 。
【测定CaO2纯度】CaO2在350℃时能迅速分解,生成CaO和O2。右图是实验室测定产品中CaO2含量的装置。
(2)检查装置![]() 气密性的方法是:连接好装置,从漏斗注水,量气管两边形成高度差,做好标记,一段时间后,高度差 ,说明气密性良好。
气密性的方法是:连接好装置,从漏斗注水,量气管两边形成高度差,做好标记,一段时间后,高度差 ,说明气密性良好。
(3)正确读取量气管内液面的初始、最终读数前都![]() 需进行的操作是 。
需进行的操作是 。
(4)加热小试管时,随着过氧化钙分解,量气管内的 液面逐渐下降,为防止试管和量气管内气体压强 过大,可将漏斗 (填“上提”或“下移”)。
(5)计算含量需要测定的数据有 。(填字母序号)
A. 氧气的体积 B. 样品的质量 C. 反应的时间
(6)若样品质量为0.20 g,反应前量气管读数为2.10 mL,反应后量气管读数为24.50 mL(常温下氧气的密度为1.429g/L)。实验中量气管的最佳规格是 。(填字母序号)
A.50 mL B.100 mL C.1 L
(7)样品中CaO2含量为 。
(8)若样品质量用w表示,反应前称量药品和小试管总质量为m g,反应后在空气中冷却,称量药品和小试管总质量为n g,则CaO2含量=![]() 。此方案测定结果偏小的原因可能是 。
。此方案测定结果偏小的原因可能是 。

查看答案和解析>>
科目:初中化学 来源: 题型:
过氧化钙(CaO2)广泛应用于水产养殖、污水处理等领域,是优良的供养剂。
制备CaO2:工业制备过氧化钙的一种方法是氢氧化钙法。
(1)Ca(OH)2和H2O2在有水存在的条件下生成CaO2·8H2O,它在120℃时完全分解为CaO2等。有关化学反应方程式为: , 。
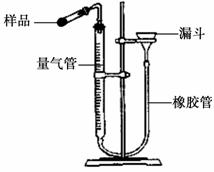 测定CaO2纯度:CaO2在350℃时能迅速分解,生成CaO和O2。右图是实验室测定产品中CaO2含量的装置。
测定CaO2纯度:CaO2在350℃时能迅速分解,生成CaO和O2。右图是实验室测定产品中CaO2含量的装置。
(2)检查装置气密性的方法是:连接好装置,从漏斗
注水,量气管两边形成高度差,做好标记,一段
时间后,高度差 ,说明气密性良好。
(3)正确读取量气管内液面的初始、最终读数前都需
进行的操作是 。
(4)加热小试管时,随着过氧化钙分解,量气管内的
液面逐渐下降,为防止试管和量气管内气体压强
过大,可将漏斗 (填“上提”或“下移”)。
(5)计算含量需要测定的数据有 。(填字母序号)
A. 氧气的体积 B. 样品的质量 C. 反应的时间
(6)若样品质量为0.20 g,反应前量气管读数为2.10 mL,反应后量气管读数为24.50 mL(常温下氧气的密度为1.429g/L)。实验中量气管的最佳规格是 。(填字母序号)
A.50 mL B.100 mL C.1 L
(7)样品中CaO2含量为 。
(8)若样品质量用w表示,反应前称量药品和小试管总质量为m g,反应后在空气中冷却,称量药品和小试管总质量为n g,则CaO2含量= 。此方案测定结果偏小的原因可能是 。
。此方案测定结果偏小的原因可能是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com