
【题目】化学兴趣小组为测定某石灰石样品中碳酸钙的质量分数,取26g石灰石样品放在烧杯中,然后向其中逐渐加入稀盐酸,使之与样品充分反应,恰好完全反应(杂质不参加反应)时,加入稀盐酸的质量为90g,反应后烧杯中物质的总质量为105g.请计算:
(1)反应生成二氧化碳的质量为 g.
(2)样品中碳酸钙的质量分数.(结果保留到0.1%)
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:初中化学 来源: 题型:
【题目】红枣醋饮中含有一种酸(C4H6O5),具有美容养颜,解酒护肝健胃的重要用途。下列关于红枣醋饮说法中正确的是
A.该酸由15个原子构成 B.该酸的相对分子质量为134
C.该酸中氢元素的质量分数最大 D.胃酸过多病人养胃首选饮料
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了探究酸碱中和反应是否放热,某同学设计了如图所示的实验装置(夹持等固定装置图略),针对该实验目的,下列评价或改进,错误的是

A.若观察到红墨水向右移,则说明该实验一定有放热现象
B.为了使实验现象更明显,可改用氢氧化钠固体
C.在打开活塞a之前应先打开橡皮管上的止水夹
D.为了使实验更具有说服力,可用氢氧化钾溶液再次实验
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碳化硅(SiC)俗称金刚砂。在空气中,碳化硅能与熔融的氢氧化钠发生如下反应:
SiC + 2NaOH + 2O2 ==== Na2SiO3 + X + H2O。请推断X的化学式
A.CO2 B.CO C.SiO2 D.Na2CO3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】多角度认识物质,能帮助我们更全面了解物质世界。以氧气和二氧化碳为例,回答下列问题:
(1)认识物质的组成和构成
①从宏观上看,氧气和二氧化碳都由 (选填“元素”、“原子”或“分子”)组成。
②从微观上看,氧气和二氧化碳都由 (选填“元素”、“原子”或“分子”)构成。
(2)认识物质的性质
①氧气的化学性质比较活泼。纳米铁粉在氧气中可自燃生成氧化铁,反应的化学方程式为 。

②将蘸有酒精的棉芯点燃后放入烧杯中,向烧杯中缓缓倾倒二氧化碳,观察到烧杯中的棉芯自下而上熄灭(如右图)。说明二氧化碳具有的性质有 ,由此可推知的灭火原理是 。若要使棉芯下半段恢复燃烧,最简单的操作方法是 。

(3)认识物质的制法
①某同学用软塑料瓶自制气体发生装置,通过捏放瓶身可随时控制反应发生和停止(如右图)。若利用该装置制氧气,反应的化学方程式为 。若利用该装置制二氧化碳,通常不选用大理石和稀硫酸作为反应物,理由是 。
②工业上常用液化空气制氧气,该过程发生 (选填“物理变化”或“化学变化”)。
(4)辩证地认识物质
①量变引起质变。例如:碳在充足氧气中燃烧生成二氧化碳,在不充足的氧气中燃烧生成 (填化学式)。②功过相对论。从“二氧化碳导致温室效应”的事实分析,“过”:使全球气候变暖导致海平面上升等;“功”: (举一例)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业铁红的主要成分是Fe2O3,还含有少量的FeO、Fe3O4.为了测定铁红中铁的质量分数,兴趣小组的同学进行了如下实验,请你参与过程分析.
资料1:草酸晶体(H2C2O43H2O)在浓H2SO4作用下受热分解,化学方程式为:
H2C2O43H2O![]() CO2↑+CO↑+4H2O
CO2↑+CO↑+4H2O
资料2:浓硫酸具有吸水性;氢氧化钠溶液能吸收二氧化碳;碱石灰固体既能吸水又能吸收二氧化碳;CO能将FeO、Fe2O3、Fe3O4还原成铁.
(1)下列可用作草酸分解制取气体的装置是 (填字母编号).
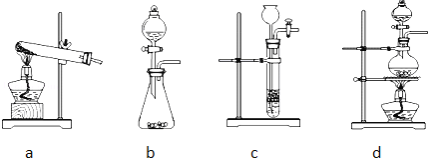
问题讨论:用如图所示装置进行实验:
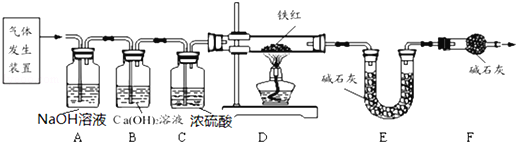
(2)实验前应先 .
(3)B装置的作用是 .
(4)对D装置加热前和停止加热后,都要通入过量的CO,其中加热前作用是:
(5)写出D装置中所发生反应的一个化学方程式
数据分析:资料3:铁的常见氧化物中铁的质量分数:
铁的氧化物FeO Fe2O3 Fe3O4 铁的质量分数77.8% 70.0% 72.4%
(6)称取铁红样品10.0g,用上述装置进行实验,测定铁红中铁的质量分数.
①D中充分反应后得到Fe粉的质量为m g,则 .
②实验前后称得E装置增重6.6g,则此铁红中铁的质量分数是 .
实验评价:反思1:本实验中如果缺少C装置(不考虑其它因素),则测得样品中铁的质量分数会 (填“偏小”、“不变”或“偏大”).
反思2:请指出 问题讨论中实验装置的一个明显缺陷 .
拓展探究:用100t含氧化铁80%的赤铁矿石理论上可冶炼出含铁98%的生铁多少吨?(结果保留1为小数)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com