
 使用红磷燃烧的方法测定空气中氧气的含量
使用红磷燃烧的方法测定空气中氧气的含量分析 (1)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
(2)根据红磷与氧气反应生成固体五氧化二磷,瓶内氧气消耗,压强降低,在外界大气压的作用下,水进入集气瓶进行解答.
(3)根据实验的注意事项进行解答.
解答 解:(1)红磷在空气中燃烧生成五氧化二磷,反应的化学方程式为:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.故填:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
(2)红磷与氧气反应生成固体五氧化二磷,瓶内氧气消耗,压强降低,在外界大气压的作用下,水进入集气瓶,所以待红磷熄灭并冷却后,打开弹簧夹,观察到烧杯中的水进入集气瓶,瓶内水面最终上升约至1刻度处.由此可知氧气约占空气总体积的五分之一;故填:$\frac{1}{5}$;
(3)实验后发现测定空气中氧气含量偏低,造成这种结果的可能原因是红磷的量不足或没有冷却到室温就打开弹簧夹.故填:红磷的量不足或没有冷却到室温就打开弹簧夹.
点评 本题主要考查用红磷测定空气组成的实验原理、操作、现象、结论和注意事项,难度稍大.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| A. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | B. | Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | ||
| C. | HCl+NaOH═NaCl+H2O | D. | Cu+2AgNO3═2Ag+Cu(NO3)2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 纤维素是由C、H、O三种元素组成的 | |
| B. | 棉线与羊毛线可用燃烧的方法区别 | |
| C. | 纤维素中C、H、O三种元素的原子个数比为6:10:5 | |
| D. | 纤维素中C、H、O三种元素的质量比为12:1:16 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 馒头或面条 | B. | 酸牛奶 | C. | 蔬菜、水果 | D. | 鸡蛋. |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 钢锭难被压缩,因为铁原子间没有间隙 | |
| B. | 二氧化碳在空气中的含量增多会引起温室效应,属于空气污染物 | |
| C. | 液化气加压后贮存在钢瓶中,因为气体分子体积很小 | |
| D. | 温度计里的汞柱下降,因为原子间隔随温度的降低而变小 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
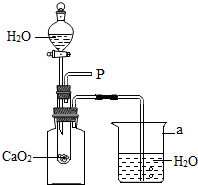 小强在回家的途中经过一鱼塘边时,发现养鱼师傅向鱼塘中撒一种微黄色的固体,鱼塘中顿时产生大量气泡,经咨询得知,这种固体的主要成分是过氧化钙(CaO2),请你与小强共同探究.
小强在回家的途中经过一鱼塘边时,发现养鱼师傅向鱼塘中撒一种微黄色的固体,鱼塘中顿时产生大量气泡,经咨询得知,这种固体的主要成分是过氧化钙(CaO2),请你与小强共同探究.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com