
| 反应前 | 反应后 | |
| 大理石样品 | 足量稀盐酸 | 称得滤液的质量 |
| 12.5g | 100.0g | 105.6g |
分析 碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,根据质量守恒定律,采用差量法根据反应的化学方程式列式计算出参加反应碳酸钙的质量,进而计算出大理石样品中碳酸钙的质量分数.
解答 解:根据质量守恒定律,碳酸钙与逸出二氧化碳的质量之差就是液体质量增加的质量.
设参加反应的碳酸钙的质量为x.
CaCO3+2HCl=CaCl2+H2O+CO2↑ 液体质量增加
100 44 100-44=56
x 105.6g-100g=5.6g
$\frac{100}{56}=\frac{x}{5.6g}$ x=10g
大理石样品中碳酸钙的质量分数为$\frac{10g}{12.5g}$×100%=80%.
答:大理石样品中碳酸钙的质量分数为80%.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,根据质量守恒定律计算出二氧化碳的质量是正确解答本题的前提和关键.


科目:初中化学 来源: 题型:选择题
| A. | HNO3 Ca(OH)2 NaCl | B. | KNO3 CuCl2 Na2SO4 | ||
| C. | NaOH MgSO4 BaCl2 | D. | HCl Na2CO3 Ca(NO3)2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
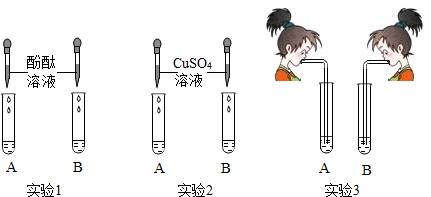
| 实验 | 实验现象 | 结论 |
| 取B 中少量溶液,加人澄清石灰水至不再 产生沉淀为止,过滤后取上层清液, 向其中加几滴酚酞试液. | 产生白色沉淀 溶液呈现红色 | 猜想3成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
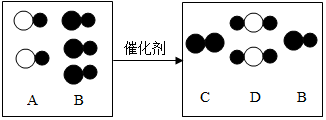
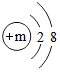 ,其微粒符号可表示为X2,则m的值为8.
,其微粒符号可表示为X2,则m的值为8.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
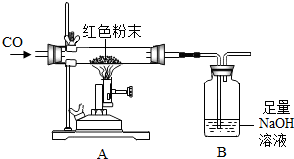 某化学兴趣小组对一包干燥的红色粉末组成进行探究,该红色粉末可能由Cu、Fe2O3两种固体中的一种或两种组成.
某化学兴趣小组对一包干燥的红色粉末组成进行探究,该红色粉末可能由Cu、Fe2O3两种固体中的一种或两种组成.| 反应前 | 反应后 | |
| Ⅰ 组 | 玻璃管和红色粉末的总质量为48.3g | 玻璃管和固体物质的总质量为47.1g |
| Ⅱ 组 | 洗气瓶和瓶中所盛物质的总质量为258.6g | 洗气瓶和瓶中所盛物质的总质量为261.91g |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量剩余固体于试管中,加水振荡,过滤 取滤液滴加无色酚酞溶液 ②取样品滴加稀盐酸 | 溶液变红 有气泡产生 | 猜想Ⅲ成立 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com