
【题目】(6分)某实验小组欲以某浓度的盐酸和大理石为原料,利用图Ⅰ所示装置制备并检验二氧化碳。已知:二氧化碳在饱和碳酸氢钠溶液中的溶解度很小。

(1)盐酸与碳酸钙反应的化学方程式为 。
(2)实验前,根据二氧化碳与石灰水的反应,该小组同学预测在B中应观察到的现象是 。
(3)实验开始后,B中并未观察到明显现象。经讨论后,该小组同学在A、B装置之间增加了C装置,重新开始实验,在B中观察到了预期现象。请结合化学方程式并用文字说明C装置的作用: 。
(4)将C装置中装满饱和碳酸氢钠溶液,即可用于收集二氧化碳,则二氧化碳应从 (填“a”或“b”)口进入C。
【答案】(1)CaCO3 + 2HCl =CaCl2 + CO2↑+ H2O
(2)产生白色浑浊
(3)将混合在CO2中的HCl除去。NaHCO3 + HCl=NaCl + CO2↑+ H2O
(4)b
【解析】
试题分析:(1)盐酸与碳酸钙反应,生成氯化钙、二氧化碳和水;
(2)二氧化碳能使澄清石灰水变浑浊;
(3)可能用的盐酸为浓盐酸,浓盐酸挥发出的氯化氢气体溶于水后先与石灰水中的氢氧化钙发生反应,然后二氧化碳才与石灰水发生反应,装置C作用是为了除去二氧化碳中混有的少量HCl气体。
(4)二氧化碳气体从b端进入,装置内气体压强增大,饱和碳酸氢钠溶液沿导管口a处排出,从而收集二氧化碳气体。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】相关叙述正确的是
A.溶液就是均一、稳定的液体
B.某物质的饱和溶液的溶质质量分数一定比不饱和溶液大
C.溶液中溶质的质量分数可以表示每100g溶液中溶质的质量
D.溶液的溶质质量分数越大,溶质的质量越大
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(5分)有一黑紫色的固体为KMnO4和MnO2的混合物,为测定混合物中KMnO4的质量分数,某同学取样20.0 g,对固体充分加热,测得固体质量随反应时间变化的曲线见下图。求:

(1)生成氧气的质量 g。
(2)样品中含高锰酸钾的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(8分)某兴趣小组同学对实验室制备氧气的条件进行如下探究实验。
(1)为探究催化剂的种类对氯酸钾分解速度的影响,甲设计以下对比实验:
Ⅰ.将3.0 g KClO3与1.0 g MnO2均匀混合加热。
Ⅱ.将x g KClO3与1.0 g CuO均匀混合加热。
在相同温度下,比较两组实验产生O2的快慢。
Ⅰ中反应的化学方程式是 ;Ⅱ中x的值应为________。
(2)乙探究了影响双氧水分解速度的某种因素。反应的化学方程式为 ,有关实验数据记录如下:
双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生O2质量 | |
Ⅰ | 50.0 g | 1% | 0.1 g | 0.013 mg |
Ⅱ | 50.0 g | 2% | 0.1 g | 0.023 mg |
Ⅲ | 50.0 g | 4% | 0.1 g | 0.044 mg |
本实验中,测量O2质量应用了图的装置。根据实验装置实验所依据的原理是 。
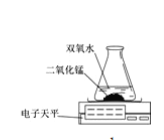
实验结论:在相同条件下,________,双氧水分解得越快。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(9分)A~H是初中化学常见的物质,其中E为黑色固体,H为蓝色沉淀,这些物质的相互转化关系如图所示,其中部分生成物和反应条件已省略.
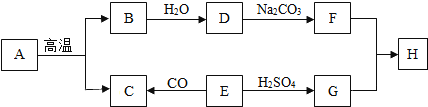
(1)写出下列物质的化学式:A ,G ,H .
(2)化学反应常伴有能量变化,物质B与水反应时会 (“吸收”或“放出”)热量.
(3)写出D→F的化学方程式: .该反应属于基本反应类型中的 反应。
(4)写出E→C的化学方程式: .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(6分)胆矾晶体部分失水后得到某硫酸铜晶体(CuSO4·xH2O),华雪同学为研究CuSO4·xH2O加热后所得物质的组成,做了以下实验:取10.7gCuSO4·xH2O晶体加热使其分解,绘制出固体的质量随温度的变化关系图。(资料:CuSO4·x H2O的相对分子质量为:160+18x)如图所示,到t1℃时该固体完全失去结晶水,(化学方程式为:CuSO4·xH2O![]() CuSO4+ xH2O↑)
CuSO4+ xH2O↑)
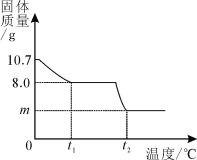
(1)(3分)计算该硫酸铜晶体(CuSO4·xH2O)中x的值。
(2)(2分)硫酸铜晶体中铜元素的质量分数是多少?(准确到0.1%)
(3)(1分)升温到t2℃,残留固体是黑色物质,则黑色固体是
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(5分)二氧化氯(ClO2)可用于自来水消毒。以粗盐为原料生产ClO2的工艺主要包括:①粗盐精制;②电解微酸性NaCl溶液;③ClO2的制取。工艺流程如下图,其中反应Ⅲ制取ClO2的化学方程式为2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O。
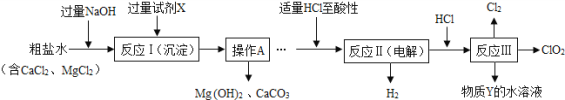
(1)试剂X是________;操作A的名称 。
(2)加入适量HCl除为了满足电解时的微酸性外,还能除去溶液中的杂质离子,请写出其中所发生的中和反应的化学方程式:________________________________。
(3)分析完成反应Ⅱ的化学方程式: _____NaCl+_____H2O![]() 。
。
(4)为提高经济效益,生产过程中除将H2和Cl2制成HCl充分利用外,还可循环使用的物质Y是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com