

| A. | 铝矾石中只含有金属氧化物 | |
| B. | 原料A可能是稀硫酸;滤液Ⅰ中要加入稍过量的原料B,原料B可能是氢氧化钠 | |
| C. | 步骤②所得沉淀是氢氧化亚铁 | |
| D. | 铝矾石炼铝需要消耗电能 |
分析 由题目的信息可知:铝矾石中含有的SiO2是非金属氧化物,故A项说法错误;原料A可能是稀硫酸也可能是盐酸,滤液Ⅰ中要加入稍过量的原料B,原料B可能是氢氧化钠是正确的;步骤②所得沉淀是氢氧化铁,氢氧化亚铁是错误的;铝矾石炼铝需要消耗电能是正确的,最后要通电分解.
解答 解:A、铝矾石中含有的SiO2是非金属氧化物,故A项说法错误,错误符合题意,故选项正确;
B、原料A可能是稀硫酸也可能是盐酸,滤液Ⅰ中要加入稍过量的原料B,原料B可能是氢氧化钠是正确的,正确但不符合题意,故选项错误;
C、步骤②所得沉淀是氢氧化铁,氢氧化亚铁是错误的,错误符合题意,故选项正确;
D、铝矾石炼铝需要消耗电能是正确的,最后要通电分解,正确但不符合题意,故选项错误;
故选A、C
点评 本考点属于实验题中的物质的制备题,综合性比较强,要掌握物质相互之间的反应规律和反应的条件.如果物质没有那种性质,就不能造实际上不存在的化学反应.本考点主要出现在选择题和实验题中.


 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案科目:初中化学 来源: 题型:选择题
 如图所示是两种气体发生化学反应的微观示意图,其中相同的球代表同种原子,下列说法正确的是( )
如图所示是两种气体发生化学反应的微观示意图,其中相同的球代表同种原子,下列说法正确的是( )| A. | 化学反应前后原子的种类不变 | B. | 生成物一定是氧化物 | ||
| C. | 化学反应前后分子的种类不变 | D. | 该反应属于置换反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
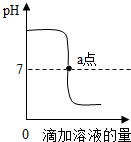 了解溶液的酸碱度具有重要的意义.
了解溶液的酸碱度具有重要的意义.| 血浆 | 7.35-7.45 |
| 胃液 | 0.9-1.5 |
| 胰液 | 7.5-8.0 |
| 尿液 | 4.7-8.4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

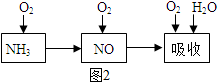
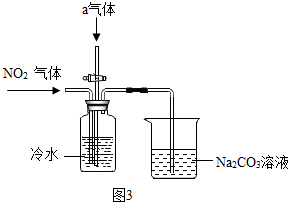
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
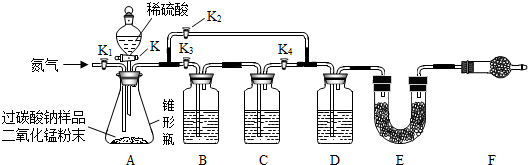
| 序号 | 实验步骤 | 实验现象 | 实验分步结论(或解释) |
| ① | 向盛有过碳酸钠固体的试管中加入适量水、振荡 | 固体溶解 | 过碳酸钠易溶于水, 能与水发生反应. |
| ② | 向该试管中加入适量的二氧化锰粉末 | 有大量气泡 产生 | |
| ③ | 将带火星的木条置于试管口 | 木条复燃 | 过碳酸钠溶于水能生成过氧化氢.过氧化氢分解,产生的气体是氧气 |
| ④ | 取试管中的上层清液加入氯化钙溶液 | 产生白色沉淀 | 过碳酸钠溶于水能生成碳酸钠. |
| 小结 | 过碳酸钠与水反应的化学方程式是Na2CO4+H2O=Na2CO3+H2O2. | ||
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 尿素[CO(NH2)2] | B. | 磷酸二氢铵(NH4H2PO4) | ||
| C. | 磷酸二氢钙[Ca(H2Po4)2] | D. | 硝酸钾(KNO3) |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com