
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
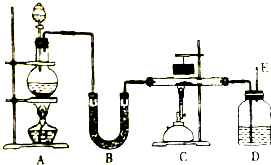 化学实验室常用甲酸(HCOOH)和浓硫酸混合加热制备一氧化碳,其化学方程式为:HCOOH$\frac{\underline{\;浓H_{2}SO_{4}\;}}{△}$CO↑+H2O,如图是制备干燥一氧化碳还原氧化铁并检验反应产物的实验装置.
化学实验室常用甲酸(HCOOH)和浓硫酸混合加热制备一氧化碳,其化学方程式为:HCOOH$\frac{\underline{\;浓H_{2}SO_{4}\;}}{△}$CO↑+H2O,如图是制备干燥一氧化碳还原氧化铁并检验反应产物的实验装置.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源:江苏省泰兴市2017届九年级下学期第二次模拟考试化学试卷 题型:选择填充题
下列我国古老工艺中属于物理变化的是
A. 米酒的酿造 B. 石膏的雕刻 C. 陶瓷的烧制 D. 钢铁的冶炼
查看答案和解析>>
科目:初中化学 来源:【全国市业模拟考试(一)化学试卷 题型:选择填充题
随着生活节奏的加快,方便的小包装食品越来越受到人们的欢迎。为了防止富脂食品氧化变质和受潮,生产厂家往往在食品包装袋中放入有某些化学物质的小袋。你认为放在这些小袋中的物质应该是( )
A. 蔗糖 无水硫酸铜 B. 食盐 生石灰
C. 还原铁粉 生石灰 D. 烧碱 生石灰
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com