
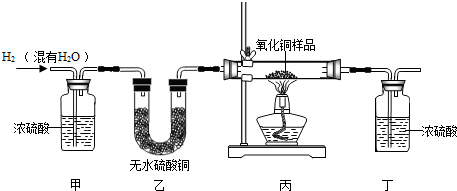
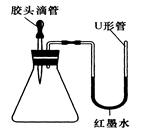
| | 装置丙 | 装置丁 |
| 反应前 | 48.8克 | 161.2克 |
| 反应后 | 46.5克 | 163.9克 |
 Cu + H2O
Cu + H2O
 ×100%="80%"
×100%="80%" 

 口算题天天练系列答案
口算题天天练系列答案科目:初中化学 来源:不详 题型:实验题
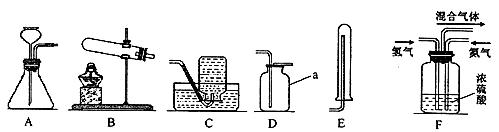
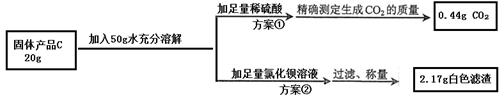
 ;已知:同温同压下气体的体积比等于气体的分子数之比)。实验室模拟合成氨气的流程如下:
;已知:同温同压下气体的体积比等于气体的分子数之比)。实验室模拟合成氨气的流程如下: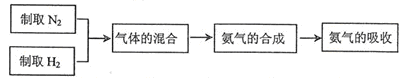
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
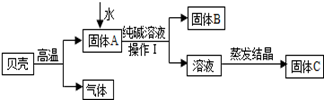
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:初中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| 实验操作 | 现象 | 结论或化学方程式 |
| 步骤Ⅰ:取少量硬水样品于试管中,向其中滴加Ca(OH)2溶液,直到反应完全。 | 有白色沉淀产生。 | MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2 |
| 步骤Ⅱ:向上述试管中滴加 溶液,直到反应完全。 | | 化学方程式: |
| 步骤Ⅲ: (填操作 名称)。 | 除去沉淀物。 | 得到澄清滤液。 |
| 步骤Ⅳ:用两试管取等量的上述滤液和原硬水样品,分别滴加 ,振荡。 | 盛有滤液的试管中 。 | 证明硬水已软化。 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com