
化学兴趣小组为测定某石灰石样品中碳酸钙的质量分数,取26g石灰石样品放在烧杯中,然后向其中逐渐加入稀盐酸,使之与样品充分反应,恰好完全反应(杂质不参加反应)时,加入稀盐酸的质量为90g,反应后烧杯中物质的总质量为105g.请计算:
(1)反应生成二氧化碳的质量
(2)样品中碳酸钙的质量分数(结果保留到0.1%)
 快捷英语周周练系列答案
快捷英语周周练系列答案科目:初中化学 来源: 题型:计算题
某兴趣小组的同学对食品中含有的维生素C(化学式为C6H8O6,可表示为Vc)进行探究.
(1)向含有Vc的溶液中滴加紫色石蕊,溶液变红,说明Vc具有的性质是 .
(2)食品中的Vc被氧气氧化时,其含量的变化如图所示,由此可得出的结论有 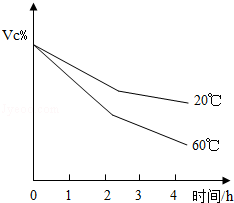
(3)小杰对某果汁饮料中Vc的含量进行测定.反应原理为C6H8O6+I2=C6H6O6+2HI,其中碘元素在反应中的 化合价变化是 .实验时取果汁饮料10mL,用煮 沸并冷却的蒸馏水稀释至50mL,向其中逐滴加入稀碘水至恰好完全反应,测得消耗碘(I2)的质量为25.4mg.则每100mL该果汁饮料中含Vc的质量是 .
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
把10g铁粉与铜粉的混合物放到盛有足量稀硫酸的烧杯中,充分反应后,烧杯中物质的总质量比反应前金属混合物与稀硫酸的总质量减少了0.1g,求混合物中铁的质量分数.
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
钢铁在生产、生活中有着广泛的应用。
(1)钢铁属于_________(填“纯净物”或“混合物”);钢铁在空气中锈蚀是铁跟空气中的水蒸气和_________共同作用的结果。为了防止钢铁的锈蚀,人们除采用在其表面涂油漆的方法外,还可_________(任填一种方法);工业上用稀盐酸除去铁锈(主要成分为Fe2O3),写出该反应的化学方程式:_________________________。
(2)某钢铁厂为分析赤铁矿中Fe2O3的质量分数:准确称取20g样品,在高温条件下用足量CO气体还原,充分反应(假设其他杂质不与CO反应)后冷却、称重,质量为15.2g。计算该赤铁矿样品中Fe2O3的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
将8.1g氧化锌固体放入100g稀硫酸中,恰好完全反应.试计算:
①可生成硫酸锌多少克?
②所用稀硫酸的溶质质量分数是多少?(化学方程式:ZnO+H2SO4=ZnSO4+H2O)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
100g某一定质量分数的稀硫酸恰好与13g锌完全反应.请计算:
(1)反应产生氢气的质量是 g.
(2)稀硫酸中溶质的质量分数.(写出计算过程).
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
某同学称取a g铜锌合金,加入足量稀硫酸,充分反应后测得生成气体的质量为b g,剩余固体经过滤、洗涤、干燥后,称得质量为c g.请问:
(1)a g铜锌合金中锌的质量为 g(用代数式表示).
(2)根据化学反应方程式,推导出a、b、c三者之间的等量关系(写出详细的计算推导过程).
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
用氢氧化钠溶液测定某硫酸溶液溶质的质量分数.实验如下:取25g该硫酸溶液,加入到烧杯中,然后把50g质量分数为10%的氢氧化钠溶液不断滴入烧杯中,同时用电子PH计不断读取反应时的PH,得出如图所示的关系,求;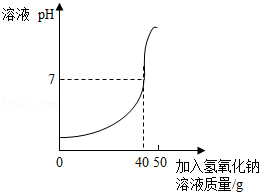
(1)该硫酸溶液溶质的质量分数.
(2)配制500g上述硫酸溶液,所需质量分数为98%的硫酸溶液的质量.
查看答案和解析>>
科目:初中化学 来源: 题型:单选题
利用下列仪器制取相关气体,不能实现的是
| A.用锌和稀硫酸制取氢气 | B.用双氧水和二氧化锰制取氧气 |
| C.用氯酸钾分解制取氧气 | D.用石灰石和稀盐酸制取二氧化碳 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com