
【题目】我国青海湖采集的天然碱样品可表示为aNa2CO3·bNaHCO3·cH2O(a、b、c为最简整数比)。小红同学为测定其组成,称取该天然碱样品16.6g进行如下实验:

已知:1.碳酸钠比较稳定,加热时不分解 ;2. 2NaHCO3![]() Na2CO3 +CO2 ↑ +H2O
Na2CO3 +CO2 ↑ +H2O
3.图中B处为两个单向阀:推注射器时A1关闭,A2处打开;拉注射器时,A1打开进空气,A2关闭。
实验步骤
实验时,组装好装置,实验前应先 ,然后,实验步骤是:
① 反复推拉注射器 ② 称量E、F的质量 ③ 关闭弹簧夹,加热D处试管直到反
应不再进行 ④ 打开弹簧夹,再次反复缓缓推拉注射器 ⑤ 再次称量E、F的质量。
(二)问题探究:
(2) E中的药品为 ,E的作用是 。C、F、G中装有碱石灰(生石灰与烧碱的固体混合物),则C的作用是 , F的作用是 。写出 F装置中所发生反应的一个化学方程式 。
(3)实验步骤②与③能否颠倒 (填“能”或“不能”)。若不进行步骤④的操作,则所测得的碳酸氢钠质量 (填“偏大”、“偏小”、“无影响”), 该操作中推注射器时缓缓的目的是 ;若没有G装置,则碳酸氢钠的质量 (填“偏大”、“偏小”、“无影响”)。
(4)下表是实验记录数据:
反应前 | 反应后 |
E的质量为100.0g | E的质量为102.25g |
F的质量为50.0g | F的质量为51.1g |
则: ① 碳酸氢钠分解生成二氧化碳的质量为 g
② 碳酸氢钠的质量为 g
③ 该天然碱的化学式中a:b:c= 。
【答案】(1)检查装置的气密性 ;(2)浓硫酸; 吸收生成的水;吸收空气中的二氧化碳和水分;吸收生成的二氧化碳;2NaOH + CO2 ==== Na2CO3 + H2O;(3)不能; 偏小;使二氧化碳被充分吸收; 偏大(4) ① 1.1 ② 4.2 ③ 2:1:2
【解析】
试题分析:(一)实验步骤 (1)实验时,组装好装置,实验前应先检验装置的气密性;(2) E中的药品为浓硫酸,其作用是吸收生成的水分;C、F、G中装有碱石灰(生石灰与烧碱的固体混合物),则C的作用是吸收空气中的二氧化碳和水分;F的作用是吸收生成的二氧化碳,F装置中所发生反应的一个化学方程式2NaOH + CO2 ==== Na2CO3 + H2O;(3)实验步骤②与③不能颠倒,若不进行步骤④的操作,则所测得的碳酸氢钠质量偏小,该操作中推注射器时缓缓的目的是使二氧化碳被充分吸收,若没有G装置,则碳酸氢钠的质量偏大;(4)根据装置的作用可知① 碳酸氢钠分解生成二氧化碳的质量为1.1g,② 碳酸氢钠的质量为X 2NaHCO3△ Na2CO3+H2O+CO2↑ 生成水的质量为Y
18 44
X Y 1.1g
168::4=X:1.1g 18:44=y:1.1g
X=4.2g y=0.45g
16.6g该天然碱中水的质量为2.25g-0.45g=1.8g 碳酸氢钠的质量为4.2g,
碳酸钠的质量为:16.6g-1.8g-4.2g=10.6g故
③ 该天然碱的化学式中a:b:c=10.6/106:4.2/84:1.8/18=2:1:2


 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:初中化学 来源: 题型:
【题目】实验室中的试剂一般要密封保存,否则可能会与空气接触而变质。某研究性学习小组发现一瓶未密闭的NaOH固体,对其成分提出以下假设,并完成了实验探究。
假设1:只含NaOH; 假设2:含NaOH和Na2CO3; 假设3:只含Na2CO3
(1)取少量样品于试管中,加入足量稀盐酸,观察到 ,说明假设1不成立,假设2或假设3成立。
(2)进一步探究的过程如下:
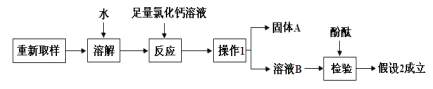
①“操作1”的名称是 ,其中要用到玻璃棒,其作用是 。
②加入足量CaCl2溶液的作用是 。
③加酚酞检验“溶液B”的现象是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学想用pH试纸测定一些物质的pH,下列做法能达到实验目的是( )
A.用湿润的pH试纸测定稀硫酸的pH
B.用干燥的pH试纸测定二氧化碳气体的pH
C.用干燥的pH试纸测定浓硫酸的pH
D.用干燥的pH试纸测定氢氧化钠稀溶液的pH
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(7分)在宏观、微观、符号之间建立联系是化学学科的特点。
(1)现有下列微粒:①2O ②2O2 ③Al3+ ④SO42-,其中能表示2个分子的是 (填序号);由③和④两种微粒构成的化合物的化学式是 。
(2)“三效催化转换器”可将汽车尾气中有毒气体处理为无毒气体,反应前后分子变化的微观示意图如下所示。
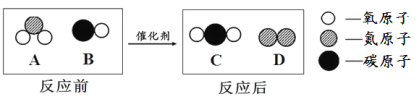
请回答以下问题:
①A中氮元素与氧元素的质量比为 。
②四种物质中,属于氧化物的是 (填字母)。
③上述变化的化学方程式为 。
④若有n个B分子参与反应,则生成物中含有的氧原子总数为 个。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列由实验现象得到的结论,正确的是( )
A.向某溶液中加入BaCl2溶液,生成不溶于稀硝酸的白色沉淀,说明该溶液中一定含SO42﹣
B.向某固体中加入稀盐酸,有气泡产生,说明此固体一定是金属
C.氧化钠晶体不导电,说明氧化钠晶体中不含离子
D.向某溶液中滴加无色酚酞试液,酚酞试液变红色,说明该溶液显碱性
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)的外观与食盐很相似,有咸味,误食易中毒.区别它们的一种方法是:将两者分别加热到320℃,不分解的是食盐,能分解并放出一种具有刺激性气味气体的是亚硝酸钠.该气体可能是( )
A.NH3 B.SO2 C.NO2 D.N2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(3分)硫酸铜晶体常用作农业和渔业的杀虫剂、杀菌剂,某同学设计了下列两条途径由废铜料(含铁)生产硫酸铜晶体,其过程如下所示:
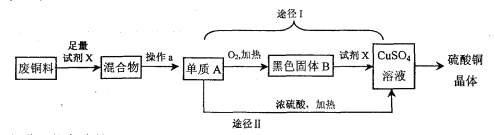
(1)操作a的名称是: ;
(2)已知:Cu+2H2SO4(浓) △CuSO4+SO2↑+2H2O。则途径I与途径II相比,其优点体现在:
①不产生二氧化硫有毒气体,不会污染空气;② ;
(3)将废铜料投入硫酸铜溶液中充分搅拌,发生反应的化学方程式为: 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(9分)医用二水合氯化钙可用于补钙、抗过敏和消炎等,以某碳酸钙样品(其中含少量Al3+、Fe3+等杂质)生产医用二水合氯化钙的工艺流程为: (已知二水合氯化钙在温度超过160°C时分解为氯化钙和水)
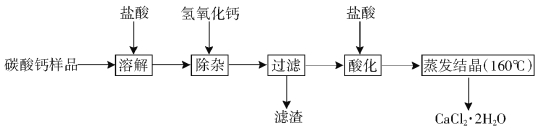
已知:查阅资料得知氢氧化物沉淀及溶解时的pH为:
氢氧化物 | Fe(OH)3 | Al(OH)3 | |
开始沉淀时的pH | 2.3 | 4.0 | 开始溶解:7.8 |
完全沉淀时的pH | 3.7 | 5.2 | 完全溶解:10.8 |
(1)在实验室进行溶解时玻璃棒的作用是 ,过滤时用到的玻璃仪器有烧杯、玻璃棒、 。
(2)除杂操作是加入稍过量的氢氧化钙,调节溶液的pH使Al3+、Fe3+全部转化为沉淀,此时应该控制溶液的的pH(X)范围是 ;滤渣A的主要成分的化学式为 。
(3)酸化时加盐酸的主要目的为了 。
(4)蒸发结晶时,必须控制温度低于160℃的原因是 。
(5)若所用碳酸钙样品12.5Kg,最后所得的产物中含氯化钙11.1Kg,则样品中碳酸钙的质量分数最大为多少 ?(写出计算过程,3分)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】两种溶液混合后能发生化学反应,且溶液总质量不会发生变化的是( )
A.碳酸钠溶液和氯化钙溶液 B.碳酸钠溶液和稀盐酸
C.氢氧化钾溶液和硫酸溶液 D.石灰水和氯化钠溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com