
分析 根据质量守恒定律,化学反应前后元素的种类质量不变来解释即可.
解答 解:甲醇和辛烷燃烧的反应物的组成元素都是碳、氢、氧,根据质量守恒定律可知,它们燃烧的产物都是水和二氧化碳;两者完全然后后碳元素完全进入二氧化碳,氢元素完全进入水,因为甲醇中碳、氢元素的质量比和辛烷中碳、氢元素的质量比不同,因此生成二氧化碳和水的质量比不同.
答:甲醇和辛烷燃烧的反应物的组成元素都是碳、氢、氧,根据质量守恒定律可知,它们燃烧的产物都是水和二氧化碳;两者完全然后后碳元素完全进入二氧化碳,氢元素完全进入水,因为甲醇中碳、氢元素的质量比和辛烷中碳、氢元素的质量比不同,因此生成二氧化碳和水的质量比不同.
点评 本题考查了质量守恒定律的应用;在发生化学反应前后元素的种类和质量是不变的.


科目:初中化学 来源: 题型:实验探究题
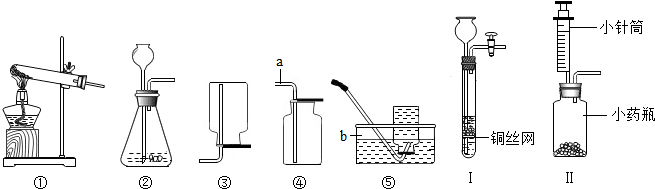
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
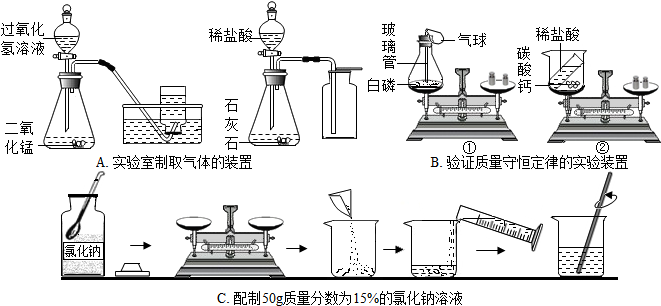
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铜与铜锌合金──稀盐酸 | B. | 硬水与软水──肥皂水 | ||
| C. | N2与CO2──燃着的木条 | D. | 水与澄清石灰水──CO2 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
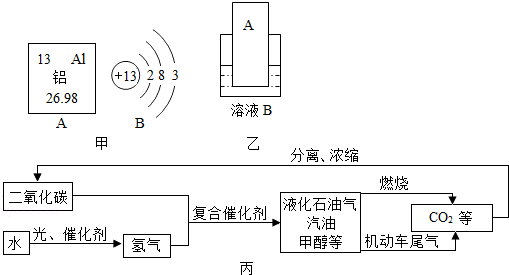
 A、B、C均为初中化学常见纯净物,它们之间的转化关系如图所示(图中“→”表示物质间存
A、B、C均为初中化学常见纯净物,它们之间的转化关系如图所示(图中“→”表示物质间存查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 方案 | 优点 | 缺点 |
| ① | 能够减轻飞船发射重量 | 不能消除呼吸过程产生的二氧化碳 |
| ② | 能够消除呼吸过程产生的二氧化碳 | 不能减轻飞船发射重量 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 5.5g | B. | 5g | C. | 4.5g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1462 |
| 沸点/℃ | 2467 | 2990 | 2750 | -- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com