
【题目】正常情况下人的胃液pH为0.8—1.5,相应含氯化氢的质量分数为0.2%—0.4%,胃液中氯化氢过多过少都不利于健康。某人出现反胃、吐酸水的症状,经检查其胃液中氯化氢的质量分数为1.495%(胃液密度约为1g/cm3)。
(1)正常情况下,人的胃液显_________性。
(2)若人的胃液总量为100mL,正常胃液中HCl的质量范围为___________________ g。
(3)服用碱性物质可以治疗胃液中HCl含量过多,你认为该患者 ___________ (填能或不能)服用熟石灰来治疗胃酸过多,理由是 ______________________________________ 。
(4)医生给患者开的药是胃舒平[有效成分是Al(OH)3],每片胃舒平含Al(OH)3 的质量为0.39g。请根据化学方程式计算该患者至少服用________片胃舒平,胃液才能恢复正常? (请写出计算过程)
【答案】 酸性 0.2—0.4g 不能 因为氢氧化钙有腐蚀性。 该患者至少服用2片胃舒平,胃液才能恢复正常。
【解析】(1) 根据正常情况下人的胃液pH为0.8—1.5解答; (2)根据胃液的体积、密度、含HCl的溶质质量分数可以计算氯化氢的质量范围;(3)根据氢氧化钙有腐蚀性分析解答;(4) 根据化学方程式可以计算服用胃舒平的片数。(1) 正常情况下人的胃液pH为0.8—1.5,小于7,显酸性;(2)100mL胃液的质量为100mL×1g/cm3=100g,正常人胃液中HCl的质量最小值为100g×0.2%=0.2g,最大值为100g×0.4%=0.4g;(3) 患者不能服用熟石灰来治疗胃酸过多,理由是因为氢氧化钙有腐蚀性;(4)该患者胃酸中至少多出HCl的质量为100ml×1g/cm3×1.495%-0.4g=1.095g。设要使该患者恢复正常,至少需要消耗Al(OH)3的质量为x。
3HCl+Al(OH)3═AlCl3+3H2O
109.5 78
1.095g x![]()
x=0.78g
至少服用胃舒平的片数为0.78g÷0.39g∕片=2片
答:至少服用2片胃舒平,胃液才能恢复正常。


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案科目:初中化学 来源: 题型:
【题目】完成下列化学方程式
(1)氧化铁与稀盐酸反应____________________
(2)氢氧化钠与三氧化硫反应____________________
(3)硫酸铜溶液与硝酸钡溶液反应____________________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(8分)化学就在我们身边,它与我们的生活息息相关。
(1)下图为某食品包装袋的部分说明。
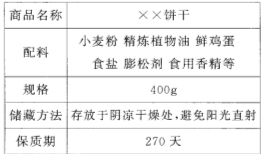
请回答下列问题:
①在饼干的配料中,富含油脂的是 ;
②配料中可用于腌渍蔬菜的物质是 ;
③小麦粉中富含糖类,糖类在人体内经过一系列的变化最终转化为水和 ;
④食用香精中含有香豆素(C9 H6 O2),香豆素中碳、氢、氧三种元素的质量比为 。
(2)现有H、C、O、Ca四种元素,请选用其中的元素写出符合下列要求的物质的化学式。
①最轻的气体 ;
②“西气东输”中“气”的主要成分 ;
③人体中含量最多的物质 ;
④可用作食品干燥剂的氧化物 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】过氧化钙晶体(化学式为:CaO2·yH2O,化学式中的“yH2O”称为结晶水),常温该晶体下为白色,能溶于酸,难溶于水、乙醇,是一种温和的氧化剂,常用于鱼类长途运输的增氧剂等。
(1) 过氧化钙晶体可用下列方法制备:
CaCl2+H2O2+NH3+H2O![]() CaO2·yH2O↓+NH4Cl。
CaO2·yH2O↓+NH4Cl。
用如下制取装置制备过氧化钙晶体。
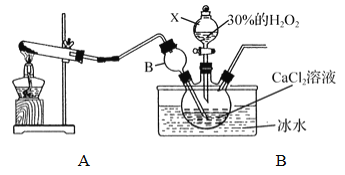
①装置A中生成的气体为________,此装置在初中化学实验中可用于制取_______(填某气体);仪器X的名称为________。
②装置C采用冰水浴控制温度在0℃左右,可能的原因主要有:
Ⅰ. 该反应是放热反应,温度低有利于提高CaO2·yH2O产率;
Ⅱ. ____________________________
③反应结束后,经过滤、洗涤、低温烘干可获得CaO2·yH2O。检验晶体已洗涤干净的方法为:取最后一次洗涤液,滴加____________,若__________,则晶体已经洗涤干净。
(2)为确定过氧化钙晶体的组成,某化学兴趣小组称取21.6克晶体用热分析仪对其进行热分解实验,并绘制成固体质量与温度关系图(过氧化钙晶体受热时会先失去结晶水),根据下图可知y=_______, 350℃时发生的分解反应方程式为_______________。
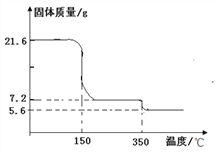
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为A、B、C三种固体物质(不含结晶水)的溶解度曲线.下列说法错误的是
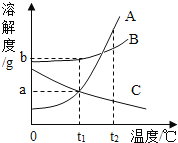
A.![]() ℃时,三种物质中B的溶解度最大
℃时,三种物质中B的溶解度最大
B.![]() ℃时,取三种物质各ag分别放入100g水中充分溶解,只有C物质能形成饱和溶液
℃时,取三种物质各ag分别放入100g水中充分溶解,只有C物质能形成饱和溶液
C.将等质量的三种物质的饱和溶液分别由![]() ℃降温到
℃降温到![]() ℃,A溶液中析出的晶体质量最大
℃,A溶液中析出的晶体质量最大
D.可用增加溶剂的方法使接近饱和的B溶液变为饱和溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
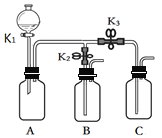
【题目】化学小组的同学用下图所示装置进行如下实验,实验前K1、K2、K3均为关闭状态。
内容 步骤 | 实验步骤 |
实验1 | B、C中分别盛有无色酚酞试液,打开K1,从分液漏斗中加入浓氨水,关闭K1,然后打开K2、K3。 |
实验2 | A中盛满CO2,B中盛有氢氧化钙溶液,C中盛有稀盐酸。 ①打开K1,从分液漏斗慢慢放入适量的氢氧化钠溶液,关闭K1。 ②一段时间后打开K2,观察到有A中有沉淀产生时,迅速关闭K2。 ③再打开K3,观察到A中有气泡产生。 |
(1)实验1中,可以观察到的现象是__________。
(2)实验2中,步骤①中所发生反应的化学方程式为____________________。
(3)实验2中,请解释步骤③产生气泡的原因为____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业废料石膏(CaSO42H2O)可以“变废为宝”,用于生产氧化钙、硫酸钾、电石(化学名称为碳化钙)等。某研究性学习小组展开了如下系列研究。
一.高纯CaO的制备
【资料一】
Ⅰ.无水硫酸铜遇水变成蓝色的硫酸铜晶体。
Ⅱ.石膏(CaSO42H2O)与碳粉高温煅烧生成氧化钙和几种气态非金属氧化物。
Ⅲ.SO2能使品红溶液褪色,也能使澄清石灰水变浑浊,还能被高锰酸钾溶液氧化而除去。
甲同学用如下装置制备CaO并验证石膏与焦炭高温反应的其他产物。

实验过程中发现:B中无水硫酸铜变蓝,C中产生_____________现象证明有SO2生成,装置_____中无明显变化和装置F中_____________现象证明有CO2生成。写出石膏与碳粉在高温条件下反应的化学方程式:___________________。
二.硫酸钾和电石的制备
乙同学模拟生产化肥硫酸钾和电石的流程如下:

【资料二】氧化钙与焦炭在高温下反应生成碳化钙和一氧化碳。
(1)反应①的化学方程式为__________________________。证明固体M中不含CaCO3的方法是____________________________(写出实验的方法、现象)。
(2)反应②的化学方程式为(NH4)2SO4 + 2KCl ═ K2SO4↓+ 2NH4Cl,该反应能析出K2SO4晶体的原因是_____________________________________。
(3)假设上述流程中制得的碳化钙(化学式为CaCx)固体中只含杂质CaO,乙小组同学为测定CaCx中x的值进行如下实验。
【资料三】碳化钙在空气中灼烧生成氧化钙和二氧化碳气体。
步骤一:称取3.76g样品于下图所示石英管中(测定装置图如下,夹持及加热装置省略),反应前缓缓通入空气,高温灼烧石英管中的样品至反应完全后继续缓缓通入空气,测得丙溶液的质量比反应前增重了4.4g。(玻璃纤维可防止固体粉末进入导管)

步骤二:将石英管内剩余固体全部转移到水中,加入足量碳酸钠溶液,经搅拌、过滤、洗涤、干燥等操作得到碳酸钙固体6克。试回答下列问题:
①装置甲的作用是_______。反应完全后继续缓缓通入空气的目的是_________。
②根据步骤一、二计算该样品中钙、碳、氧的质量比为______________,计算确定CaCx的化学式(请写出计算过程)________。
③应用:丙同学经查阅资料知道实验室常用电石(主要成分为碳化钙)与水反应制取乙炔气体(发生装置如图)。经实验发现,电石与水反应非常剧烈,为控制反应的速度以得到平稳的气流,下列改进方法可行的是______。
A.改长颈漏斗为分液漏斗或注射器 B.将电石研成粉末
C.将锥形瓶置于冰水浴中 D.用饱和食盐水代替水(电石与氯化钠不反应)

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“见著知微,见微知著”是化学思维的方式。
(1)从微观知宏观
下图所示为元素周期表中部分元素的相关信息,根据要求回答相关问题

①元素与硫元素化学性质相似的原因是____________;
②写出12号和17号元素形成化合物的化学式__________.
(2)从宏观知微观
①木炭在氧气中燃烧比在空气中燃烧更剧烈,结合下图A从微观角度解释其原因_______________________;

②H2SO4溶液能与BaCl2溶液反应产生白色沉淀,其微观变化过程如上图B所示,参加反应的离子是_________(填离子符号)。CuCl2溶液能与NaOH溶液反应产生蓝色沉淀;从反应的微观实质可以推测,CuSO4溶液可以和某溶液反应同时产生两种沉淀,写出该反应的化学方程式___________________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是一种新型多功能水处理剂。下图为制取(K2FeO4)的流程,请根据图示回答下列问题:

(1)固体B中含有的物质是_______________________;
(2)操作I的名称是_________,玻璃棒在操作中的作用是____________;
(3)请写出反应①的化学方程式________;反应②属于______反应(填基本反应类型);
(4)写出溶液C中溶质的一种用途_________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com