
【题目】完成下列化学方程式
(1)氧化铁与稀盐酸反应____________________
(2)氢氧化钠与三氧化硫反应____________________
(3)硫酸铜溶液与硝酸钡溶液反应____________________
 优等生题库系列答案
优等生题库系列答案科目:初中化学 来源: 题型:
【题目】下列图像不能正确反映其对应关系的是( )
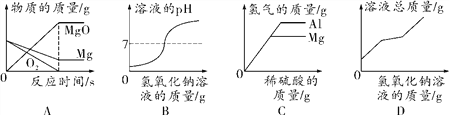
A. 等质量的镁和氧气充分反应
B. 将氢氧化钠溶液滴入稀硫酸中
C. 将质量分数为20%的稀硫酸分别滴入等质量的镁粉和铝粉中
D. 将一定质量分数的氢氧化钠溶液逐滴加入一定质量的氯化铁和盐酸的混合溶液中
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某兴趣小组用图1装置进行实验时发现:烧杯中饱和石灰水先变浑浊,后逐渐澄清。
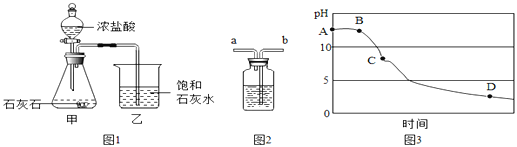
⑴ 写出甲装置中发生反应的化学方程式_______________;
⑵ 为探究“饱和石灰水浑浊后变澄清的原因”,该小组同学开展了如下活动:
【查阅文献】碳酸钙(碳酸钠等)与二氧化碳、水反应生成可溶于水的碳酸氢钙(碳酸氢钠等)
【提出假设】假设1:二氧化碳与碳酸钙、水发生反应生成碳酸氢钙;
假设2:__________________________;
【设计实验】为除去CO2中的氯化氢气体,小华在图1中甲、乙装置之间增加图2装置,装置的连接顺序是甲→_________→_________→乙(填字母序号);其中盛放的试剂合理的是___________(填选项序号:A.浓硫酸 B.NaOH溶液 C.饱和NaHCO3溶液;
【实验现象】饱和石灰水浑浊后,继续通入足量CO2,沉淀部分溶解但最终并未完全澄清。
【得出结论】假设2成立;
⑶同学们在老师指导下仍用图1所示装置进行实验,但同时用pH传感器监测烧杯中溶液的pH,所得图像如图3所示:
①AB段pH几乎不变的原因可能是_____________________;D点处溶液的溶质主要有(填化学式)__________;
② BC段主要发生两个化学反应:a二氧化碳与澄清石灰水反应;b(写出化学方程式)_______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】除去下列物质中混有的杂质,所用试剂和操作方法不正确的是![]()
物质 | 所含杂质 | 除杂质选用的试剂或方法 | |
A | NaCl溶液 | NaOH | 滴加适量的稀盐酸 |
B | Cu | Fe | 加入足量的稀盐酸并过滤 |
C |
| CO | 在氧气中点燃 |
D |
|
| 加入足量的水溶解并过滤、洗涤、干燥 |
A. A B. B C. C D. D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室常利用以下装置完成气体制备及性质实验![]() 请回答:
请回答: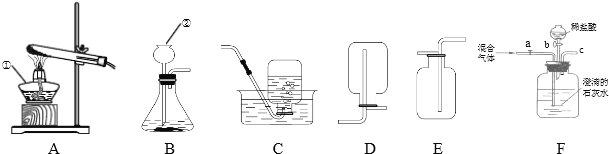
![]() 指出编号仪器的名称:
指出编号仪器的名称:![]() _________,
_________,![]() ___________.
___________.
![]() 以上 _______
以上 _______![]() 从A--E中选择
从A--E中选择![]() 装置有一处明显错误,请加以改正____
装置有一处明显错误,请加以改正____![]() 利用改正后的装置继续完成后面的实验.
利用改正后的装置继续完成后面的实验.
![]() 欲使用高锰酸钾制取氧气,应选择的发生装置是 _______
欲使用高锰酸钾制取氧气,应选择的发生装置是 _______![]() 填字母
填字母![]() ,反应原理用化学方程式表示为 _____;为防止高锰酸钾粉末进入导管,应采取的措施是 ____;若使用C装置收集氧气,实验结束时,应先从水槽中移出导管,再熄灭酒精灯,原因是 ______.
,反应原理用化学方程式表示为 _____;为防止高锰酸钾粉末进入导管,应采取的措施是 ____;若使用C装置收集氧气,实验结束时,应先从水槽中移出导管,再熄灭酒精灯,原因是 ______.
![]() 将
将![]() 和CO的混合气体通过F装置
和CO的混合气体通过F装置![]() 液体药品均足量
液体药品均足量![]() ,实验开始时关闭活塞b,打开活塞a,广口瓶中观察到的现象是 ____,此时从导管c逸出的气体主要是 ______
,实验开始时关闭活塞b,打开活塞a,广口瓶中观察到的现象是 ____,此时从导管c逸出的气体主要是 ______![]() 一段时间后,再关闭活塞a,打开活塞b,将分液漏斗中的稀盐酸滴入广口瓶中,此时溢出的气体主要是 ___
一段时间后,再关闭活塞a,打开活塞b,将分液漏斗中的稀盐酸滴入广口瓶中,此时溢出的气体主要是 ___![]() 反应原理用化学方程式表示为 ______
反应原理用化学方程式表示为 ______![]() 欲收集该气体,应选择的装置是 ___
欲收集该气体,应选择的装置是 ___![]() 填序号
填序号![]() 验满的方法是 ___.
验满的方法是 ___.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列四个图象中,能正确反映对应变化关系的是
|
|
|
|
A.向一定量的氢氧化钠溶液中滴加稀盐酸 | B.向一定量的稀盐酸中加入大理石 | C.一定量的稀盐酸中加入铁粉 | D.加热一定量的高锰酸钾固体 |
A. A B. B C. C D. D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】钴(Co)常见化合价为+2、+3。资料:氢氧化钴 Co(OH)2粉红色固体,难溶于水;氢氧化高钴Co(OH)
(1)写出硫酸高钴的化学式_________________;CoCO读作_________________。
(2)写出氯化钴溶液和氢氧化钠溶液反应的化学方程式_________________________________。
(3)2Co(OH)+6_________________=2CoCl+Cl↑+6HO
(4)177g钴在空气中加热至白热时完全燃烧生成________g Co3O4
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面科普短文(原文作者:王龙飞等,有删改)。
纯净的臭氧(O3)在常温下是天蓝色的气体,有难闻的鱼腥臭味,不稳定,易转化为氧气。它虽然是空气质量播报中提及的大气污染物,但臭氧层中的臭氧能吸收紫外线,保护地面生物不受伤害。而且近年来臭氧的应用发展较快,很受人们的重视。
生产中大量使用的臭氧通常由以下方法制得。
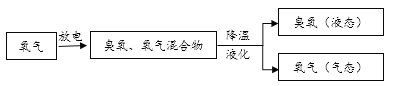
臭氧处理饮用水。早在19世纪中期的欧洲,臭氧已被用于饮用水处理。由于臭氧有强氧化性,可以与水中的有害化合物(如硫化铅)发生反应,处理效果好,不会产生异味。
臭氧做漂白剂。许多有机色素的分子遇臭氧后会被破坏,成为无色物质。因此,臭氧可作为漂白剂,用来漂白麻、棉、纸张等。实践证明,臭氧的漂白作用是氯气的15倍之多。
臭氧用于医用消毒。与传统的消毒剂氯气相比,臭氧有许多优点,如表所示。
表 臭氧和氯气的消毒情况对比
消毒效果 | 消毒所需时间(0.2 mg/L) | 二次污染 | 投资成本 (900 m3设备) | |
臭氧 | 可杀灭一切微生物,包括细菌、病毒、芽孢等 | < 5 min | 臭氧很快转化为氧气,无二次污染,高效环保 | 约45万元 |
氯气 | 能杀灭除芽孢以外的大多数微生物,对病毒作用弱 | > 30 min | 刺激皮肤,有难闻气味,对人体有害,有二次污染、残留,用后需大量水冲洗 | 约3~4万元 |
依据文章内容回答下列问题。
(1)臭氧的相对分子质量为_________。
(2)臭氧处理饮用水时,利用了臭氧的_________(填“物理”或“化学”)性质。
(3)臭氧转化为氧气的微观示意图如下,请在方框中补全相应微粒的图示。

![]()
(4)为了快速杀灭病毒,应选择的消毒剂是__________。
(5)下列关于臭氧的说法中,正确的是________。
A.臭氧的漂白作用比氯气强
B.由氧气制得臭氧的过程中,既有物理变化也有化学变化
C.臭氧在生产生活中有很多用途,对人类有益无害
D.臭氧稳定性差,不利于储存,其应用可能会受到限制
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】正常情况下人的胃液pH为0.8—1.5,相应含氯化氢的质量分数为0.2%—0.4%,胃液中氯化氢过多过少都不利于健康。某人出现反胃、吐酸水的症状,经检查其胃液中氯化氢的质量分数为1.495%(胃液密度约为1g/cm3)。
(1)正常情况下,人的胃液显_________性。
(2)若人的胃液总量为100mL,正常胃液中HCl的质量范围为___________________ g。
(3)服用碱性物质可以治疗胃液中HCl含量过多,你认为该患者 ___________ (填能或不能)服用熟石灰来治疗胃酸过多,理由是 ______________________________________ 。
(4)医生给患者开的药是胃舒平[有效成分是Al(OH)3],每片胃舒平含Al(OH)3 的质量为0.39g。请根据化学方程式计算该患者至少服用________片胃舒平,胃液才能恢复正常? (请写出计算过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com