

分析 酒精灯是常用的加热仪器,水槽是盛水的仪器;制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.如图H所示,将二氧化碳倒入烧杯中,观察到现象是:下面的蜡烛先熄灭,说明的蜡烛后熄灭;说明二氧化碳具有的性质是:二氧化碳既不能燃烧,也不能支持燃烧;二氧化碳的密度比空气大;根据红磷燃烧产生大量白烟,以及测定空气中氧气含量的实验原理利用红磷燃烧消耗空气中的氧气,使左边集气瓶内气体体积变小,压强变小,从而在外部大气压的作用下使烧杯内的水进入集气瓶,通过测量进入集气瓶中水的量来确定空气中氧气的体积分数去分析解答.
解答 解:(1)酒精灯是常用的加热仪器,水槽是盛水的仪器,故答案为:酒精灯;水槽;
(2)如果用氯酸钾和二氧化锰制氧气就需要加热,氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,配平即可;故答案为:A;2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
(3)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;若用C装置代替B装置进行实验,优点为:可以控制反应的发生和停止;故答案为:D;可以控制反应的发生和停止;
(4)铁和氧气在点燃的条件下生成四氧化三铁,配平即可;故答案为:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4
(5)如图H所示,将二氧化碳倒入烧杯中,观察到现象是:下面的蜡烛先熄灭,说明的蜡烛后熄灭;说明二氧化碳具有的性质是:二氧化碳既不能燃烧,也不能支持燃烧;二氧化碳的密度比空气大;故答案为:下面的蜡烛先熄灭,说明的蜡烛后熄灭;二氧化碳既不能燃烧,也不能支持燃烧;二氧化碳的密度比空气大;
(6)磷和氧气在点燃的条件下生成五氧化二磷,配平即可;下列有关此实验的说法正确的是:燃烧匙中的红磷不可以换成硫和木炭;选用足量红磷进行实验是为了耗尽集气瓶内氧气;故答案为:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;BC;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、装置改进的优点和气体的性质等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.


科目:初中化学 来源: 题型:解答题
| 物 质 | 样 品 | 消耗稀盐酸质量 | 反应后溶液质量 |
| 质量(g) | 12 | 72.4 | 80 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 如图装置(夹持仪器略去)可用于探究碳及其氧化物的某些性质.
如图装置(夹持仪器略去)可用于探究碳及其氧化物的某些性质.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
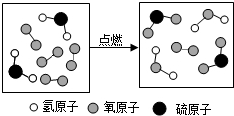
| A. | 生成物中有单质 | B. | 反应前后氧元素的化合价不变 | ||
| C. |  中硫元素的化合价为+2价 中硫元素的化合价为+2价 | D. | 参加反应的 和 和 的质量比为17:24 的质量比为17:24 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com