
【题目】用“侯氏制碱法”制得的纯碱中常含有氯化钠等杂质,化学兴趣小组欲对某品牌纯碱样品中碳酸钠的质量分数进行实验探究,他们设计了下列两种实验方案进行试验.
[方案一]样品与氯化钙溶液反应,测定Na2CO3的质量分数
(1)样品与氯化钙溶液的反应实验(杂质不与氯化钙溶液反应):取一定量纯碱样品配成溶液后,滴加过量的CaCl2溶液.
(2)分析滴加的CaCl2溶液要过量的原因: ;
(3)将反应后的混合物进行过滤,把获得的沉淀物洗涤、干燥、称量.利用沉淀物质量计算Na2CO3的质量分数为91%.如果不洗涤沉淀物会造成测定结果大于91%,这是因为 .
[方案二]样品与稀盐酸反应,测定Na2CO3的质量分数
利用如图所示实验装置(铁架台略去)和试剂,通过测定样品和稀盐酸反应产生的CO2气体的质量,计算Na2CO3的质量分数(装置气密性良好,忽略盐酸的挥发性且每步反应或作用都是完全的).

(4)打开止水夹K,先对装置A和B(已连接)通入已除去CO2的空气一会儿,其目的是 ,然后再接上装置C和D.
(5)关闭止水夹K,加入足量的稀盐酸(杂质不与盐酸反应).
(6)待装置A中的反应结束后,再一次打开止水夹K,继续往装置通入已除去CO2的空气一会儿,若省略此步骤,将会使测定结果 (选填“偏大”或“偏小”).若没有装置D,将会使测定结果 (选填“偏大”或“偏小”).
【答案】(2)使样品中的碳酸钠完全反应;(3)若不洗涤沉淀物,那么沉淀物的质量为增大,利用沉淀物质量计算Na2CO3的质量就会增大;(4)为了排尽装置A和B中含有的CO2;(6)偏小;偏大.
【解析】
(2)滴加的CaCl2溶液要过量的原因与碳酸钠充分反应;
(3)不洗涤碳酸钙表面可能会附着一层可溶性物质使沉淀物质量增加,所以使得计算出的碳酸钠的质量增大从而导致样品中Na2CO3的质量分数偏大;
(4)空气中含有二氧化碳,所以打开止水夹K,先对装置A和B(已连接)通入已除去CO2的空气一会儿,以排尽装置A和B中含有的二氧化碳,再接上装置C和D;
(6)待装置A中的反应结束后,再一次打开止水夹K,继续往装置通入已除去CO2的空气一会儿,这样做是为了将生成的二氧化碳完全吸收,否则会导致结果偏小;装置D的作用是防止空气中的二氧化碳和水蒸气进入装置C,所以若没有装置D,将会使测定结果偏大.


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:初中化学 来源: 题型:
【题目】为研究盐酸、氢氧化钙两种物质的化学性质,做了如图所示的6个实验.
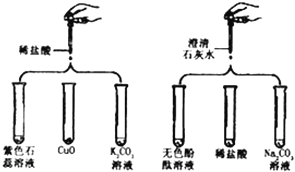
(1)实验后某试管中为蓝色溶液,该试管中发生反应的化学方程式为: .
(2)实验后某试管中为红色溶液,向其中再加入足量的一种液体后溶液变为无色.由此推断,该试管中最初盛有的物质是 .
(3)实验后某试管的底部有白色固体,过滤后向滤液中滴加稀盐酸,一段时间后有气泡出现.由此推断,该试管中最初发生反应的化学方程为 .
(4)实验后某试管中只得到无色溶液,向其中加入足量的Na2C03溶液,无明显变化.由此推断,该试管中最初发生反应的化学方程式为 .
(5)实验结束后,把6支试管中的所有液体集中倒入一个大烧杯中,大烧杯中的溶液呈红色.此烧杯的溶液中所含的溶质是 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列判断错误的是( )
A.汽油清洗油污是溶解现象
B.“真金不怕火炼”说明金的熔点高
C.集中回收废旧电池能减少土壤污染
D.煤制成蜂窝煤是为了提高燃烧效率
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如图所示,下列叙述正确的是( )
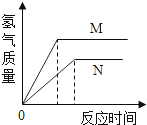
A.M、N两种金属中较活泼的是N B.生成H2的质量M<N
C.相对原子质量较大的是N D.产生H2的速率N>M
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com