
| 物质 | X | Y | Z | Q |
| 反应前质量(g) | 20 | 2 | 1 | 37 |
| 反应后质量( g) | 未测 | 32 | 1 | 12 |
| A. | 物质Z可能是该反应的催化剂 | B. | 反应后物质X的质量为15g | ||
| C. | 反应中Y.Q的质量比是6:5 | D. | 物质Y一定是催化剂 |
分析 根据质量守恒定律进行分析,反应后质量增加的是生成物,减少的是反应物,由表格信息可知反应后Y质量增加了32g-2g=30g,是生成物;Q质量减少了37g-12g=25g,是反应物;而Z质量应该不变,可能做催化剂,故X应是反应物,质量减少了30g-25g=5g克,故未测值为20-5g=15g;参加反应的X和Q等于生成的Y质量.所以推断,而反应物是X和Q,生成物是Y,所以是化合反应,根据质量关系即可推出一些量之间的关系.
解答 解:
根据质量守恒定律进行分析,反应后质量增加的是生成物,减少的是反应物,由表格信息可知反应后Y质量增加了32g-2g=30g,是生成物;Q质量减少了37g-12g=25g,是反应物;而Z质量应该不变,可能做催化剂,故X应是反应物,质量减少了30g-25g=5g克,故未测值为20-5g=15g;参加反应的X和Q等于生成的Y质量.所以推断,而反应物是X和Q,生成物是Y,所以是化合反应.
A、由分析可知:Z质量应该不变,可能做催化剂,说法正确;
B、由分析可知:X应是反应物,质量减少了30g-25g=5g克,故未测值为20-5g=15g,说法正确;
C、反应后中Y.Q的质量比为(32g-2g):(37g-12g)=6:5,说法正确;
D、由表格信息可知反应后Y质量增加了32g-2g=30g,为生成物,则物质Y一定不是催化剂,说法错误.
故选:D.
点评 解此题需根据质量守恒定律,认真分析各物质的质量变化情况,仔细推敲,即可求解.


 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:初中化学 来源: 题型:解答题
 汽车既给生活带来了便利,但也让我们的生活环境越来越糟糕,人类必须想出一个较为切实可行的办法来解决这个问题.发展太阳能汽车或许是其中-个解决途径.请回答下列问题:
汽车既给生活带来了便利,但也让我们的生活环境越来越糟糕,人类必须想出一个较为切实可行的办法来解决这个问题.发展太阳能汽车或许是其中-个解决途径.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
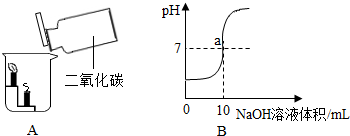
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 变质食品中常含有霉菌毒素,不可食用 | |
| B. | 食用甲醛水溶液浸泡过的鸭肠毛肚 | |
| C. | 为了自己和他人的健康,拒绝烟草,远离毒品 | |
| D. | 少年儿童不能盲目吃各种营养补品 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 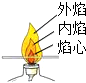 比较火焰各层温度 | B. | 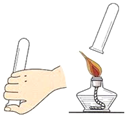 检验氢气的纯度 | ||
| C. | 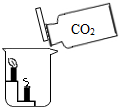 验证CO2的密度比空气大 | D. | 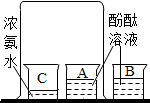 探究空气的组成成分 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 通过煮沸方法使硬水软化 | |
| B. | NaCl和NaNO2(亚硝酸钠)都有咸味,都可用作食物的调味品 | |
| C. | 在发酵的面团中加入小苏打以提高馒头的口感和除去酸味 | |
| D. | 加热,观察外形变化鉴别热塑性塑料和热固性塑料 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com