
【题目】某固体粉末可能含有碳酸钙、氧化铜、氧化铁、木炭粉中的几种,取mg该固体粉末按下列流程进行实验(本流程涉及到的反应均为初中化学常见的反应,且各步均恰好完全反应)。
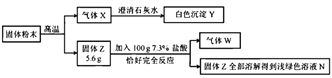
下列说法中正确的是
A. 溶液N中只含一种溶质
B. 原固体粉末中可能含有碳酸钙
C. 白色沉淀Y一定是碳酸钙,气体W一定是氢气
D. 原固体粉末中一定没有氧化铜,一定含有碳酸钙
【答案】BC
【解析】
能使澄清石灰水变浑浊的气体是二氧化碳,所以X是CO2,二氧化碳与澄清石灰水反应生成碳酸钙,Y是CaCO3;N是浅绿色溶液,N中含有Fe2+,固体粉末中含有氧化铁、木炭粉,3C+2Fe2O3 ![]() 4Fe+3CO2↑,Fe +2HCl== FeCl2+H2↑,所以w是氢气。则固体粉末中一定含有氧化铁、木炭粉,可能含有碳酸钙,因为固体Z完全溶于酸,氧化铜和碳反应生成的铜不与酸反应,故粉末中无氧化铜。A. 溶液N中含 FeCl2,CaO + 2HCl == CaCl2 + H2O,可能含CaCl2 ,错误;B. 原固体粉末中可能含有碳酸钙,正确;C. 白色沉淀Y一定是碳酸钙,气体W一定是氢气,正确;D. 氧化铜和碳反应生成的铜不与酸反应,固体Z完全溶于酸,所以原固体粉末中一定没有氧化铜,可能含有碳酸钙,错误。故选BC。
4Fe+3CO2↑,Fe +2HCl== FeCl2+H2↑,所以w是氢气。则固体粉末中一定含有氧化铁、木炭粉,可能含有碳酸钙,因为固体Z完全溶于酸,氧化铜和碳反应生成的铜不与酸反应,故粉末中无氧化铜。A. 溶液N中含 FeCl2,CaO + 2HCl == CaCl2 + H2O,可能含CaCl2 ,错误;B. 原固体粉末中可能含有碳酸钙,正确;C. 白色沉淀Y一定是碳酸钙,气体W一定是氢气,正确;D. 氧化铜和碳反应生成的铜不与酸反应,固体Z完全溶于酸,所以原固体粉末中一定没有氧化铜,可能含有碳酸钙,错误。故选BC。


科目:初中化学 来源: 题型:
【题目】如图是某品牌自行车的示意图。请根据题目提供的信息回答问题:
(1)图中标示的三种材料中属于合成材料的是________(填序号)。
(2)请用微粒的基本性质解释用打气筒给自行车打气,空气能被压入车胎内的原因:_________________。
(3)下列空气成分中与钢铁生锈有关的物质是________(填字母)。
A 水 B 氧气 C 氮气 D 二氧化碳
(4)铁锈的主要成分是Fe2O3,请写出用稀硫酸除去铁锈的化学方程式_________________。
(5)金属防锈十分重要!请你就自行车使用过程,如何有效地防止自行车零部件生锈,谈谈你的做法:______________________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】20℃时,在各盛有100克水的烧杯中,分别加入10克甲、乙、丙三种纯净物(不含结晶水,不与水反应),充分溶解后,结果如图。下列说法正确的是( )
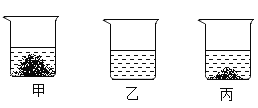
A. 所得溶液可能都是饱和溶液
B. 20℃时,乙溶液的溶质质量最小
C. 溶液溶质的质量分数:甲>丙>乙
D. 升高温度,溶液溶质的质量分数一定变大
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有氧化铜、氢氧化铜和硫酸铜的混合物20克,加入100克9.8%的稀硫酸恰好完全反应,反应结束后蒸发,所得硫酸铜的质量可能是( )
A. 35克B. 16克C. 27克D. 30克
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙、丁四种物质在反应前后的质量关系如图所示,下列有关说法错误的是
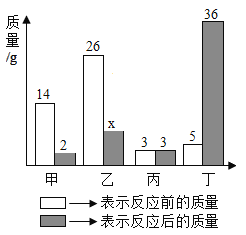
A. 参加反应的甲和乙质量比为2:7 B. 丙可能是该反应的催化剂
C. 丁一定是化合物 D. x的值是7
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】对销售的化肥,国家有明确的质量要求。某兴趣小组对市售的某钾肥进行了检测,称取2.0g样品放入烧杯中,加入适量的水溶解后,逐滴加入10%的BaCl2溶液,产生沉淀的质量与所加入BaCl2溶液质量的关系如图1所示(假定杂质不参加反应)。
已知:K2SO4+BaCl2═BaSO4↓+2KC1。

(1)20.8g BaCl2溶被中所含溶质的质量为_____g。
(2)通过计算,判断该钾肥中K2SO4的质量分数是否符合图2的包装说明________?(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(4分)某兴趣小组进行粗盐提纯并配制NaCl溶液,请回答下列问题:
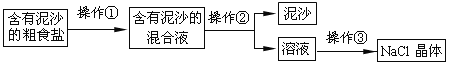
(1)操作①、②、③依次为下图中的(填字母) 。
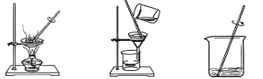
![]()
(2)若NaCl的产率偏低(![]() ),则可能的原因是(填字母) 。
),则可能的原因是(填字母) 。
A.过滤时滤纸有破损
B.蒸发时有固体溅出
C.溶解含有泥沙的粗食盐时,加入的水量不足
(3)用上述实验所得NaCl晶体配制5%NaCl溶液50.0g,需称取NaCl g,配制时需要的玻璃仪器有烧杯、玻璃棒、滴管、 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向盛有193.8g硫酸铜溶液的烧杯中,逐滴加入质量分数为8%的氢氧化钠溶液,反应过程中生成沉淀的质量与所用氢氧化钠溶液质量关系如图所示。(化学方程式为:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4)
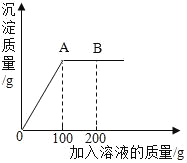
(1)恰好完全反应时,所消耗氢氧化钠溶液中含溶质的质量为_____克。
(2)恰好完全反应时溶液中溶质的质量分数_____。
(3)B点时溶液中含有的溶质有_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化工厂用废硫酸制备硫酸钾的流程如下,请回答下列问题:
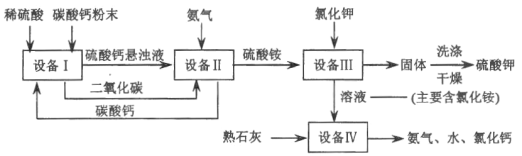
资料:己知20℃时硫酸铵、硫酸钾溶解度如下表:
物质 | 硫酸钾 | 氯化钾 | 氯化铵 | 硫酸铵 |
溶解度/g(20℃) | 11.1 | 34.2 | 37.2 | 75.4 |
(1)“设备I”中将碳酸钙研成粉末的目的是_____。
(2)“设备II”中发生的化学反应方程式是_____。
(3)“设备III”中发生的化学反应方程式是_____。反应物之一硫酸铵[(NH4)2SO4)]中氮元素的化合价为_____。洗涤从“设备III”中得到的固体时,不用水而是用饱和硫酸钾溶液,其目的是_____。
(4)上述流程中可循环使用的物质除水外,还有_____(填写化学式).
(5)根据本题所给的信息推断实验室_____(能、不能)用碳酸钙粉末和稀硫酸反应制备得到二氧化碳。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com