�⣺��1������a���������ȵľƾ��ƣ�����b��������ˮ������ˮ�ۣ�����ƾ��ƣ�ˮ�ۣ�
��2��Aװ���ʺ��ڸ���������ȷֽ�����ȡ����������������ȷֽ���������ء��������̺��������䷴Ӧ����ʽΪ��2KMnO
4
K
2MnO
4+MnO
2+O
2����
���2KMnO
4
K
2MnO
4+MnO
2+O
2����
��3������Ŀ����Ϣ��֪�����ֹ��巴Ӧ����Ҫ���ȣ��������ܶȱȿ���С�Ҽ�������ˮ�����壬����ֻ��Ӧ�������ſ�������
���A��D��
��4�������ǿ����к�����ߵ����壬������������ͭ�ڼ��ȵ������£�����ͭ�͵�����ˮ���䷴Ӧ����ʽΪ��2NH
3+3CuO

3Cu+N
2+3H
2O��
���2NH
3+3CuO

3Cu+N
2+3H
2O��
��5�����ڴ�����ȼ�յ������ǣ�����ȼ�ա��������䡢�ų����������ɺ�ɫ���壻����������Ӧ���ɵ��������������䷴Ӧ����ʽΪ��3Fe+2O
2
Fe
3O
4��
�������ȼ�գ�3Fe+2O
2
Fe
3O
4��
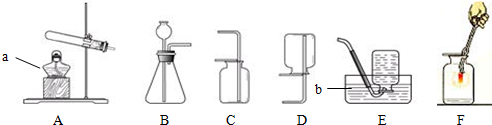
��������1������ʵ���ҳ������������ƺ���;������գ�
��2��Aװ��������ȡ��Ӧ���ǹ��壬��Ӧ�����Ǽ��ȵ����壻
��3����Ӧ�ķ���װ�õ�ѡȡ������+�� ���ȡ��ͣ���Ϊ��������һ���ܶȱȿ���С�Ҽ�������ˮ�����塱������ֻ��Ӧ�������ſ������ռ���
��4����Ϊ�����к�����ߵ������ǵ�����������������ͭ�ڼ��ȵ������£�����ͭ�͵�����ˮ�����ҳ������С������6��Ȼ������ԭ����ƽ���ɣ�
��5�����ڴ�����ȼ�յ������ǣ�����ȼ�ա��������䡢�ų����������ɺ�ɫ���壮
���������������Ŀ��Ҫ��dz�������ķ���װ�ú��ռ�װ����ѡȡ�����������ݣ����������������Լ�������ʵ������ȡ��������ʱ����Ū��ͼʾ��Ϣ�ȵȣ�Ȼ���ʵ�顢�����龰��Ϣ��ϸ�µط��������ʵ��ͼ�ȣ��������������ȡԭ������װ��ѡ�䡢�жϻ���ѡ������ķ���װ�ã��ٸ���������ܽ��ԡ��ܶȼ����Ƿ���ˮ���߿���������Ӧ�����жϡ�ѡ���ռ�װ�ã�

 K2MnO4+MnO2+O2����
K2MnO4+MnO2+O2���� K2MnO4+MnO2+O2����
K2MnO4+MnO2+O2���� 3Cu+N2+3H2O��
3Cu+N2+3H2O�� 3Cu+N2+3H2O��
3Cu+N2+3H2O�� Fe3O4��
Fe3O4�� Fe3O4��
Fe3O4��




