
����Ŀ����3�֣��綯���г���С�����Ƚ�ͨ�����ж���Ϊ���ṩ���ܵ�Ǧ���أ��ֳơ���ƿ�����������ŵ��ǿ��Գ��ѭ��ʹ�ã���ƿ�ڷ����Ļ�ѧ��Ӧ�ǣ�
PbO2������+ 2H2SO4 + Pb = 2PbSO4��+ 2H2O
ij��ƿ��װ��36%��ϡ����1200 g����ƿ����ʱ��310��5 g��Ǧ�μӷ�Ӧ���Լ��㣺
��1��ԭϡ�������������ʵ������� g��
��2����ƿ����ʱ���������������
��3����Ӧ��������Һ�����ʵ��������������������ȷ��0��01%��
���𰸡� ��1��432g ; (2)294g ;(3)14��36g
��������
�����������1��ԭ��m(����)=1200g��36%=432 g����������������������������������������1����
��2���⣺�������Ĵ�ϡ�������Ϊx��ͬʱ����ˮ������Ϊy��
PbO2������+ 2H2SO4+Pb = 2PbSO4��+ 2H2O
196 207 36
x 310��5g y
![]()
x =294g ����������������������������������������1����
![]()
y=54g
ʣ��m(����)=432g��294g=138g
ʣ��m(��Һ)=1200g��294g+54g=960g
��3��ʣ��H2SO4��Һ�����ʵ���������=![]() x 100% =14��38% ������1����
x 100% =14��38% ������1����
��������ϡ����������Ϊ294g����ʱ��ƿ��������Һ�����ʵ�����������14��38%��
����:���ݻ�ѧ����ʽ�ļ��㡢�й���Һ�ļ���


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����彡���벻����ѧ�������й�������ȷ����
A������Ǧ���⡢��������������Ԫ��
B����ȩ���ݹ��ĺ���Ʒ�����ڳ���ʳ����
C��ά������20���֣������������ڲ��ܺϳɣ���Ҫ��ʳ����ȡ
D��ù����ס�����ȵ�280��ʳ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����5�֣��ƵĻ��������ճ�������Ӧ�ù㷺��
��1����Ԫ�����ڱ��У���Ԫ�ص���Ϣ��ͼ��ʾ����Ԫ�ص����ԭ������Ϊ_____��
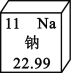
��2���������ƿ�������ɱ������������Ƶ�������_____��дһ�֣���
��3���������ƣ�NaClO����84����Һ����Ч�ɷ֣�������������Ԫ�صĻ��ϼ�Ϊ_____��
��4��̼�������Ƿ��ͷ۵���Ҫ�ɷ֣�̼�����������ᷴӦ�Ļ�ѧ����ʽΪ_________��
��5�������ƣ�NaNH2���Ǻϳ�ά����A��ԭ�ϡ���ҵ�����������ƵĻ�ѧ��Ӧ����ʽΪ
2Na + 2NH3 ��2NaNH2 + H2�����÷�Ӧ���ڻ�����Ӧ�����е�_______��Ӧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ��Ӧ�����кͷ�Ӧ����
A��CaO+2HCl��CaCl2+H2O
B��2NaOH+CO2��Na2CO3+H2O
C��CaCO3+2HCl��CaCl2+H2O+CO2��
D��Ca(OH)2+2HCl��CaCl2+2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����5�֣���Ԫ�ض��������������Ҫ���塣
��1������ȱ�ƻ�����ļ����� ������ĸ��ţ���
A����������������Ͳ� B�������˻�����ƶѪ C�������˻������������
��2��A��B��C�dz����ĺ��ƻ����ת����ϵ��ͼ��ʾ������A��B��������Ԫ����ɡ�
![]()
��A���׳��� ������ũҵ�ϵ���;�� ��
����B����Ȼʯ���У�����Ϊ�������ϵ��� ��
��B��C�Ļ�ѧ����ʽ�� ����дһ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ƣ�NaNO2���������ʳ�κ����ƣ�����ζ����ʳ���ж����������ǵ�һ�ַ����ǣ������߷ֱ���ȵ�320�������ֽ����ʳ�Σ��ֽܷⲢ�ų�һ�־��д̼�����ζ��������������ơ������������( )
A��NO2 B��SO2 C��NH3 D��N2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����8�֣��������������Ʒ��ij��ȤС��ͬѧ��ijƷ����������չ������̽������ش�
���⡣

����֪���ϡ�
��SiO2������ˮ���Ҳ����ᷴӦ ��K12�����͡��㾫�Ⱦ�������ˮ
��ʵ��̽����
����ȡһС�����࣬��������ˮ����ֽ�����ã�����ϲ���Һ��pHΪ8.3����������� �ԡ�
������ȤС��ͬѧ���������ʵ�鷽����������3��ʵ�顣ͨ������SiO2�������Ӷ�ȷ����������SiO2������������ʵ��������£�
��ȷ��ȡ2.0g������壬������ˮ����ܽⲢ���ˡ�
��������ת�����ձ��У��������ϡ���ᣬ������ Ϊֹ��
��______��ϴ�ӡ����ﲢ�����õ�ʣ�������������������
ʵ���� | 1 | 2 | 3 |
ʵ��ǰ��g�� | 2.00 | 2.00 | 2.00 |
ʵ���g�� | 0.43 | 0.44 | 0.45 |
������ʵ�����ݽ��м��㣬��������SiO2
����������Ϊ %��
����˼ʵ����̡�
A.�������м�����ˮ��Ŀ���� ��
B.�������з�����Ӧ�Ļ�ѧ����ʽΪ ��
C.��β���ʵ�����ݵ�Ŀ���� ��
D.����֤���������������������ѡ����Լ��� ������д�����ͬ���������ʣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����6�֣�������ͼ�ش����⡣
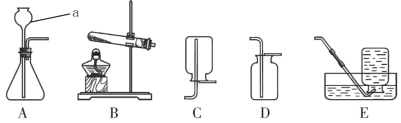
��1��ʵ������a�������� ��
��2��ʵ�����ø��������ȡ�����Ļ�ѧ����ʽΪ �����õķ���װ���� ����װ��D�ռ�������ԭ���� ��
��3��ʵ������ȡ���ռ�������̼ѡ�õ�װ���� ����Ӧ�Ļ�ѧ����ʽΪ
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͨ���Ų�ķ��������жϳ���IJ��أ������ܹ��ŵ������ԭ���ǣ� ��
A�����Ӽ��м�� B�������ڲ��ϵ��˶�
C�����ӵ��������������С D����������ԭ�ӹ��ɵ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com